摘要
高龄患者进行高危手术如腹部大血管手术的手术风险高,围术期管理困难,需从术前基础疾病评估、手术重要环节的预计、术中容量管理、突发事件处理、血流动力学监测、术后并发症预防及处理等要点入手,以安全有效的完成手术。术前准备需要合理选用各种监测仪器、保温措施、预备血液制品、预先与外科医师充分沟通,了解可能影响血流动力学的重要手术操作;术中主要通过Flotrac对心排血量及每搏量变异度进行监测,再结合其他监测指标进行目标导向液体治疗,避免过多的液体及血液制品输注造成脏器过度负担。通过动脉血气分析的监测,及时调整内环境,从而减少术中和术后并发症的发生。采用综合性麻醉管理,可确保术前准备充分,术中监测指标全面,病情变化及时控制,急救迅速有效,是值得临床推广应用的有效管理方法。
【关键词】 大血管;癌栓;目标导向液体治疗;动脉压力波形心排血量监测;每搏量变异度
1. 病例介绍
患者男,77岁,身高173 cm,体重76 kg。因“体检发现腹腔内肿瘤1周”入院。既往高血压病史,服用非洛地平缓释片,平素血压控制在130/80 mm Hg(1 mm Hg=0.133 kPa)左右。
实验室检查:血常规:血红蛋白(Hb)122 g/L,血小板(PLT)73×109/L;凝血功能:凝血酶原时间(PT)17 s,活化部分凝血活酶时间(APTT)48.5 s(较对照延长15 s),国际标准化比值(INR)1.4;肝功能:正常;心电图:窦性心律,左心室高电压;胸部X线摄影:心肺未见明显异常;心脏彩超:二尖瓣少量反流,射血分数(EF)63%,短轴收缩率(FS)30%;肺功能:肺通气功能轻度减退。计算机体层摄影(CT)示:右肝占位性病变,肝静脉入下腔静脉口占位;腹部超声:肝静脉、下腔静脉入口4.0 cm×2.6 cm絮状回声。诊断:①下腔静脉占位性质待查,肝癌癌栓?②高血压病。拟施手术:下腔静脉切开取栓术备下腔静脉置换术。
2. 麻醉管理
2.1 术前评估
2.1.1 实际麻醉术前评估
患者高龄,既往有高血压病史,血压控制理想。术前检查未发现有心脏、大血管的慢性疾病或代谢性疾病。血常规提示血小板减少,凝血指标PT、APTT、INR延长,考虑可能与肝脏原发疾病导致的凝血和止血功能异常相关。此外,在肝静脉入下腔静脉口存在占位,肝癌癌栓待排,为了去除占位改善血流,术中可能会在肝上行下腔静脉阻断,这会导致连同门静脉的回流同时被阻断,短时间内回心血量骤减,可能造成循环在短期内出现巨大的波动。同时下腔静脉切开取栓时,因为存在丰富的侧枝循环出血可能较多,术前需充分准备血液制品,并考虑采取精确而灵敏的监测方法监测循环的变化。下腔静脉癌栓在围术期可能发生脱落造成肺栓塞,手术中如果下腔静脉撕裂也可能发生空气栓塞,均需要提高警惕加以预防。
2.1.2 术前评估分析
2.1.2.1 高血压患者术前评估[1]
对高血压患者需要进行详细的术前检查,明确引起高血压的原因、高血压的程度、靶器官的受累情况、治疗药物及血压控制情况。
高血压的程度 1、2级高血压者(血压<180/110 mm Hg)麻醉危险性与一般患者相仿,手术并不增加围术期心血管并发症的发生危险。而对于3级高血压(血压≥180/110 mm Hg)者,围术期发生心肌缺血、心力衰竭及脑血管意外的危险明显增加。
靶器官的受累情况高血压伴重要脏器功能损害者,麻醉手术的危险性显著增加。术前应评估患者有无心绞痛、左心室肥厚、充血性心力衰竭、脑血管疾病、卒中、外周血管疾病、肾功能不全等重要脏器受累。
拟行手术的危险程度① 高危手术(心脏危险性>5%):急诊大手术,尤其是老年人;主动脉或其他大血管手术;外周血管手术;长时间手术(>4 h)、大量体液移位和(或)失血较多等。本例患者手术属于高危手术;②中危手术(心脏危险性<5%):颈动脉内膜剥离术;头颈部手术;腹腔内或胸腔内手术;矫形外科手术;前列腺手术等;③低危手术(心脏危险性<1%):内镜检查;浅表手术;白内障手术;乳腺手术等。
血压控制目标除紧急手术外,择期手术一般应在血压得到控制之后进行。择期手术的降压目标以中青年患者血压控制在<130/85 mm Hg,老年患者控制在<140/90 mm Hg为宜。对合并糖尿病的高血压患者,应降至130/80 mm Hg以下。对高血压合并慢性肾脏病者,血压应控制在130/80 mm Hg甚至125/75 mm Hg以下。对于急诊手术患者,可在进行术前准备的同时适当控制血压。对血压>180/100 mm Hg的患者,可在严密的监测下,行控制性降压,调整血压至140/90 mm Hg。
血压控制不佳时是否推迟手术美国心脏病学会/美国心脏学会(ACC/AHA)在2007年发表的指南中指出:轻至中度高血压者(<180/110 mm Hg)可以进行手术,但建议重度高血压者(≥180/110 mm Hg)应延期行择期手术。但因为缺乏大样本研究结果,目前尚无明确推迟手术的高血压阈值。当前推迟手术的主要理由有两点:①推迟手术可以改善终末器官的损害;②高血压患者疑有靶器官损害需要进一步评估。
常用抗高血压药物及其对麻醉的影响[2] 根据最新的ACC/AHA关于围术期心血管评估的指导意见,常用抗高血压药物在术前的管理方法如下:
利尿剂:可能会加重手术相关的体液缺失,目前主张术前2~3 d停用。长期服用利尿剂患者易发生低钾血症,围术期要严密监测血钾,及时补钾。
β受体阻滞剂:是目前临床应用较多的一类药,可降低术后心房颤动发生率、非心脏手术心血管并发症的发生率和病死率,适用于术前血压控制。长期服用β受体阻滞剂的患者应当持续用药至术晨,避免术前突然停药导致术中心率的反跳。围术期要维持此类药物使用的种类和剂量,无法口服药物的高血压患者应经肠道外给药。
钙通道阻滞剂:能增强静脉麻醉药、吸入麻醉药、肌肉松弛药和镇痛药的作用,不主张术前停药,可持续用药至术晨。
血管紧张素转化酶抑制剂(angiotensin converting enzyme inhibitors,ACEI)和血管紧张素Ⅱ受体阻滞剂(angiotensin receptor blocker,ARB)类药物:可能会加重手术相关的体液缺失,增加术中发生低血压的危险。ACEI作用缓和,术前不必停药。ARB类药物氯沙坦及其代谢产物羟基酸能抑制血管紧张素Ⅱ受体和血管紧张素Ⅰ受体,且羟基酸比氯沙坦效力大10~40倍,目前推荐手术当天停用。
交感神经抑制剂可乐定:是中枢性抗高血压药,若术前突然停药,术中血压严重反跳,甚至诱发高血压危象,术前不必停用。
利血平:主要通过消耗外周交感神经末梢的儿茶酚胺而发挥作用。服用该药的患者对麻醉药的心血管抑制作用非常敏感,术中很容易发生血压下降和心率减慢。术中发生低血压,应该选用直接作用的拟交感神经药物如肾上腺素、去甲肾上腺素。对于长期服用利血平患者最好术前7 d停服并改用其他抗高血压药物。
2.1.2.2 下腔静脉阻断相关并发症
根据术前影像学检查结果,预计术中会阻断下腔静脉行切开取栓操作。要在肝外分离和阻断下腔静脉,尤其是肝上下腔静脉,风险较大,一旦撕裂,就意味着大出血和空气栓塞。因此麻醉需做好应对准备。
下腔静脉阻断部位不同对循环的影响[3] 下腔静脉阻断又分为肝下下腔静脉阻断和单纯完全下腔静脉阻断两种。在肝脏切除手术中进行肝下下腔静脉阻断的主要目的为降低中心静脉压(CVP),从而大大减少肝切过程中来自肝静脉的逆向出血。有研究表明,可以降低CVP约4 cm H2O(1 cm H2O=0.098 kPa)。而当肿瘤侵犯肝段下腔静脉时,可以采用单纯完全下腔静脉阻断。肝上下腔静脉阻断因为连同门静脉的血流一并阻断,会造成回心血量骤减,应当事先做好充分的扩容,在阻断后要有经上肢回流入心脏的快速补液途径来维持心脏的前负荷,以避免心脏出现“空虚”导致血压过低无法维持重要脏器的基本灌注,甚至使心功能不佳的患者出现心搏骤停。本例患者因癌占位位置较高,术中拟行肝上下腔静脉阻断。
空气栓塞当5 mL以上的空气进入人体血管并导致心脏、肺、脑等部位发生栓塞时引起的一系列的症状,称为空气栓塞。某些外科手术和诊疗操作如体外循环下心内直视手术、肝脏移植、血液透析或加压输血输液均是导致空气栓塞常见的原因。下腔静脉阻断后切开取栓过程也是发生空气栓塞的高危手术操作。
病理生理特点:空气进入静脉-右心房-右心室,少量空气进入肺动脉后分散到肺小动脉内,直至毛细血管。大量空气随着心脏跳动,使空气与血液混合成泡沫状,如进入肺动脉,阻塞肺动脉分支,阻塞血液在肺内运行,引起严重的缺氧甚至死亡;进入冠状动脉,阻塞冠状脉脉循环,引起严重的心功能障碍也会导致死亡;进入脑部则损害中枢神经系统。
临床表现:少量空气栓塞可无表现。气体较多时,患者表现为肺动脉高压,右心衰竭、CVP明显升高、呼气末二氧化碳分压(PETCO2)下降、动脉压下降,低氧血症和高碳酸血症。严重时出现心搏骤停,甚至突然死亡。
监测:①经食管超声心动图(TEE):TEE是监测心内气体栓子的最敏感的方法。一般直径小于2 mm的栓子都能直接清楚地显示,可敏感地检测节段性室壁运动异常,还能清晰显示心内分流,为反常栓塞提供诊断依据;②PETCO2和血流动力学:少量空气栓塞可无表现。气体较多时,患者表现为肺动脉高压,右心衰竭、CVP升高、PETCO2下降、动脉压下降,低氧血症和高碳酸血症;③经食管或心前区多普勒超声血流探查和听诊、呼气末氮气(ETN2)等。
治疗:①气栓症较血栓症和其他原因的栓塞预后要好。一旦发现有空气栓塞,应立即通告手术医师,暂停手术,查找空气入血的原因;②停用氧化亚氮(N2O),予纯氧吸入;③经中心静脉导管从右心抽出空气是理想的处理方法;④予升压药维持血压;⑤调整为头低左侧卧位;⑥心搏骤停按心肺复苏抢救。
2.1.2.3 肿瘤引起的肺栓塞
肿瘤引起的肺栓塞与其他原因所致的肺栓塞无明显临床区别。临床症状的轻、重程度取决于栓子堵塞动脉的大小、受累动脉的横截面积、涉及肺段数目、发生速度及患者本身心、肺功能状态等。从无症状到猝死,复杂而多变,栓塞面积<20%可能无症状。术前可根据肿瘤癌栓生长的部位考虑放置近心端的下腔静脉滤器,以免癌栓脱落引起肺栓塞[4]。
2.2 术中管理
高龄患者进行高危手术,手术风险高,术中循环受手术影响剧烈,出入量大,血压容易波动。因此术中需严密监测,维持循环稳定及水电解质酸碱平衡,避免低血压,保证重要脏器的灌注。存在大量出血风险的患者同时也要考虑麻醉药经失血丢失的问题,应通过适当的监测保证一定的麻醉深度。
2.2.1 实际麻醉术中管理
入室后行常规无创血压、心电图、氧饱和度、脑电双频指数(BIS)等监测,开放外周静脉18 G,连接输血加温导管。基础状态:血压138/80 mm Hg,心率82次/min,脉搏血氧饱和度(SpO2)96%。
2.2.1.1 麻醉诱导与监测设备的建立
诱导前给予患者醋酸林格氏液500 mL静脉滴注扩容。然后依次给予咪达唑仑2 mg,依托咪酯30 mg,舒芬太尼35 μg,罗库溴铵50 mg,起效后行气管内插管,予呼吸机辅助呼吸。潮气量540 mL,呼吸频率12次/min。
经右侧颈内静脉穿刺置入双腔深静脉导管,监测CVP。经左桡动脉建立有创动脉血压监测,并连接Flotrac传感器,行动脉压力波形心排血量(APCO)监测,持续监测心排血量及心排血指数(CO/CI)、每搏量及每搏量指数(SV/SVI)、每搏量变异度(stroke volume variation,SVV)。此外监测BIS、鼻咽温,监测CVP。留置导尿管,接尿瓶,监测尿量。
2.2.1.2 麻醉维持
术中给予2%七氟烷吸入麻醉,呼出气体最低肺泡有效浓度(MAC)监测提示在1.2左右,间断给予苯磺酸顺阿曲库铵及舒芬太尼静脉注射,并持续微泵静注右美托咪啶0.4 μg·kg-1·h-1辅助镇静和镇痛。
2.2.1.3 术中突发事件应对及处理
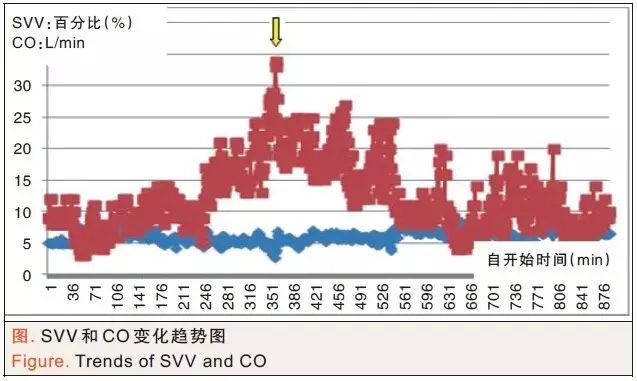
循环及容量管理术中绝大部分时间循环稳定,收缩压90~130 mm Hg,舒张压50~80 mm Hg,平均动脉压60~100 mm Hg。术中在下腔静脉阻断后切开血管取栓时出现一过性CO骤然降低和失血量增加,10 min内累计失血1500 mL,血压最低降至58/40 mm Hg,此时SVV为术中最高达到34%,CO降至最低2.9 L/min(SVV、CO变化趋势见图,箭头所指为发生低CO时刻)。在加压快速输血补液的同时间断给予去氧肾上腺素100 μg×3次。低血压时间总计小于5 min,随后迅速恢复至106/62 mm Hg。术中共计失血3000 mL,输注晶体液1200 mL,胶体液1500 mL,红细胞悬液1600 mL,血浆800 mL,血小板20 U。尿量300 mL。
内环境调整根据血气分析结果,调整呼吸参数,补充钾、钙离子等电解质,应用碳酸氢钠维持酸碱度(pH)>7.20。监测乳酸值,应用醋酸林格氏液替代乳酸林格氏液,尽量减少乳酸的摄入。血气分析变化见表。
纠正凝血功能[5] 肝病患者的凝血异常通常由凝血系统和纤维蛋白溶解(纤溶)系统异常、血小板数量及其功能下降所致。肝脏病变时肝细胞合成凝血因子(除钙离子和组织因子外的其他凝血因子)的能力减低,特别是Vit K相关性的凝血因子(Ⅱ、Ⅶ、Ⅸ、Ⅹ)可能受到明显影响,同时也会导致抗凝蛋白(抗凝血酶、肝素辅助因子Ⅱ、蛋白C、蛋白S等)的合成能力降低。而肝脏疾病常并发纤溶亢进甚至弥散性血管内凝血(DIC),此时血浆中纤溶酶水平增高,纤溶酶不仅可以水解纤维蛋白(原),而且可以水解多个凝血因子(因子Ⅶ、Ⅸ、Ⅹ、Ⅺ、Ⅻ),同时也消耗大量的抗凝蛋白,致使凝血因子或抗凝蛋白的血浆水平降低,易出现凝血和抗凝机制紊乱。考虑到患者术前血小板数量偏低,PT、APTT延长,术中短时间失血量较大,进一步加重了凝血因子和血小板的丢失,遂给予输注新鲜冰冻血浆800 mL以补充凝血因子和纤维蛋白原,血小板20 U补充血小板,根据血钙水平补充钙剂2 g,以改善凝血功能。
体温监控及保护手术全程行鼻温监控,通过输血加温导管,对静脉输注的液体、血液制品进行加温,同时予患者下半身被覆加温毯,减少体热丢失。
2.2.2 术中麻醉管理分析
2.2.2.1 容量监测的方法[6]
无创血流动力学监测① 心率:麻醉手术期间患者心率突然或逐渐加快,可能是低血容量的早期表现,但需与手术刺激、麻醉偏浅、血管活性药物作用和心脏功能异常等其他原因进行鉴别。
②无创血压:一般维持术中收缩压大于90 mm Hg或平均动脉压大于60 mm Hg;老年、高血压和重症脓毒症患者,血压应该维持较高水平。血压下降除外麻醉过浅或手术操作刺激,应考虑循环血容量不足,但不是容量不足的敏感指标。
③尿量、颈静脉充盈度、四肢皮肤色泽和温度:尿量是反应肾灌注和微循环灌注状况可参考的指标,术中尿量应维持在0.5 mL·kg-1·h-1以上,但麻醉手术期间抗利尿激素分泌增加,可影响机体排尿,故尿量并不能及时和准确地反映血容量的变化。颈静脉充盈度、四肢皮肤色泽与温度也是术中判断血容量状态的指标。
④ SpO2:SpO2是围术期的重要监测项目,在组织血流灌注良好的情况下,SpO2波形随呼吸变化则提示患者血容量不足。
⑤ TEE:可有效评估心脏充盈程度,能准确判定心脏前负荷和心脏功能,现已逐渐成为重症患者术中重要的监测项目。
有创血流动力学监测① CVP:判断血管内容量的常用监测指标。通常平卧位时压力传感器需放置于右第四肋间、腋中线水平,侧卧位时则应放置于右第四肋间,胸骨右缘水平,并在呼气末(无论自主呼吸或正压通气)记录,应重视CVP的动态变化。影响CVP的因素诸多,如心功能、正压通气、腹腔内压、手术操作等。
②肺动脉楔压(PAWP):反映左心功能和左心容量的有效指标,PAWP升高是左心室功能失调的表现之一。
③ SVV:在机械通气情况下,由于呼吸机的作用引起肺血管内血容量发生规律性的波动,导致左心室SV发生相应的波动。SV波动的差值百分比越大(SVV大),说明血容量不足,通过补液能够明显提高CO。SV波动的差值百分比越小(SVV小),说明血容量充足,通过补液不能明显提高CO,需要通过提高外周阻力、应用强心药物等其他方法来改善CO。
容量相关实验室检查① 动脉血气、电解质、血糖、胃黏膜pH(pHi)及血乳酸:在循环血容量和组织灌注不足时需及时进行动脉血气监测。也需进行及时的电解质和血糖的变化监测。血乳酸和pHi测定是评估全身以及组织灌注的有效指标,对麻醉手术患者的液体治疗具有重要的指导作用。
② Hb和血细胞比容(Hct):贫血时机体代偿机制包括:a. CO增加;b. 全身器官的血流再分布;c. 增加某些组织血管床的摄氧率;d. 调节Hb与氧的结合能力。发生术中出血量较多或液体转移量较大时,应监测Hb含量。
③凝血功能:大量输血、输液以及术野广泛渗血时,均应及时监测凝血功能。凝血功能监测包括血小板计数、PT、APTT、INR、血栓弹力图(TEG)和Sonoclot凝血,以及血小板功能分析(SCT)等。
2.2.2.2 SVV在容量监测中的作用
SVV监测的基本原理 SVV是指在一个呼吸周期中左心室SV的变异度,反应的是胸腔内压力变化引起的回心血量改变。其产生的机制是在正压机械通气时,胸腔内继发性压力的变化导致SV在吸气时升高,呼气时下降。血容量不足时,SV在呼气时相对于吸气时的下降幅度增大,导致SVV数值增大。
经外周动脉波形分析系统对动脉压力波形进行分析,应用统计分析计算脉搏压特性;通过动脉波形的上升来识别心跳周期,并计算出心率;从人口统计学资料中评估不同患者的差异性和校准血管的差异性(即顺应性和阻力);最后通过对单位时间内的血压数据和波形进行分析测得CO。
SVV在容量治疗中的作用 通过计算出的SVV值可以预测心血管系统对液体负荷的反应性,可以更准确地判断循环系统的前负荷状态,在控制呼吸时SVV的正常值是10%~13%。对于机械通气的患者来说,排除心律失常和手术操作等影响,SVV数值越大,给予容量负荷后CO增加越多,表明有效血容量就不足。当SVV>13%,就有必要行输液治疗;当SVV<10%,给予容量负荷后就很难出现CO的增加,应避免输入过多的液体。
除了SVV以外,还有其他动态血流动力学指标如脉搏压变异度(pulse pressure variation,PPV)、收缩压变异度(systolicpressure variation,SPV)、SV增量等,均能反映机体是否具有补液的反应性,即反映当前的容量状态在心室功能曲线(Frank-starling曲线)上的位置。
补液试验、被动抬腿试验、自主呼吸时CVP的波动以及超声心动图等方法也同样可以判断上述问题。补液试验通常是输注100~500 mL 或7~10 mL/kg胶体液,在10~30 min 输注完毕,SV或CO增加5%~20%被认为是具有补液反应性。被动抬腿试验是对平卧位患者,被动将双腿抬高至45°,重力使得回心血量增加150~300 mL,SV或CO增加10%~15%被认为是具有补液反应性。自主呼吸吸气时胸内压下降2 mm Hg以上伴随CVP下降1 mm Hg以上,被认为具有补液反应性。通过超声心动图则更能直观地观察心脏前负荷状态。临床上可以根据实际情况灵活应用。
SVV的局限性 SVV监测只能在机械通气下开展。机械通气的潮气量设置对SVV有明显的影响,通常要求在8 mL/kg以上。最新APCO监测可应用于心房颤动患者,但严重心律失常会影响SVV的测定,无法准确反映循环系统液体敏感性及容量状态。SVV还受外周血管阻力和气道压力变化的影响。
2.2.2.3 容量复苏的液体选择
容量复苏可选择晶体液和胶体液。
晶体液主要是用来补充细胞外液和其中的电解质,但扩容效率低、效应短暂,可引起外周水肿、肺水肿。因为紧张和应激,围术期血糖通常会升高,且由于糖利用受限和高血糖对缺血性神经系统的不利影响,除婴幼儿以外,成人一般很少使用5%葡萄糖溶液。乳酸林格氏液含有与血浆相近的电解质,是低渗液体,含有少量乳酸,故对严重颅脑损伤、脑水肿和严重肝脏功能受损患者不宜使用,可给予更接近血浆成分和理化特性的醋酸林格氏液。高渗氯化钠溶液适用于烧伤和水中毒患者,但不能过量过快使用,否则会引起溶血和中枢脑桥脱髓鞘。
胶体液的优点是维持血管内容量的效率高,持续时间长,外周水肿轻,缺点是价格昂贵,可引起凝血功能障碍、肾功能损害及诱发过敏反应。明胶对肾功能影响较小,但容易发生过敏反应。羟乙基淀粉主要的不良反应是大剂量长时间使用时引起凝血功能障碍和肾功能损害。人血白蛋白可将细胞间隙的水吸入血管内,补充血容量。
2.2.2.4 液体治疗的方案选择
液体治疗方案主要有:标准液体治疗、限制性液体治疗和目标导向液体治疗。
标准液体治疗方案中,液体补充包括五个部分:①每日正常生理需要量;②术前禁饮食所致液体缺失量和手术前累计液体缺失量;③麻醉导致的血管扩张和有效循环血容量减少;④术中失血量;⑤ 第三间隙液体丢失量。有研究显示标准液体治疗方案往往使术中输液过量,产生组织水肿并增加术后并发症发生率。
限制性液体治疗方案中,麻醉导致血管扩张和有效循环血容量不足,术中非显性失水以及第三间隙液体丢失量不予补充。有研究表明,限制性液体治疗方案,能减少肺部感染和肺水肿发生,但增加围术期低血容量的发生,缩血管药物的使用频率和用量也明显增加。













