▎药明康德内容团队报道
今日(5月10日),中国国家药品监督管理局药品审评中心(CDE)最新公示,恒瑞医药的CDK 4/6抑制剂SHR6390片的两项上市申请被纳入拟优先审评公示名单,针对的适应症为——拟联合氟维司群用于激素受体(HR)阳性、人表皮生长因子受体2(HER2)阴性的特定乳腺癌患者。
截图来源:CDE官网
CDK 4/6全称为细胞周期蛋白依赖性激酶4和6,它是驱动细胞分裂的关键调节因子。研究发现,CDK 4/6在许多癌细胞中呈现过表达的现象,导致癌细胞分裂周期失控,无限增殖。临床研究证实,超过一半的乳腺癌患者会过表达细胞周期蛋白D,且大部分为雌激素受体阳性乳腺癌患者。由于细胞周期蛋白D直接作用于CDK 4/6,因此CDK 4/6已成为HR阳性转移性乳腺癌患者的重要分子靶点。SHR6390是恒瑞医药研发的一款口服、高效、选择性的在研小分子CDK 4/6抑制剂,为1类新药。据悉,SHR6390能够选择性地抑制CDK4/6激酶活性,进而阻断CDK4/6-Rb信号通路,诱导细胞G1期的阻滞,并选择性地抑制Rb高表达肿瘤细胞的增殖,进而达到抗肿瘤的作用。优先审评公示信息显示,本次恒瑞医药SHR6390片有两个规格拟被纳入优先审评,分别为150mg和125mg。这两个申请针对的适应症均为:拟联合氟维司群用于HR阳性、HER2阴性的经内分泌治疗后进展的复发或转移性乳腺癌的治疗。
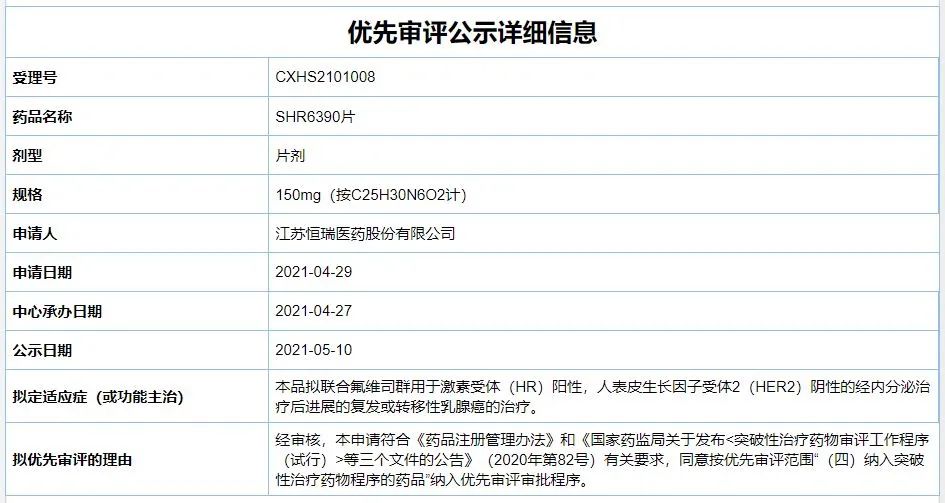
根据恒瑞医药在2020年12月发布的新闻稿,CDK 4/6抑制剂SHR6390片已在一项针对晚期乳腺癌患者的3期临床中达到主要研究终点。据介绍,这是一项名为SHR6390-III-301的多中心、随机、对照、双盲3期临床研究,旨在评估SHR6390联合氟维司群对比安慰剂联合氟维司群治疗既往接受内分泌治疗后疾病进展的HR阳性、HER2阴性的局部晚期或晚期转移性乳腺癌的有效性和安全性。研究的主要终点是根据RECISTv1.1标准评估的无进展生存(PFS)。
据介绍,该研究共入组361例受试者,患者按照2:1随机入组,分别接受SHR6390治疗或安慰剂联合氟维司群治疗,每28天为一个治疗周期。其中前3周连续服药SHR6390或安慰剂,后1周休息(不服药),治疗直至疾病进展、毒性不可耐受或其他需要终止治疗的情况。研究结果表明:对于既往接受过内分泌治疗的HR阳性、HER2阴性晚期乳腺癌患者,与安慰剂联合氟维司群相比,接受SHR6390联合氟维司群治疗可显著延长患者的无进展生存期。本次,SHR6390片的上市申请被纳入拟优先审评意味着,这款创新疗法将有望很快惠及到乳腺癌患者。值得一提的是,除二线治疗激素受体阳性乳腺癌外,SHR6390还在进行应用于晚期一线相关治疗的关键研究。其中,一项SHR6390联合芳香化酶抑制剂对比芳香化酶抑制剂治疗HR阳性、HER2阴性晚期乳腺癌的3期研究正在开展中,该研究针对的是在晚期阶段未接受过系统治疗的患者。期待SHR6390的其它临床研究也顺利进行,早日为更多患者带来新的治疗选择。注:本文旨在介绍医药健康研究进展,不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。
参考资料:
[1]中国国家药监局药品审评中心. Retrieved May 10, 2021, from http://www.cde.org.cn/news.do?method=changePage&pageName=service&frameStr=25#[2]恒瑞医药SHR6390片治疗晚期乳腺癌III期临床研究达到主要研究终点. Retrieved Dec 24,2020, from https://mp.weixin.qq.com/s/H9AIFjvY0Nk3y5i1GOsgqQ版权说明:本文来自药明康德内容团队,欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台。转载授权请在「医药观澜」微信公众号留言联系我们。














