

摘
要:
目的
研究紫花地丁
Viola yedoensis
全草的化学成分。
方法
采用硅胶、
ODS
、
Sephadex LH-20
凝胶和半制备型高效液相等柱色谱方法进行分离纯化,通过理化性质结合
NMR
、
MS
等谱学数据分析鉴定化合物结构。
结果
从紫花地丁
95%
乙醇提取物中分离得到
21
个化合物,分别鉴定为秦皮乙素
-6-
O
-β-
D
-
呋喃芹糖基
-(1→2)-β-
D
-
吡喃葡萄糖苷(
1
)、吲哚
-3-
甲酸乙酯(
2
)、脱氢地芰普内酯(
3
)、滨蒿内酯(
4
)、蒲公英苦素(
5
)、水杨苷(
6
)、丁香苷(
7
)、
4-
羟基
-4-[3′-(β-
D
-
葡萄糖基
)
亚丁基
]-3,5,5-
三甲基
-2-
环己烯
-1-
醇(
8
)、柑橘苷
A
(
9
)、
(7
S
,8
R
)-
二氢去氢二松柏醇
-9-
O
-β-
D
-
吡喃葡萄糖苷(
10
)、山柰素
-3-
O
-α-
L
-(4-
O
-
乙酰基
)
鼠李糖基
-7-
O
-α-
L
-
鼠李糖苷(
11
)、山柰酚
-7-
O
-α-
L
-
鼠李糖苷(
12
)、山柰酚
-3-
O
-α-
L
-
鼠李糖苷(
13
)、山柰酚
-3-
O
-α-
L
-
鼠李糖基
-7-
O
-α-
L
-
鼠李糖苷(
14
)、山柰酚
-3-
O
-β-
D
-
葡萄糖苷(
15
)、芹菜素(
16
)、
(
+
)-
异地芰普内酯(
17
)、尿苷(
18
)、腺苷(
19
)、
6-
羟基
-
香豆素
-7-
O
-α-
L
-
鼠李糖基
-(1→6)-
O
-β-
D
-
葡萄糖苷(
20
)、
(7
S
,8
R
)-
二氢去氢二松柏醇
-4-
O
-β-
D
-
吡喃葡萄糖苷(
21
)。
结论
化合物
1
为新化合物,命名为紫丁葡芹苷,
2
为新天然产物,
5
~
11
和
18
为首次从堇菜属中分离得到,
12
和
21
为首次从紫花地丁中分离得到。

紫花地丁
Viola yedoensis
Makino
为堇菜科堇菜属植物,是一种多年生草本植物,具有清热解毒、凉血消肿的功效,主要用于治疗疔疮肿毒、痈疽发背、丹毒、毒蛇咬伤等症状
[1]
。其用药历史悠久,始载于《千金方》。现代药理研究表明,紫花地丁具有抗炎、抗氧化、抗病毒、抗菌、抗肿瘤、抗凝血等作用
[2-4]
。目前,已从该植物中发现香豆素、黄酮、木脂素、萜类、甾体、生物碱等类化学成分
[5-9]
。但关于紫花地丁活性成分的研究报道还较少,为进一步丰富紫花地丁的化学结构类型,完善其物质基础,探寻活性较好的化合物,本实验对紫花地丁全草
95%
乙醇水提取物的化学成分进行系统研究,从中分离得到
21
个化合物,分别鉴定为秦皮乙素
- 6-
O
-β-
D
-
呋喃芹糖基
-(1→2)-β-
D
-
吡喃葡萄糖苷
[aesculetin-6-
O
-β-
D
-apiofuranosyl-(1→2)-β-
D
-gluco-pyranoside
,
1
]
、吲哚
-3-
甲酸乙酯(
ethyl indole-
3- carboxylate
,
2
)、脱氢地芰普内酯(
dehydrololiolide
,
3
)、滨蒿内酯(
scoparone
,
4
)、蒲公英苦素(
taraxacin
,
5
)、水杨苷(
salicin
,
6
)、丁香苷(
syringin
,
7
)、
4-
羟基
-4-[3′-(β-
D
-
葡萄糖基
)
亚丁基
]-3,5,5-
三甲基
-2-
环己烯
-1-
醇(
(
E
)-4-hydroxy-4-[3′-(β-
D
-glucopyra-nosyloxy)butylidene]-3,5,5-trimethyl-2-cyclohexen-l- one
,
8
)、柑橘苷
A
(
citroside A
,
9
)、
(7
S
,8
R
)-
二氢
去氢松柏醇
-9-
O
-β-
D
-
吡喃葡萄糖苷
[(7
S
,8
R
)-dihydro-
de
hydrodiconiferyl alcohol-9-
O
-β-
D
-glucopyranoside
,
10
]
、山柰素
-3-
O
-α-
L
-(4-
O
-
乙酰基
)
鼠李糖基
-7-
O
-α-
L
-
鼠李糖苷
[kaempferol-3-
O
-α-
L
-(4-
O
-acetyl) rhamno-
pyranoside-7-
O
-α-
L
-rhamnopyranoside
,
11
]
、山柰酚
-
7-
O
-α-
L
-
鼠李糖苷(
kaempferol-7-
O
-α-
L
-rhamno- pyranoside
,
12
)、山柰酚
-3-
O
-α-
L
-
鼠李糖苷(
kaempferol-3-
O
-α-
L
-rhamnopyranoside
,
13
)、山柰酚
-3-
O
-α-
L
-
鼠李糖基
-7-
O
-α-
L
-
鼠李糖苷(
kaempferitrin
,
14
)、山柰酚
-3-
O
-β-
D
-
葡萄糖苷(
kaempferol 3-
O
-β-
D
-glucopyranoside
,
15
)、芹菜素
(
apigenin
,
16
)、
(
+
)-
异地芰普内酯
[(
+
)- isololiolide
,
17
]
、尿苷(
uridine
,
18
)、腺苷(
β-adenosine
,
19
)、
6-
羟基
-
香豆素
-7-
O
-α-
L
-
鼠李糖基
-(1→6)-
O
-β-
D
-
葡萄糖苷
[6-hydroxy
coumarin-7-
O
-α-
L
-rhamnosyl- (1→6)-
O
-β-
D
-glucoside
,
20
]
、
(7
S
,8
R
)-
二氢去氢松柏醇
-4-
O
-β-
D
-
吡喃葡萄糖苷
[(7
S
,8
R
)-dihydrodehydro-diconiferyl alcohol 4-
O
-β-
D
-glucopyranoside
,
21
]
。其中,化合物
1
为新化合物,
2
为新天然产物,
5
~
11
和
18
为首次从堇菜属中分离得到,
12
和
20
为首次从该植物中分离得到。
1
仪器与材料
UltiMate 3000
型高效液相色谱仪(美国
Thermo Fisher
公司),
LC-20AR
型制备液相色谱仪(日本
Shimadzu
公司),
Avance 600
型核磁共振仪(瑞士
Bruker
公司,
TMS
内标),
X500 QTOF
型高分辨质谱仪(美国
AB Sciex
公司)。柱色谱硅胶(
60
~
100
、
300
~
400
,目青岛海洋化工厂),柱色谱硅胶(
200
~
300
目,北京伊诺凯有限公司),薄层色谱硅胶预制板(烟台市化学工业研究所),
LH-20
型羟丙基葡聚糖凝胶(
Sephadex LH-20
,
40
~
63 μm
,德国
Merck
公司),
ODS
柱色谱填料(
ODS-A-HG
,
50 μm
,
YMC
公司)。实验所用色谱甲醇为美国
Tedia
公司,其他提取分离试剂均为分析纯(天津市富宇精细化工有限公司)。
紫花地丁全草于
2018
年
3
月采购于湖北聚瑞中药饮片有限公司,原产地为河南省平顶山市,经山东中医药大学王厚伟副教授鉴定为堇菜科植物紫花地丁
V. yedoensis
Makino
的干燥全草。
2
提取与分离
取紫花地丁干燥全草
5 kg
,用
95%
乙醇水回流提取
3
次,每次
2 h
,提取液合并后滤过,将滤液减压浓缩得总浸膏
600 g
。总浸膏经硅胶柱色谱(
60
~
100
目)分离,以石油醚、二氯甲烷、二氯甲烷
-
甲醇(
50
∶
1
)、二氯甲烷
-
甲醇(
10
∶
1
)、二氯甲烷
-
甲醇(
5
∶
1
)、二氯甲烷
-
甲醇(
2
∶
1
)、甲醇作为流动相梯度洗脱,共得到
7
个流分
Fr. A
~
G
。
Fr. B
经硅胶柱色谱(
200
~
300
目)分离,以石油醚
-
二氯甲烷
-
甲醇(
100
∶
0
∶
0
、
20
∶
1
∶
0
、
10
∶
1
∶
0
、
5
∶
1
∶
0
、
2
∶
1
∶
0
、
1
∶
1
∶
0
、
0
∶
100
∶
0
、
0
∶
10
∶
1
、
0
∶
2
∶
1
、
0
∶
0
∶
100
)梯度洗脱,得到
7
个组分
Fr. B-1
~
B-7
。
Fr. B-2
经
Sephadex LH-20
柱色谱分离,得到
4
个组分
Fr. B-2-1
~
B-2-4
。
Fr. B-2-3
经
Sephadex LH-20
和
ODS
柱色谱分离,得到
9
个组分
Fr. B-2-3-1
~
B-2-3-9
。
Fr. B-2-3-1
经半制备型
HPLC
分离,以甲醇
-
水(
30
∶
70
)洗脱,得到化合物
3
(
t
R
=
65 min
,
14.8 mg
)。
Fr. B-2-3-2
经半制备型
HPLC
分离,以甲醇
-
水(
35
∶
75
)洗脱,得到化合物
4
(
t
R
=
75 min
,
1.9 mg
)。
Fr. B-2-3-5
经半制备型
HPLC
分离,以甲醇
-
水(
50
∶
50
)洗脱,得到化合物
5
(
t
R
=
65 min
,
5.6 mg
)。
Fr. B-2-4
经
300
~
400
目硅胶柱色谱分离,再经半制备型
HPLC
分离,以甲醇
-
水(
60
∶
40
)洗脱,得到化合物
2
(
t
R
=
49 min
,
1.7 mg
)。
Fr. B-7
经硅胶柱色谱(
300
~
400
目)分离,以二氯甲烷
-
甲醇(
100
∶
0
、
100
∶
1
、
50
∶
1
、
20
∶
1
、
10
∶
1
、
5
∶
1
、
2
∶
1
、
0
∶
100
)梯度洗脱,经薄层色谱(
TLC
)分析合并洗脱液,得到
15
个组分
Fr. B-7-1
~
B-7-15
。
Fr. B-7-5
经
Sephadex LH-20
和
ODS
柱色谱分离,再经半制备型
HPLC
分离,以甲醇
-
水(
29
∶
71
)洗脱,得到化合物
17
(
t
R
=
37 min
,
22.7 mg
)。
Fr. C
经
200
~
300
目硅胶柱色谱分离,以二氯甲烷
-
甲醇(
100
∶
0
、
500
∶
1
、
50
∶
1
、
20
∶
1
、
10
∶
1
、
5
∶
1
、
2
∶
1
、
0
∶
100
)梯度洗脱,得到
9
个组分
Fr. C-1
~
C-9
。
Fr. C-2
经
Sephadex LH-20
柱色谱以及半制备型
HPLC
分离,以甲醇
-
水(
60
∶
40
)洗脱,得到化合物
16
(
t
R
=
50 min
,
7.8 mg
)。
Fr. D
经硅胶柱色谱(
200
~
300
目)分离,以二氯甲烷
-
甲醇(
50
∶
1
、
20
∶
1
、
10
∶
1
、
7
∶
1
、
5
∶
1
、
1
∶
1
、
0
∶
100
)梯度洗脱,得到
9
个组分
Fr. D-1
~
D-9
。
Fr. D-7
经
Sephadex LH-20
和
ODS
柱色谱分离,得到
15
个组分
Fr. D-7-1
~
D-7-15
。
Fr. D-7-2
经半制备型
HPLC
分离,以甲醇
-
水(
10
∶
90
)洗脱,得到化合物
19
(
t
R
=
70 min
,
34.4 mg
)和
6
(
t
R
=
90 min
,
15.8 mg
)。
Fr. D-7-3
经半制备型
HPLC
分
离,以甲醇
-
水(
20
∶
80
)洗脱,得到化合物
7
(
t
R
=
60 min
,
6.8 mg
)。
Fr. D-7-5
经半制备型
HPLC
分离,以甲醇
-
水(
30
∶
70
)洗脱,得到化合物
8
(
t
R
=
47 min
,
6.0 mg
)和
9
(
t
R
=
50 min
,
15.2 mg
)。
Fr. D-7-7
经半制备型
HPLC
分离,以甲醇
-
水(
37
∶
63
)洗脱,得到化合物
10
(
t
R
=
71 min
,
2.9 mg
)。
Fr. D-7-9
经半制备型
HPLC
分离,以甲醇
-
水(
40
∶
60
)洗脱,得到化合物
15
(
t
R
=
100 min
,
2.8 mg
)。
Fr. D-7-10
经半制备型
HPLC
分离,以甲醇
-
水(
48
∶
52
)洗脱,
得到化合物
13
(
t
R
=
56 min
,
5.0 mg
)。
Fr. D-7-13
经半制备型
HPLC
分离,以甲醇
-
水(
50
∶
50
)洗脱,得到化合物
11
(
t
R
=
60 min
,
11.2 mg
)。
Fr. D-7
经
Sephadex LH-20
柱色谱和反复
ODS
柱色谱分离,最后经
Sephadex LH-20
柱色谱纯化,得到化合物
14
(
18.5 mg
)。
Fr. E
经
200
~
300
目硅胶柱色谱分离,以二氯甲烷
-
甲醇(
100
∶
0
、
100
∶
1
、
50
∶
1
、
20
∶
1
、
10
∶
1
、
5
∶
1
、
2
∶
1
、
1
∶
1
、
0
∶
100
)梯度洗脱,得到
8
个组分
Fr. E-1
~
E-8
。
Fr. E-3
经
Sephadex LH-20
柱色谱分离,重结晶纯化得到化合物
12
(
22.9 mg
)。
Fr. E-5
经
Sephadex LH-20
和
ODS
柱色谱分离,得到
12
个组分
Fr. E-5-1
~
E-5-12
。
Fr. E-5-2
经半制备型
HPLC
分离,以甲醇
-
水(
9
∶
91
)洗脱,得到化合物
18
(
t
R
=
23 min
,
13.4 mg
)。
Fr. E-5-4
经半制备型
HPLC
分离,以甲醇
-
水(
20
∶
80
)洗脱,得到化合物
20
(
t
R
=
59 min
,
7.7 mg
)。
Fr. E-5-5
经半制备型
HPLC
分离,以甲醇
-
水(
20
∶
80
)洗脱,得到化合物
1
(
t
R
=
77 min
,
8.9 mg
)。
Fr. E-5-8
经半制备型
HPLC
分离,以甲醇
-
水(
35
∶
65
)洗脱,得到化合物
21
(
t
R
=
46 min
,
6.5 mg
)。
3
结构鉴定
化合物
1
:白色粉末;
[α]
20D
−76.5
(
c
0.1
,
MeOH
);
(cm
−
1
)
: 3405, 2537, 2400, 1667, 1560,1503, 1263
;
HR-ESI-MS
的准分子离子峰为
m
/
z
495.111 2 [M
+
Na]
+
(计算值为
495.111 5
),确定分子式为
C
20
H
24
O
13
,不饱和度为
9
。
IR
提示该化合物含有羰基(
1667 cm
−
1
)和羟基(
3405 cm
−
1
)基团。
13
C-NMR
谱(表
1
)中共显示
20
个碳信号,其中
9
个归属为香豆素骨架,其余
11
个碳信号分别归属为
1
个五碳糖和
1
个六碳糖片段。
1
H-NMR
谱中显示了
1
个
β
构型的葡萄糖基质子信号
δ
H
4.86
,但因与水峰重合,无法获得偶合信息;通过
HSQC
和
DEPT
谱图发现
H-1′ (
δ
H
4.86)
与
C-1′ (
δ
C
103.4)
相关,确定为葡萄糖基端基质子信号。
1
H-NMR
谱中还给出了
1
个芹糖基端基质子信号
δ
H
5.35 (1H, d,
J
= 3.8 Hz, H-1′′)
。在
NMR
谱中,
δ
H
7.82 (1H, d,
J
= 9.3 Hz,H-4), 6.21 (1H, d,
J
= 9.3 Hz, H-3)
与
δ
C
163.8, 146.2,113.2
,提示有
α-
吡喃酮片段;
NMR
谱还显示
2
个单峰芳香质子信号
δ
H
7.51 (1H, s, H-5), 6.79 (1H, s, H-8)
,结合
δ
C
153.6, 152.9,144.5, 117.4, 112.9
和
104.4
提示苯环上含
2
个对位氢,综合以上信息,推测存在
6,7-
二氧取代香豆素结构片断。
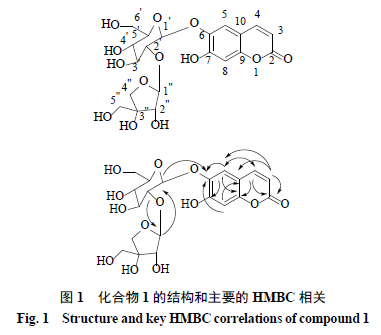
HMBC
谱(图
1
)中,
H-3 (
δ
H
6.21)
与
C-2 (
δ
C
163.8), C-5 (
δ
C
117.4), C-10 (
δ
C
112.9)
相关,
H-4 (
δ
H
7.82)
与
C-2 (
δ
C
163.8), C-5 (
δ
C
117.4),C-9 (
δ
C
152.9)
相关,
H-5 (
δ
H
7.51)
与
C-4 (
δ
C
146.2), C-6 (
δ
C
144.5),C-7 (
δ
C
153.7), C-9 (
δ
C
152.9)
相关,
H-8 (
δ
H
6.79)
与
C-6 (
δ
C
144.5), C-10 (
δ
C
112.9)
相关,进一步证明了
6,7-
二取代香豆素片段的存在。与已知化合物秦皮乙素
-
6-
O
-β-
D
-
呋喃芹糖基
-(1→6)-β-
D
-
吡喃葡萄糖苷相比
[10]
,结构相似,都含有葡萄糖和芹糖,不同之处在于糖的连接位置,化合物
1
中的芹糖基连接于葡萄糖基的
2
位碳上。在
HMBC
谱上,葡萄糖基
H-1′
与
C-6 (
δ
C
144.5)
相关,进一步证明葡萄糖基
C-1′
与香豆素
C-6
位相连;芹糖基
H-1′′
与
C-2′ (
δ
C
83.7)
相关,葡萄糖基
H-2′
与
C-1′′ (
δ
C
112.8)
相关,可以确认芹糖基
C-1′′
与葡萄糖基的
C-2′
位相连。综上所述,鉴定化合物
1
的结构为秦皮乙素
-6-
O
-β-
D
-
呋喃芹糖基
-(1→2)-β-
D
-
吡喃葡萄糖苷,为
1
个新化合物,命名为紫丁葡芹苷。核磁数据见表
1
。

化合物
2
:白色固体。
ESI-MS
m
/
z
: 190.08 [M
+
H]
+
,212.06 [M
+
Na]
+
。
1
H-NMR (600 MHz, CDCl
3
)
δ
: 8.58 (1H, s, NH), 8.19
~
8.15 (1H, m, H-2), 7.91 (1H, d,
J
= 3.0 Hz, H-4), 7.41
~
7.39 (1H, m, H-7), 7.26
~
7.25 (2H, m, H-5, 6), 4.38 (2H, q,
J
= 7.1 Hz, H-9), 1.41 (3H, t,
J
= 7.1 Hz, H-10)
;
13
C-NMR (150 MHz, CDCl
3
)
δ
: 165.5 (C-8), 136.3 (C-7a), 131.1(C-2), 126.0 (C-3a), 123.4 (C-6), 122.2 (C-4), 121.8 (C-5), 111.7 (C-7), 109.4(C-3), 60.0 (C-9), 14.8 (C-10)
。经
SciFinder
检索,化合物
2
在文献中通过合成得到
[11]
,因此其作为
1
个天然产物首次从植物中分离得到,是新的天然产物,结构鉴定为吲哚
-3-
甲酸乙酯。
化合物
3
:黄色油状物。
ESI-MS
m
/
z
: 195.10 [M
+
H]
+
,217.08 [M
+
Na]
+
。
1
H-NMR (600 MHz, CDCl
3
)
δ
: 5.89 (1H, s, H-7), 2.92 (1H, dd,
J
= 13.6, 1.8 Hz, H-4a), 2.64 (1H, d,
J
= 13.6 Hz, H-2a), 2.44 (1H, dd,
J
=14.3, 1.9 Hz, H-4b), 2.39 (1H, d,
J
=14.3 Hz, H-2b), 1.55 (3H, s, H-11), 1.39 (3H, s, H-9), 1.26 (3H, s, H-10)
;
13
C-NMR (150 MHz, CDCl
3
)
δ
: 204.7 (C-3), 178.5 (C-8), 170.9(C-6), 114.7 (C-7), 86.3 (C-5), 54.2 (C-4), 53.8 (C-2), 36.0 (C-1), 29.9(C-11), 26.9 (C-9), 26.2 (C-10)
。以上数据与文献报道一致
[12]
,故鉴定化合物
3
为脱氢地芰普内酯。
化合物
4
:无色针状结晶(甲醇)。
ESI-MS
m
/
z
: 207.06 [M
+
H]
+
,229.04 [M
+
Na]
+
。
1
H-NMR (600 MHz, CDCl
3
)
δ
: 7.60 (1H, d,
J
= 9.4 Hz, H-4), 6.83 (1H, s, H-5), 6.82 (1H, s, H-8), 6.26 (1H,d,
J
= 9.4 Hz, H-3), 3.93 (3H, s, 6-OCH
3
), 3.90 (3H, s, 7-OCH
3
)
;
13
C-NMR (150 MHz, CDCl
3
)
δ
: 161.6 (C-2), 153.1 (C-7), 150.2(C-9), 146.6 (C-6), 143.5 (C-4), 113.8 (C-3), 111.6 (C-10), 108.2 (C-5), 100.2(C-8), 56.6 (6-OCH
3
), 56.6 (7-OCH
3
)
。以上数据与文献报道一致
[13]
,故鉴定化合物
4
为滨蒿内酯。
化合物
5
:黄色粉末。
ESI-MS
m
/
z
: 243.09 [M
+
H]
+
,265.08 [M
+
Na]
+
。
1
H-NMR (600 MHz, CDCl
3
)
δ
: 6.50 (1H, s, H-6), 6.25 (1H, s,H-3), 5.06 (1H, dd,
J
= 12.7, 3.3 Hz, H-8), 2.96 (1H, dd,
J
= 16.8, 3.3 Hz, H-9a), 2.77 (1H, dd,
J
= 16.8, 12.7 Hz, H-9b), 2.50 (3H, s,H-14), 2.24 (3H, s, H-15), 1.99 (3H, s, H-13)
;
13
C-NMR (150 MHz, CDCl
3
)
δ
: 194.4 (C-2), 173.7 (C-12), 161.7(C-5), 154.9 (C-7), 147.6 (C-10), 144.0 (C-4), 134.5 (C-3), 128.6 (C-1), 124.5(C-11), 111.3 (C-6), 77.2 (C-8), 41.5 (C-9), 22.3 (C-14), 14.4 (C-15), 9.1(C-13)
。以上数据与文献报道一致
[14]
,故鉴定化合物
5
为蒲公英苦素。
化合物
6
:黄色结晶(甲醇)。
ESI-MS
m
/
z
: 309.09 [M
+
Na]
+
。
1
H-NMR (600 MHz, CD
3
OD)
δ
: 7.35 (1H, dd,
J
= 7.5, 1.5 Hz, H-6), 7.29 (1H, dt,
J
= 7.5, 1.5 Hz, H-4), 7.20 (1H, d,
J
= 7.5 Hz, H-3), 7.06 (1H, dt,
J
= 7.5, 0.9 Hz, H-5), 4.93 (1H, d,
J
= 7.4 Hz , H-1′), 4.76 (1H, d,
J
=12.9 Hz, H-7b), 4.60 (1H, d,
J
= 12.9Hz, H-7a), 3.90 (1H, dd,
J
= 12.2,2.1 Hz, H-6′b), 3.72 (1H, dd,
J
=12.2, 5.4 Hz, H-6′a), 3.56
~
3.42 (4H, m, H-2′
~
5′)
;
13
C-NMR (150 MHz, CD
3
OD)
δ
: 156.9 (C-2), 131.9 (C-1), 130.3(C-6), 130.2 (C-4), 124.0 (C-5), 117.0 (C-3), 103.0 (C-1′), 78.1 (C-3′), 77.7(C-5′), 74.9 (C-2′), 71.3 (C-4′), 62.4 (C-6′), 60.9 (C-7)
。以上数据与文献报道一致
[15]
,故鉴定化合物
6
为水杨苷。
化合物
7
:白色结晶(甲醇)。
ESI-MS
m
/
z
: 395.13 [M
+
Na]
+
。
1
H-NMR (600 MHz, CD
3
OD)
δ
: 6.77 (2H, s, H-3, 5), 6.56 (1H, d,
J
= 15.8 Hz, H-7), 6.35 (1H, dt,
J
=15.8, 5.6 Hz, H-8), 4.89 (1H, d,
J
=7.7 Hz, H-1), 4.24 (2H, dd,
J
= 5.6,1.4 Hz, H-9), 3.87 (6H, s, 2
×
OCH
3
), 3.80 (1H, dd,
J
= 12.0, 2.4 Hz, H-6′b), 3.68 (1H, dd,
J
= 12.0, 5.2 Hz, H-6′a), 3.21
~
3.50 (4H, m, H-2′
~
5′)
;
13
C-NMR (150 MHz, CD
3
OD)
δ
: 154.5 (C-2, 6), 136.0 (C-1), 135.4(C-4), 131.4 (C-7), 130.2 (C-8), 105.6 (C-1′), 105.5 (C-3, 5), 78.5 (C-3′),78.0 (C-5′), 75.9 (C-2′), 71.5 (C-4′), 63.7 (C-9), 62.7 (C-6′), 57.2 (2
×
OCH
3
)
。以上数据与文献报道一致
[16]
,故鉴定化合物
7
为丁香苷。
化合物
8
:黄色油状物。
ESI-MS
m
/
z
: 387.18 [M
+
H]
+
,409.16 [M
+
Na]
+
。
1
H-NMR (600 MHz, CD
3
OD)
δ
: 5.86 (3H, m, H-2, 7, 8), 4.42 (1H,m, H-9), 4.34 (1H, d,
J
= 7.8 Hz, H-1′),3.85 (1H, dd,
J
= 11.7, 1.9 Hz, H-6′a),3.62 (1H, dd,
J
= 11.7, 5.5 Hz, H-6′b),3.23
~
3.35 (3H, m, H-3′
~
5′), 3.17 (1H, m, H-2′), 2.52 (1H,d,
J
= 17.0 Hz, H-6b), 2.15 (1H, d,
J
= 16.9 Hz, H-6a), 1.92 (3H, s, H-13),1.29 (3H, d,
J
= 6.4 Hz, H-10), 1.04(6H, d,
J
= 3.7 Hz, H-11, 12)
;
13
C-NMR (150 MHz, CD
3
OD)
δ
: 201.3 (C-1), 167.4 (C-3), 135.4(C-8), 131.7 (C-7), 127.3 (C-2), 102.9 (C-1′), 80.2 (C-4), 78.3 (C-5′), 78.2(C-3′), 77.4 (C-9), 75.4 (C-4′), 71.8 (C-2′), 63.0 (C-6′), 50.8 (C-6), 42.6(C-5), 24.8 (C-12), 23.6 (C-11), 21.3 (C-10), 19.7 (C-13)
。以上数据与文献报道一致
[17]
,故鉴定化合物
8
为
4-
羟基
- 4-[3′-(
β-
D
-
葡萄糖基
)
亚丁基
]-3,5,5-
三甲基
-2-
环己烯
-1-
醇。
化合物
9
:黄色油状物。
ESI-MS
m
/
z
: 409.16 [M
+
Na]
+
。
1
H-NMR (600 MHz, CD
3
OD)
δ
: 5.89 (1H, s, H-8), 4.52 (1H, d,
J
= 7.8 Hz, H-1′), 4.32 (1H, m, H-3),2.20 (3H, s, H-10), 1.47 (3H, s, H-12), 1.38 (3H, s, H-13), 1.16 (3H, s, H-11)
;
13
C-NMR (150 MHz, CD
3
OD)
δ
: 213.1 (C-7), 200.9 (C-9), 119.2(C-6), 101.5 (C-8), 98.8 (C-1′), 78.9 (C-5), 78.7 (C-3′), 77.9 (C-5′), 75.4(C-2′), 71.8 (C-4′), 63.9 (C-3), 63.0 (C-6′), 50.0 (C-2), 48.2 (C-4), 37.2(C-1), 32.7 (C-11), 30.2 (C-13), 26.8 (C-10), 26.8 (C-12)
。以上数据与文献报道一致
[18]
,故鉴定化合物
9
为柑橘苷
A
。
化合物
10
:黄色油状物;
[α]
20D
−34.2°
(
c
0.1
,
MeOH
)。
ESI-MS
m
/
z
: 545.14 [M
+
Na]
+
。
1
H-NMR (600 MHz, CD
3
OD)
δ
: 6.99 (1H, d,
J
= 1.7 Hz, H-2), 6.87 (1H, dd,
J
= 8.1, 1.7 Hz , H-6), 6.78 (1H, s, H-2′), 6.76 (1H, d,
J
= 8.1 Hz, H-5), 6.73 (1H, s, H-6′),5.60 (1H, d,
J
= 6.2 Hz, H-7), 4.35(1H, d,
J
= 7.8 Hz, H-1′′), 4.21 (1H,dd,
J
= 9.7, 5.5 Hz, H-9a), 3.87 (1H,m, H-9b), 3.86 (3H, s, 3′-OMe), 3.82 (3H, s, 3-OMe), 3.75 (1H, t,
J
= 8.8 Hz, H-6′′a), 3.65 (2H, m, H-8,6′′b), 3.57 (2H, t,
J
= 6.5 Hz, H-9′),3.35 (1H, m, H-5′′), 3.28 (2H, m, H-3′′, 4′′), 3.23 (1H, m, H-2′′), 2.62 (2H,t,
J
= 7.6 Hz, H-7′), 1.81 (2H, m,H-8′)
;
13
C-NMR (150 MHz, CD
3
OD)
δ
: 149.2 (C-3), 147.6 (C-4), 147.5(C-4′), 145.4 (C-3′), 137.1 (C-1′), 134.9 (C-1), 129.8 (C-5′), 119.9 (C-6),118.4 (C-2′), 116.2 (C-5), 114.3 (C-6′), 110.8 (C-2), 104.7 (C-1′′), 89.1(C-7), 78.4 (C-3′′), 78.2 (C-5′′), 75.3 (C-2′′), 72.6 (C-9), 71.8 (C-4′′), 63.0(C-6′′), 62.4 (C-9′), 56.9 (3′-OMe), 56.6 (3-OMe), 53.4 (C-8), 36.0 (C-8′),33.0 (C-7′)
。以上数据与文献报道一致
[19]
,故鉴定化合物
10
为
(7
S
,8
R
)-
二氢去氢二松柏醇
-9-
O
-β-
D
-
吡喃葡萄糖苷。
化合物

















