|
l
重磅产品落地开花,国产研发回报兑现。
2
月
22
日,药监局批准复宏汉霖的利妥昔单抗注射剂(商品名:汉利德)和乐普的“生物可吸收冠状动脉雷帕霉素洗脱支架系统”(
NeoVas
)上市。复宏汉霖的利妥昔单抗是国内首款
biosimilar
药物,标志国产药物在较难研发的
biosimilar
领域拔下一城,主要获批适应症为非霍奇金淋巴瘤。乐普
NeoVas
达到国际领先水平,我们估计第一代可吸收支架将会替代
15%-20%
左右的现有支架,在此基础上,可降解支架
2021
年左右为乐普贡献近
6
亿元净利润。
l
收益基本面未变,看好创新药及
CRO
行业长期发展。
在后“
4+7
”时代,针对市场对于创新药资金来源及
CRO
行业的疑虑,我们认为:
1
)创新药行业是否受到影响与创新药收益率有关,与仿制药企利润不直接相关;
2
)从药品价格、生命周期看,国产创新药收益率仍可观;
3
)药品创新方向是未满足的临床需求,不是追求全球新;
4
)纵观美国、日本、印度、欧洲等制药业发展史,创新药产业的兴起与历史环境、科技发展及政策鼓励密切相关。特殊的市场环境及特定的历史政策帮助了美国、日本创新药产业崛起,中国无法复制日本、美国模式,但也迎来了自身的历史机遇。
l
政策渐稳,推荐政策相对免疫及业绩增长强的标的。
政策明确试点先行,关注联动情况,正值年报季,我们建议短期内关注政策相对免疫及强业绩确定性公司:
1
)非药类龙头公司,包括连锁医疗服务、药店(爱尔眼科、通策医疗、益丰药房、老百姓),消费类属性较强标的(鱼跃医疗);
2
)短期降价压力较小、具备品种持续兑现能力的创新药企和
CRO/CMO
板块(恒瑞医药、泰格医药、药明康德);
3
)趋势向好的细分行业公司(我武生物)、业绩增长强劲标的(恩华药业)等。
l
行情趋好,海通医药
2
月组合平均上涨
18.4%
。
2019
年
2
月月度组合:泰格医药、益丰药房、恒瑞医药、迈瑞医疗、药明康德、爱尔眼科、美年健康、鱼跃医疗、我武生物(排名不分先后)。医药板块上涨强劲,海通医药
2
月组合平均上涨
18.4%
,同期全指医药上涨
20.9%
,跑输医药指数
2.5
个百分点。其中收益靠前的有泰格医药(
+29.3%
)、益丰药房(
+26.9%
)、恒瑞医药(
+21.8%
)等。
l
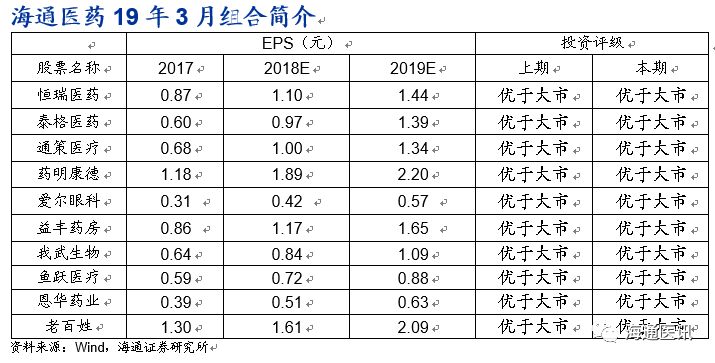
海通医药
19
年
3
月组合:
恒瑞医药、泰格医药、通策医疗、药明康德、爱尔眼科、益丰药房、我武生物、鱼跃医疗、恩华药业、老百姓
(排名不分先后)。
风险提示:政策推进不达预期,医保控费加剧风险,估值波动的风险。
|



1.
医药行业
观点
1.1
行业看
法
:
1.1.1
重磅产品落地开花,国产研发回报兑现
2
月
22
日,药监局批准复宏汉霖的利妥昔单抗注射剂(商品名:汉利德)和乐普的“生物可吸收冠状动脉雷帕霉素洗脱支架系统”上市。
首款国产
biosimilar
上市,验证国产研发实力。
复宏汉霖的利妥昔单抗是国内首款
biosimilar
药物,标志国产药物在较难研发的
biosimilar
领域拔下一城,主要获批适应症为非霍奇金淋巴瘤。复宏汉霖的利妥昔单抗对标
Genentech
(罗氏子公司)明星药品“美罗华”,是
FDA
批准的第一个肿瘤单抗药物,
2018
年全球销售额因欧洲市场生物类似药竞争下降至
68
亿瑞士法郎,海外市场(包括中国)销售
13.6
亿瑞士法郎,其中中国地区同比增长
40%
。美罗华
2000
年进入中国,
2017
年医保谈判进入国家医保乙类目录,医保支付标准为
2418
元(
100mg/10ml/
瓶)或
8289.87
元(
500mg/50ml/
瓶)。
国产支架研发进入可降解时代。
乐普的“生物可吸收冠状动脉雷帕霉素洗脱支架系统”(
NeoVas
)的试验数据表明该产品性能达到国际领先水平,与美国雅培公司生产的
XIENCE
金属药物支架临床效果相当。完全可吸收支架可解决支架术后再狭窄的问题,目前主流可吸收支架为聚乳酸或聚乙酸材料,植入
2-3
年后完全降解为二氧化碳和水,如果出现术后再狭窄,由于血管里边没有残留的金属物,干预起来相对容易得多,受到医生的欢迎,是支架未来的发展趋势。我们估计,第一代可吸收支架将会替代
15%-20%
左右的现有支架,主要受限于材料,存在径向支撑力较差、支架厚度较厚、易断裂、血栓率较高的问题。在此基础上,我们估计可降解支架
2021
年左右为乐普贡献近
6
亿元净利润。

1.1.2
收益基本面未变,看好
创新药及
CRO
行业长期发展
“
4+7
”集采对医药行业产生巨大影响,近期我们连续发布三篇深度《囚徒困境的症结》、《一张典型的药企收入利润表剖析》、《“
4+7
”后国产创新药会受到影响吗?》,期望以
3-5
年甚至更长的维度去判断行业未来。
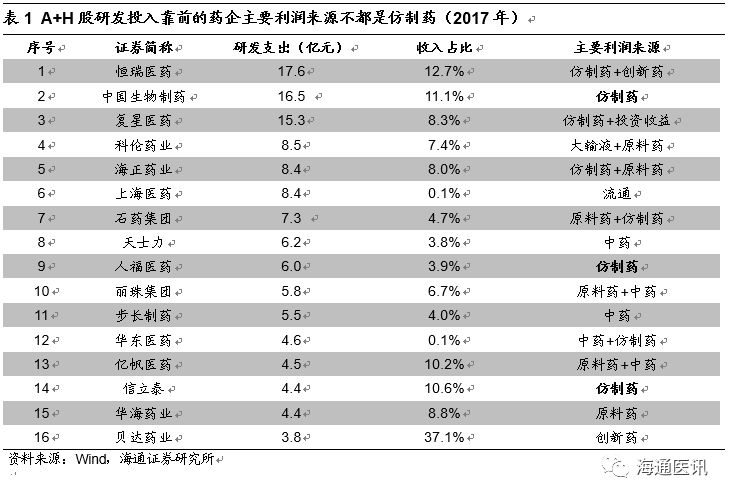
创新药行业是否受到影响与创新药收益率有关,与仿制药企利润不直接相关。
我们认为仿制药盈利能力下降将驱动价值回归,创新药盈利能力将显现。创新药的研发费用只有部分来自于仿制药利润,上市仿制药企研发投入占医药研发投入不超过
40%
。通过梳理
2017-18
年
CDE
登记的临床试验数量以及阶段,测算临床试验所需花费的研发费用,我们预计
2018
年仿制药研发投入
127.1
亿元,创新药研发投入约
200
亿元。从行业角度看,资金来源无论是
PE/VC
投资或是企业本身的利润不是最重要的,重要的是有了资金投入,国产创新药能够获批上市并且获得较为客观的受益,对于整个行业来说是正反馈的。比如君实和信达的
PD-1
单抗已上市,我们预计恒瑞的卡瑞利珠单抗能在
2019Q1
获批上市,无论是
biotech
公司还是大药企的
PD-1
单抗,都能够满足国内患者的临床需求,也都能够同进口品种竞争当。

从药品价格、生命周期看,国产创新药收益率仍可观。
对于国产新药的收益率,我们的观点是:
1
)国产创新药时间窗口前移,外资新药上市之后
2-3
年内就能上市,那么窗口期还会有很长时间;
2
)“专利悬崖”的问题虽然导致品种永续价值下降,但由于进医保更快,达峰时间会更短,产生的收益不一定会明显下降。况且我们认为新药市场的专利悬崖不会像欧美那么猛烈,主要原因是支付能力弱导致专利到期前渗透率不高。
3
)另外,价格是国产新药的优势,但并不意味着绝对价格低,也不意味着按成本加成定价。
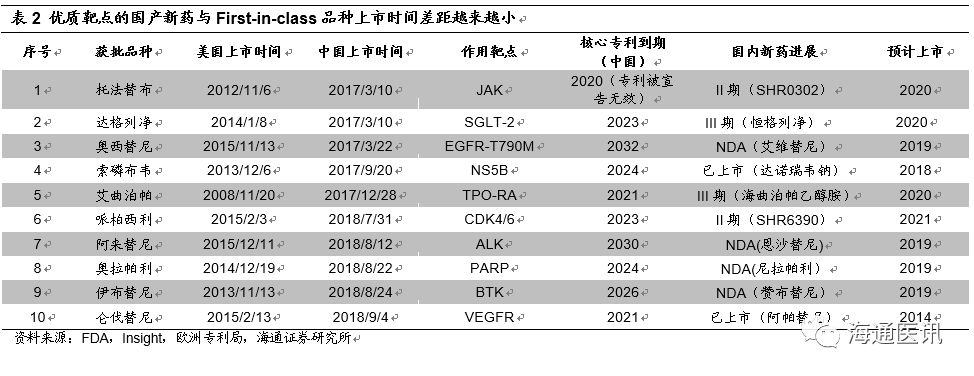
药品创新方向是未满足的临床需求,不是追求全球新。
我们认为,当前阶段
Fast-Follow
是性价比最高的战略选择。
First-in-Class
药物对国内药企来说风险较大,收益不一定高,解决未满足的临床需求才是药物研发的基本目的。由于欧美国家与我国的疾病谱相差较大,我们在部分疾病领域的临床需求需要国内新药来满足。另外,由于支付能力有限以及药品价格不会像美国那么高,因此国产创新药集中在大领域,大病种才能有市场空间。
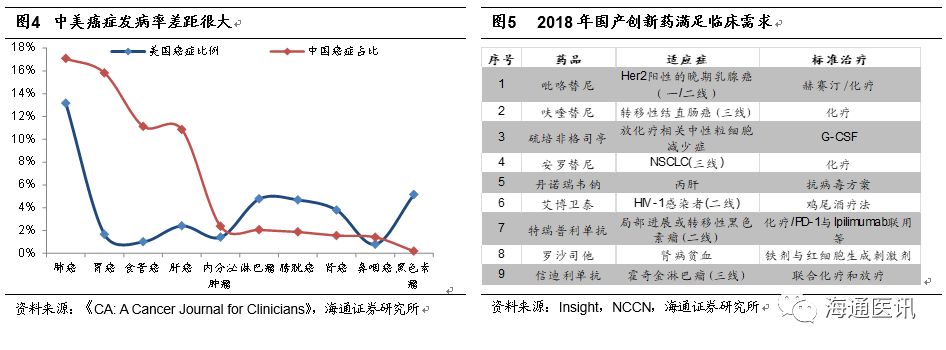
纵观美国、日本、印度、欧洲等制药业发展史,创新药产业的兴起与历史环境、科技发展及政策鼓励密切相关。特殊的市场环境及特定的历史政策帮助了美国、日本创新药产业崛起,中国无法复制日本、美国模式,但也迎来了自身的历史机遇。
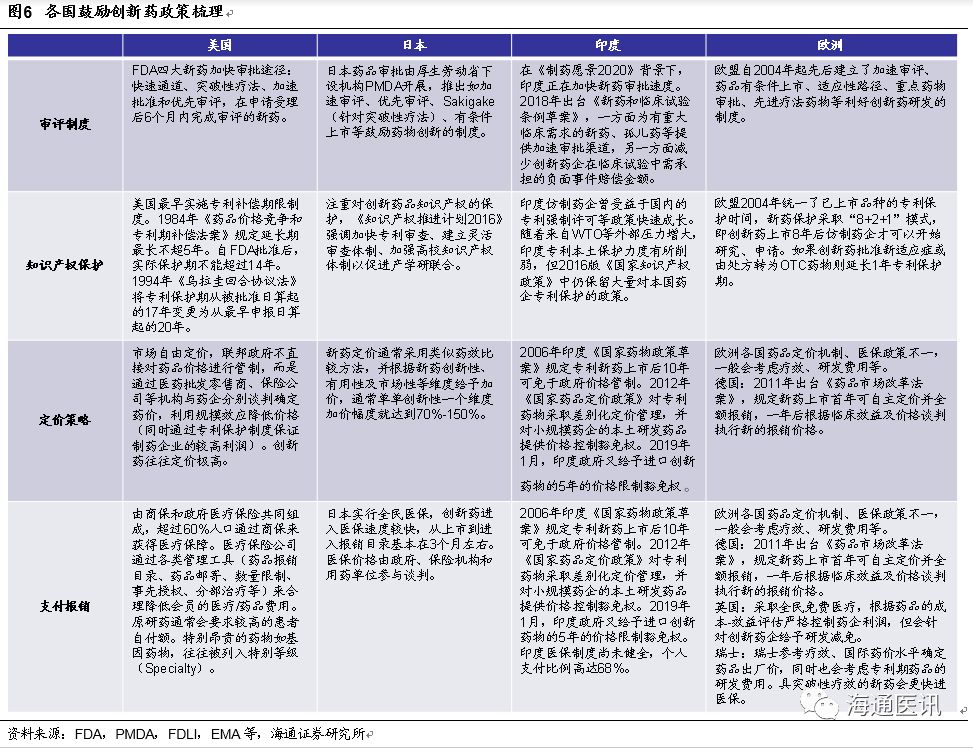
1.1.3
政策渐稳,推荐政策相对免疫及业绩增长强的标的
政策渐稳,推荐政策相对免疫及业绩增长强的标的。政策试点明确,关注联动情况,正值年报季,我们建议短期内关注政策相对免疫及强业绩确定性公司:
1
)非药类龙头公司,包括连锁医疗服务、药店(爱尔眼科、通策医疗、益丰药房、老百姓),消费类属性较强标的(鱼跃医疗);
2
)短期降价压力较小、具备品种持续兑现能力的创新药企和
CRO/CMO
板块(恒瑞医药、泰格医药、药明康德);
3
)趋势向好的细分行业公司(我武生物)、业绩增长强劲标的(恩华药业)等。
1.2
2019
年
3
月组合
结合个股基本面情况,我们给出的
2019
年
3
月组合为:
恒瑞医药、泰格医药、通策医疗、药明康德、爱尔眼科、益丰药房、我武生物、鱼跃医疗、恩华药业、老百姓
(排名不分先后)。

2
.
201
9
年
2
月组合回顾
2.1
海通医药
2019
年
2
月月度组合表现
2019
年
2
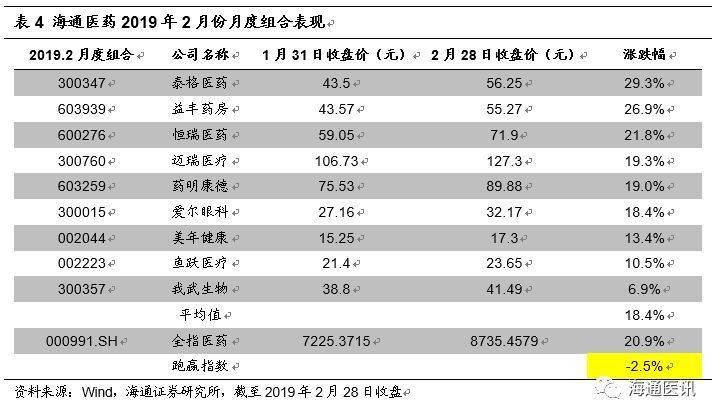
月月度组合:恒瑞医药、泰格医药、药明康德、鱼跃医疗、迈瑞医疗、我武生物、爱尔眼科、美年健康、益丰药房(排名不分先后)。医药板块上涨强劲,海通医药
2
月组合平均上涨
18.4%
,同期全指医药上涨
20.9%
,跑输医药指数
2.5
个百分点。其中收益靠前的有泰格医药(
+29.3%
)、益丰药房(
+26.9%
)和恒瑞医药(
+21.8%
)等。
2.2
近期市场表
现
:医药板块跑输上证综指
2
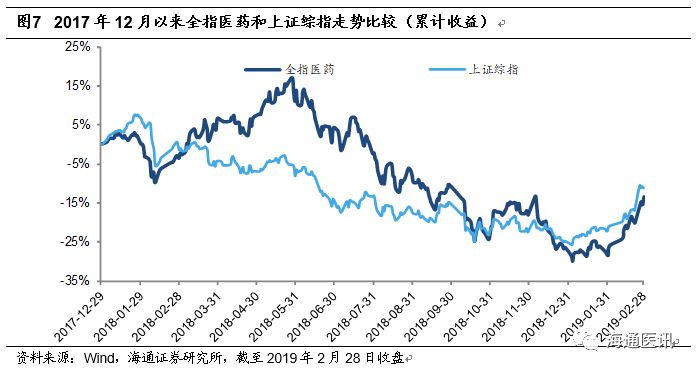
月份医药板块指数大幅上涨。
2
月全指医药指数上涨
20.90%
,同期上证综指上涨
13.79%
,医药指数大幅跑赢上证综指
7.11
个百分点。年初至今,全指医药指数上涨
17.54%
,
2
月医药指数涨幅已覆盖上月跌幅。
2.3
个股市场表现
2
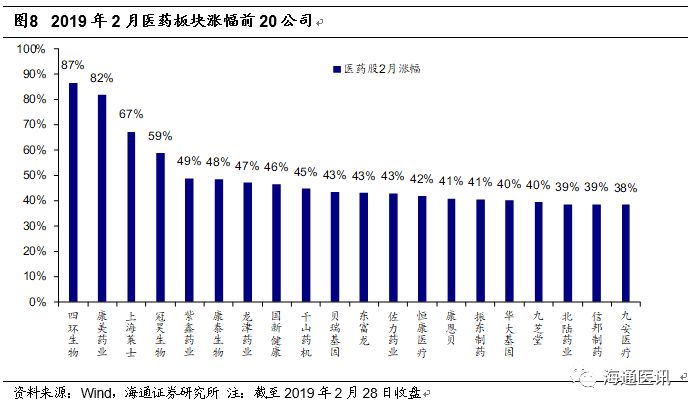
月份医药板块涨幅排名前
20
的公司为:四环生物、康美药业、上海莱士、冠昊生物、紫鑫药业、康泰生物、龙津药业、国新健康、千山药业、贝瑞基因、东富龙、佐力药业、恒康医疗、康恩贝、振东制药、华大基因、九芝堂、北陆药业、信邦制药、九安医疗等。涨幅前
20
标的大部分上涨
40%
以上,主要是生物制品、中药、医疗器械等细分领域等标的。
2.4
估值水平
目前医药板块按2月28日收盘价计算的动态PE(TTM)为28.9倍(剔除负值),不含原料药为29.1倍。我们认为目前医药板块估值回升,仍处于历史低位水平。
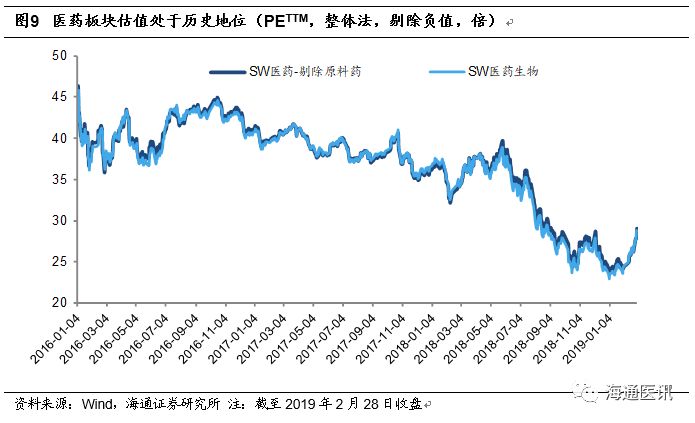
医药板块相对于全部A股的溢价水平自2010年以来一直呈现高位水平,2014年以来,溢价率持续下降,当前相对溢价率97.59%。

3.
医药行业及个股动向
3.1
国内罕见病诊疗指南首次发布,两款孤儿药确定医保支付标准
事件:
2
月
27
日,《罕见病诊疗指南(
2019
年版)》正式发布。该指南涵盖
121
种罕见病,对
121
种罕见病详细阐述了定义、病因和流行病学、临床表现、辅助检查、诊断、鉴别诊断和治疗,并在每一种罕见病的最后提出了诊疗流程,以清晰的流程图形式向读者展现诊断流程和治疗原则,对提高我国罕见病规范化的诊疗水平具有重要意义。
2019
年
2
月
21
日,经戈谢病、庞贝氏病特效药医保准入谈判小组与相关药品生产企业谈判,确定了戈谢病特效治疗药注射用伊米苷酶(商品名:思而赞)和庞贝氏病特效治疗药注射用阿糖苷酶α(商品名:美尔赞)的医保支付标准。注射液
400
单位
/
瓶的思儿赞医保支付
20700
元
/
瓶,注射液
50mg/
支的美儿赞医保支付
5306.3
元
/
支。
点评:
罕见病诊疗逐渐规范,孤儿药研发加速。
自
2015
年以来,管理部门先后推出了孤儿药临床试验、注册的优先审评审批制度,以及针对国外已批准上市的罕见病用药有条件批准上市制度,利好孤儿药研发、引进工作。我们认为本次首款《罕见病诊疗指南》面世,进一步明确了罕见病诊疗的临床规范,为孤儿药的临床使用提供指导,利好孤儿药进一步有效使用。
减关税
+
医保提升支付能力。
孤儿药减关税、进医保利好罕见病患者支付能力。我们认为近期罕见病药品减关税有望进一步促进孤儿药降价。国务院从
3
月
1
日起,对首批
21
个罕见病药品和
4















