撰文:
L
编辑:
CCL
所属部门:
研之成理理论化学研习社
(2)ETS-NOCV是一种结合ETS(extended transition state)和NOCV(natural orbitals for chemical valence)的一种新方法。它适合用来定性,并且定量地描述构成各种化学键:donor–acceptor、共价键、分子内弱键、分子间弱相互作用,ETS-NOCV能够对这些化学键的进行简洁的表征。不过现在一般用来研究势能面上的一些能量极小值点,比如反应物、过渡态、中间产物、最终产物等等,“化学键”两端的分子或分子片段之间的相互作用。不过这并不是说ETS-NOCV不能用于其它结构状态下。
NOCV能够将分子片段之间的相互作用,分拆为具有化学直观意义的π键、σ键、δ键,定量地得到它们对Total Orbital Interaction的贡献,并得到形成此键的电子转移情况。从而对化学反应的理解更加深刻而直观!
在原始的ETS方法中,互相作用的片段,其结合能(TotalBonding Energy)ΔEtotal分为如下几个部分:
ΔE
total
=ΔE
dist
+ ΔE
elstat
+ ΔE
Pauli
+ ΔE
orb
其中,
§ ΔE
dist
:实际上也叫做“准备能”,也就是“片段”从它的自由状态(孤立存在的时候,能量最低点),能量升高,变形为在分子中的形状,这个过程中,所增加的能量,该项非负。
§ ΔE
elstat
:在分子中,片段之间的经典的静电相互作用能
§ ΔE
Pauli
:两个片段的占据轨道之间的排斥作用,该项非负
§ ΔE
orb
:包括两个部分:一个片段占据轨道与另一个占据轨道之间的相互作用,这种作用使得片段倾向于结合在一起;另一个部分是片段自己的占据轨道和自己的空轨道的相互作用,这种作用导致片段本身的进一步极化。该项一般为负(如果成键)。
片段发生相互作用(对应ΔE
orb
),结合在一起,电子密度会发生变化,密度变化量可以表达为:
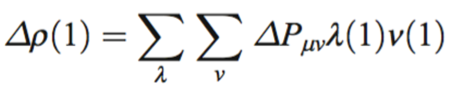
其中1表示坐标,μ和ν分别表示所有片段的占据轨道和空轨道。
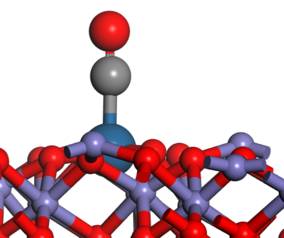
在ETS-NOCV方法中,ΔE
orb
的表达式: