提起溶出度,我想所有的药物研发的工作者都不陌生,众所周知大多口服固体制剂在给药后必经通过吸收入血液循环
,
达一定血药浓度方能达到治疗疾病的目的,而药物的被吸收的前提条件又是取决于药物从制剂中的溶出或释放、药物在生理条件下的溶解以及在胃肠道的渗透,因此溶出度实验成了评价口服固体制剂性能的重要实验,通过该实验可以充分药物质量、处方和工艺过程。最重要的是,可以通过该实验评价药物的体内行为。
通过上述简要介绍,溶出度考察的重要性已经不言而喻,那么在固体口服制剂溶出度的研究中到底有哪些因素会对溶出度产生影响的呢,下面就针对影响固体制剂溶出度的主要因素,小编就从多个方面阐述改善固体制剂的溶出度的方法。
1.
药物晶型的影响
对于多晶型药物,不同的多晶型分子空间排列不同
,
溶解度有差异,不同固体间溶解度的差异就会直接导致固有溶出速率的差异
,
进而影响制剂在体内的吸收和生物利用度,不仅如此,不同多晶型还可能有不同的水吸附性、稳定性,有些时候也会对颗粒压片成型的性能及某些辅料的润滑性产生影响。
2.
药物粒径的影响
说起粒径大小和溶出度的关系,可以用
Noyes-Whitney
公式进行表示:
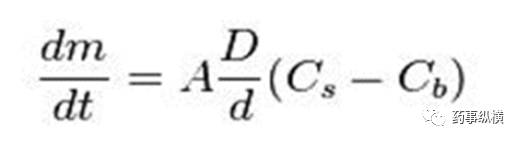
m:
材料的质量
t
:时间
D
:扩散系数
A
:比表面积
d
:溶质表面溶剂的边界层厚度
Cs
:在表面溶质的质量浓度
Cb
:在溶剂中溶质的质量浓度
通过上式我们可以清楚了解到粒径的大小一般跟参数
A
(比表面积)和
d
(溶质表面溶剂的边界层厚度)有关;对于参数
A
(比表面积),一般情况下,随着粒径的减小,其粒度细微均匀,参数
A
比表面积增大,孔隙率增加,吸附性增强,溶解性增强,亲和力变大,化学反应速率增加,改善了药物的溶出度,能使有效成分较好地分散、溶解在胃液里,且与胃黏膜的接触面积变大,更易被胃肠道吸收,从而提高了生物利用度,达到更好的治疗效果,有研究结果证实,
同等重量的药物,细粉比粗粉的绝对生物利用度提高
20%
。
一般情况下粒度越小,表面积越大,溶解越快,
但粒径并不和溶出度成线性关系,当粒径减小的一定程度后,颗粒表面越来越光滑,原药材特征越来越不明显,且微粉化技术的应用并未改变原药材的主要官能团结构,相反如果粒径太小,反而影响超微粉体的溶出效果。
3.
辅料对溶出度的影响
3.1
亲水性的填充剂对溶出度的影响
疏水性药物表面与水性介质间的接触角大
(>90
。
)
,毛细管作用力反向,不利于使水性介质渗入药物内部,从而使药物难以发生崩解溶出。若在疏水性药物中适当加入亲水性辅料,则有利于改善整个药物的亲水性,从而使水性介质易渗入药物内部后发生崩解溶出。它的作用机理是在处方中选用的亲水性辅料会在疏水性药物粒子的表面包上一层亲水性的
“
膜
”
,通过改善药物的润湿性从而促进药物的溶出。亲水性辅料的种类有很多,如具有毛细管作用的淀粉、微晶纤维素、甲基纤维素,乳糖、甘露醇以及酶类等等,上述亲水性辅料中乳糖改善溶出的作用最好,微晶纤维素作用较差,同时亲水性辅料改善溶出度的作用与其用量有关,如果亲水性辅料用量太少不足以覆盖疏水性药物粒子表面,不足以改善其润湿性,改善溶出度的作用也就不明显。
既然写到这里,在上述辅料中提到了甘露醇,那我们就对甘露醇作个简单的了解,甘露醇
-
有甜味,溶解时吸热,对口腔有舒服感,故广泛用于醒酒药、口中清凉剂等咀嚼片的制造,其颗粒型专作直接压片的赋形剂。注意:
甘露醇虽然不能被胃肠道很好的吸收,但能增加肠道渗透压,改变胃肠道中的水通量。这个渗透压在肠道的上部和下部都能改变胃排空和肠道转运时间。
众所周知,吸收药物的总量取决于药物在肠道中的吸收速率和药物在肠道中停留的总时间,因此甘露醇能够显著影响全身给药药物的吸收
。除了甘露醇外,木糖醇和山梨醇也有相似的功效,
PEG400
也已被证明会影响药物的吸收。因此对此类辅料的使用应格外注意。
3.2
表面活性剂对溶出度的影响
表面活性剂的使用能够从五个方面对药物吸收产生影响:
①表面活性剂的使用不但能降低药物界面张力的作用,使固体药物与胃肠道体液间的接触角变小,而且还能增加疏水性药物粒子表面的润湿性,从而加速药物的溶出和吸收。
②表面活性剂的使用能够防止片剂崩解产生的细小粒子聚结(反絮凝),能够使药物分散后保持较大的比表面积,从而加速药物的释放。
③表面活性剂的使用能够溶解上皮细胞的脂质体,从而提高上皮细胞膜的渗透性,可使药物的吸收增加。
④表面活性剂能形成胶束,从而对难溶性药物起增溶作用,可加快药物的溶出。
⑤表面活性剂能与某些药物相互作用形成复合物,其溶解度、分子大小、扩散速度、油水分配系数等发生变化,故能够增强或降低药物对生物膜的渗透性。
常用表面活性剂有聚山梨酯类、司盘类等。如
0.1
%聚山梨酯
80
的加入可促进非那西丁的溶出,浓度在
0
~
0.1
%的范围以内,聚山梨酯
80
的浓度愈高,溶出愈快。当然,在选用表面活性剂时不但要选用得当,而且还要用量适当,这样才能达到药物增溶的目的。注意如果表面活性剂的浓度增加至临界胶团浓度时,药物被包裹或镶嵌于胶团中而又不易被释放出,反而会影响药物的溶出。
3.3
黏合剂对溶出度的影响
3.3.1
粘合剂的种类对溶出度的影响
采用聚乙烯吡咯烷酮(
PVP
)作黏合剂制成的颗粒,表面具亲水性,压片后
水分易湿润而渗入片剂内部,崩解快,有利于药物的溶出。如研究人员利用
PVP
制成槲皮素固体分散体,使槲皮素在水中的溶解度增加
7~110
倍。而羟丙基甲基纤维素
(HPMC)
作为黏合剂可降低药物的接触角,使药物易于润湿,故能有效地改变片剂的二次崩解,从而显著提高溶出度。
但是,一些采用淀粉浆作黏合剂进行湿法制粒的,则制剂溶出度明显不理想。
国内生产的复方磺胺甲噁唑片(
Co.SMZ
)原用淀粉浆制粒,改用
HPMC
后,溶出速率从
20
分钟的
40%~50%
上升至
80%
。同时据小编了解如果在辛伐他汀片中使用羟丙基纤维素作粘合剂,也会致使辛伐他汀片的溶出速率大幅度的提高;粘合剂的选择及使用请参考来自药事纵横文竹先生的《(汇总)粘合剂的种类、特征与正确选型》一文,本文总结的甚是全面,小编在这里就不献丑了。
3.3.2
粘合剂的加入工艺对溶出度的影响
影响溶出度不只有粘合剂的种类,研究中发现粘合剂的的加入工艺:例如粘合剂的加入温度、加入方式、加入速度和加入时间均会影响溶出度产生影响。下面我们拿粘合剂的加入温度来举例说明温度是如何影响溶出度如下图所示:
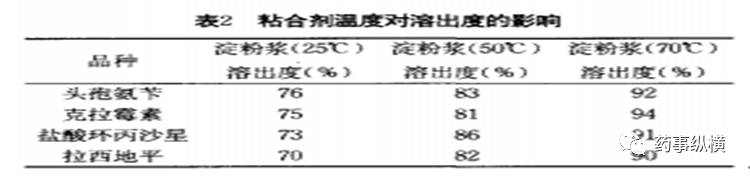
从上表可以看出淀粉浆的温度越低,淀粉浆的粘度就越大,与主药结合后不能均匀的润湿原料药,出现局部过湿现象,制得的颗粒不均匀,硬度增大,使药物溶出度减小。
3.4
崩解剂的种类及加入方式对溶出度的影响
关于片剂中加入崩解剂促使片剂崩解的机理,国内外有很多人进行了研究,其见解不尽相同,被较多人接受的机理有以下几个,即:
(
1
)崩解剂吸水膨胀,体积增大,产生膨胀力(又称崩解力)而使片剂的结合力瓦解,此一机理被很多人承认。不少学者测定了淀粉粒的吸水膨胀性能。目前国内外公认为性能较好的崩解剂如羧甲基淀粉钠、低取代
—
羟丙纤维素、羧甲基纤维素钙等都有较强的吸水膨胀性能;
(
2
)崩解剂可增加片剂的孔隙率,不少人曾以淀粉为崩解剂做实验,的确可增加某些片剂的孔隙率;
(
3
)崩解剂被水润湿时产生润湿热,使片剂孔隙中的空气的温度升高而压力增大;
(
4
)崩解剂在片剂中产生一结合力较小的
“
弱结合点
”
,所以有利于崩解等等,后三种机理使用的范围较窄。
崩解剂不同,其崩解作用不同,淀粉是常用的崩解剂,但其崩解性能并不好,目前国内外公认性能较好的崩解剂有羧甲基淀粉钠(
CMS-Na
)
,
低取代度的羟丙纤维素(
L-HPC
),羧甲基纤维素钙(
CMC-Ca
),交联羧甲基纤维素和交联
PVP
等。前两种国内已有辅料厂正式生产,内在质量已达到或接近国外同产品的水平,仅色泽等项稍差,已在国内较大范围内推广,取得很好的社会效益。
CMC-Ca
正在审批生产和试用中,交联
CMC
和交联
PVP
有待研制。
以上几种崩解剂的崩解性能都与其分子结构(聚合度、取代度)有关,例如高取代度的羟丙纤维素不宜用为崩解剂,常为粘合剂和片剂等的包衣材料。此外,各种崩解剂都有各自的适用范围,例如
CMS-Na
对多数片剂的崩解作用很好,但对阿司匹林不太适用;由国外引进的某些制剂规定必须使用
CMS-Na
为崩解剂。
崩解剂的用量和加入方法也有影响,在一定范围内,崩解剂的用量增多,片剂崩解加快,但有些崩解剂本身的
‘
可压性
’
不好,用量太多致使片剂的硬度降低。崩解剂的加入方法有三种,即:
(
1
)外加法,崩解剂与干燥后的颗粒混合,崩解剂位于颗粒之外;
(
2
)内加法,在制粒前加入,崩解剂位于颗粒之内;
(
3
)内、外加法,即部分崩解剂加入颗粒之内,另一部分混入干燥的颗粒中。
试验证明,当崩解剂的用量相同时,采用外加法制成的片剂崩解快,但崩解后形成的粒子较粗,随后再缓缓崩解成药物原粉;内加法制成的片剂崩解较慢,但崩解后形成的粒子较细,比表面积大,有利于药物溶出;内、外加法制成的药片的崩解速度和粒子细度属于两者之间。
片剂的崩解是一个比较复杂的过程,其机理和影响因素复杂,与片剂的原、辅料,压力等等都有关系,如用微晶纤维素作辅料压成之药片是因氢键结合而成型,遇极性溶剂后氢键断开,片剂的结合力瓦解等等,小编在此不一一讨论。崩解剂的选择及使用请参考来自药事纵横文竹先生的《(汇总)各种崩解剂特性对比及其使用要点解析》一文,本文对崩解剂的剖析颇有深度,小编在这里就不拾人牙慧了。
3.5
运用适宜的助流剂对溶出度的影响
助流剂是降低颗粒间磨差力的辅料,一般在压片前加入,他能够增加颗粒的流动性,以满足高速压片机所需要的迅速、均匀的填充要求,其最终目的是保证片剂的片重差异符合要求,微粉硅胶和玉米淀粉均是良好的助流剂。
提起微粉硅胶,不得不对其进行一个简要的介绍,微粉硅胶(即无定形
SiO2
)早期被作为吸附剂,其吸水、吸油性能好,是带负电荷的触变胶,很轻,每克表面积为
300
~
350
平方米。对带正电荷的药物,它能在药物表面形成负电膜,流动性佳,是亲水性很强的难溶性物质,通过毛细作用来辅助崩解。微粉硅胶能吸附难溶解性药物,可以将微粉后的原料和微粉硅胶混合均匀再加入其它辅料混合,利用微粉硅胶吸附难溶性药物作为增加溶解性的方法;其实在研究中发现也可以直接将微粉硅胶溶到粘合剂里面,可以增加主药的比表面积,从而大大加快药物的崩解,来提高某些药物的溶出速率。
3.6.
润滑剂种类和用量对溶出度的影响
润滑剂是用于降低颗粒和片剂与冲模之间摩擦力的辅料,常在压片前加入混合使用,能够起到较好的抗黏连的作用,减小片剂的出片力,常用的润滑剂包括硬脂酸、硬脂酸镁、硬脂酸钙、氢化蓖麻油等等。其中对于硬脂酸镁、硬脂酸钙等疏水性辅料的使用应当格外注意,如果此类辅料在处方中用量过大或者在工艺中混合时间过长,有可能使润滑剂均匀的覆盖在药物粒子表面,由于其较强的疏水性,会阻碍水分的进入,从而延缓药物的溶出速度。
小编曾在研究某药物时,由于厂家无法提供大粒径的原料药,尝试了很多方案都无法减缓药物的溶出速率,最后就是利用先将原料药和硬脂酸镁过度混合后,再和其他辅料混合压片,使用该方法处理后做到了减缓自制品的溶出速率,实现了和参比制剂的完美拟合。
4.
工艺对溶出的影响
4.1
工艺路线的选择对溶出度的影响
当配方相同,制备工艺路线选择不同时也会对药物的溶出产生显著的影响。我们可以从改变制备工艺路线来提高药物的溶出。小编在几年的研发历程中也遇到过类似的问题:某原研药物在其专利和文献资料中公布的制备工艺路线是干法制粒工艺,因此在该仿制药研发的初期我们一直采用和原研产品一样的工艺路线
--
干法制粒进行研究,采用干法制粒工艺路线上我们用了三个月的时间进行了相关研究始终无法做到在区分力介质下的溶出曲线拟合,并且自制品的溶出终点较参比制剂慢十几个点。
后再次查阅相关资料,对该原料药的性质进行了仔细分析,通过原料药影响因素和强制降解实验数据的认真分析,我们发现该原料只是对湿不稳定,但对热的稳定性良好,后我们认为可以选择湿法制粒工艺进行尝试性研究,我们将粘合剂溶于乙醇溶液,后通过高剪切湿法制粒设备进行制粒,压片,对使用该工艺的处方进行溶出度考察发现不但解决了溶出终点的问题,而且还实现了和参比制剂溶出曲线的完美拟合。同时后期该产品的稳定性研究成果表明杂质无明显增长,也证明了使用湿法制粒工艺路线的可行性。
4.2
原辅料加入顺序对溶出度的影响
同样的药物辅料,混合方法的不同则会可能得到不同的溶出速度。例如:
①湿法制粒前将处方量的辅料崩解剂加入到原料中制粒
(
内加法
)
,制粒后将处方量的辅料崩解剂加入到干颗粒中混合
(
外加法
)
,以及将处方量部分辅料崩解剂加入到原料中制粒,剩余部分辅料崩解剂加入到干颗粒中混合
(
内外加法
)
。通过实验比较证明崩解溶出性能为:内外加法
>
外加法
>
内加法。
②还可采用将量小的药物先溶于适宜的溶剂中再与辅料混合,增大表面积,
③将药物与亲水性辅料共同混合粉碎,有效的降低药物的表面自由能,减少了药物细粒聚集现象的发生。上述方法均表明原辅料的加入顺序能够药物的溶出速率。
4.3
制粒设备对溶出度的影响
药物的颗粒粒度对于药物的质量有着直接的影响,颗粒度对药物的溶出性能起决定作用。颗粒的粒度、均匀度、流动性影响着片剂的硬度、重量差异和含量均匀度。
颗粒的粒度越小,压出片的硬度越大,而均与度、流动性好的颗粒才能保证重量差异小,药物含量分布均匀,颗粒的二次崩解好从而改善药物的溶出性能,采用不同的制粒设备,例如采用流化床一部制粒、高剪切湿法制粒机混合制粒、挤出滚圆机的一步挤出滚圆制粒等均能制得的颗粒大小均匀、外观原整、流动性好,干燥后均能得到近似球形的细小颗粒,这种颗粒制得的片剂往往外观光洁细腻,药物溶出比较均匀。
而使用摇摆式制粒机时需要注意,摇摆式制粒机的制粒工艺是滚轴往复搓,拌软材,挤压出颗粒,制得的颗粒往往硬度较大,崩解度、释放度、颗粒的二次崩解等方面有时会出现问题,进而可能会对药物溶出度产生不良影响。
4.4
颗粒的粒度分布对溶出度的影响
不同的粒度分布肯定会对药物溶出度产生影响,下面有小编来举例说明这一问题:分别取供试原料,按照工艺处方制粒后,分别用
2
、
4
、
5
、
6
号筛网整粒,得不同粒径的颗粒,取各种颗粒,分别用压片机压片,用智能溶出仪按照药典方法检测溶出度,测得不同粒径颗粒相应的溶出度,结果见下图:
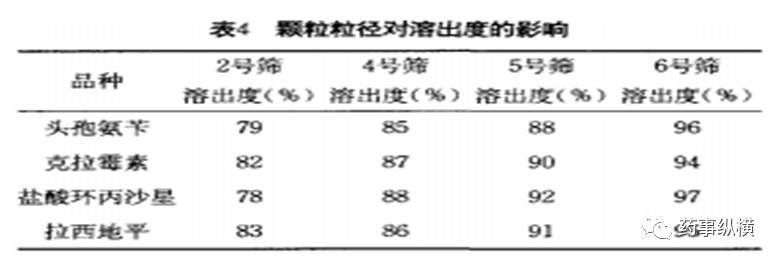
从上图可以清楚的看出不同粒径的颗粒测得的溶出度也不相同,一般会随着颗粒粒径的增大颗粒逐渐降低。因此在处方工艺考察期间,颗粒的粒度分布是药物考察的一个极其重要的一个指标。
4.5
压片工艺对溶出度的影响
在压片时应着重于压力、片重、硬度等的调节,压力的大小可改变骨架片的密度,使片剂的比表面积、孔隙率和孔道率发生变化,从而影响药物的释放。一般情况下,压力越大,片剂比表面积、孔隙率及孔径减小,水分子进入片剂内部的速度变慢,崩解时间延长。但是,比表面积并不总是随着压力的增大而减小,一些药物片剂存在一个表面积最大时的压力(临界压力),在此压力之前加压,主要是颗粒或结晶的破碎,所以压力越大,片剂比表面积越大,吸水速率快,一次崩解快。因此,在压片时应着重于将压力调整在适宜的度上。
同样我们借鉴一个例子来更加直观的来说明这一问题:分别取供试原料,按照工艺处方制粒后,整粒,混合,再保证其他工艺条件不变的条件下,只改变压片机压力进行压片,用智能溶出仪按照药典方法检测溶出度,测得不同压力条件相应的溶出度,结果见下图:
 结果显示:不同分装压力条件下,不同品种的溶出度也不相同,对于口服速释片剂一般情况随着压力增大,溶出度有所降低。
结果显示:不同分装压力条件下,不同品种的溶出度也不相同,对于口服速释片剂一般情况随着压力增大,溶出度有所降低。
4.6
包衣工艺对溶出的影响
根据小编几年的药物研发经验,小编认为包衣工艺和制粒工艺终点的判断,是药物研发中的两大难点,考察包衣工艺不仅仅要考察包衣增重,包衣片包衣材料的选择、包衣片片心水分的控制、包衣片干燥温度和干燥时间均会对片剂后期稳定性考察期间的片心性状、溶出度和有关物质产生重大影响,对于一些特殊的品种包衣房间空气的温湿度和包衣锅的大小均会影响包衣的效果。
具体包衣是怎么影响溶出度的,还是让小编来举例说明吧。小编同事曾研发过这样一个复方制剂,处方工艺研究完成后进行了小试三批放大,同时对三批样品均进行了稳定性留样考察,在对三批加速三月样品溶出度考察时发现有一批样品无法在介质中崩散,同时掰开片剂发现片心成由原来的类白色变化为淡黄色,后通过回看原始记录,发现不能崩散批次在包衣片在包衣过程中相比于其他两批次包衣速率较快,包衣片最后阶段包衣干燥时间较短。后通过完善包衣工艺,顺利解决了该问题。
5.
结论
影响片剂溶出度的因素太多太多,小编认为绝不仅仅是小编总结的这些因素,小编始终认为要想成为制剂大咖,就要永远不断的去实践、
实践
、
实践
,总结、总结、总结,只有不断去汲取新的知识才能够拓展研发的思路,只有不断在实践中总结经验才能拥有解决问题的能力。来吧,朋友,让我们一起携手,从
保障人民的健康为出发点,让我们共同做好药,放心药。
参考文献
-
现代药物制剂技术丛书:口服缓控释制剂
-
现代药物制剂技术丛书:口服药物吸收与转运
-
固体口服制剂的研发
-
药学理论与实践
-
FDA
生物等效性标准
-
片剂包衣的工艺和原理
郑俊民译
-
药剂辅料大全
作者:罗明生、高天慧
-
片剂溶出度影响因素分析
作者:闫丽、商萍
-
影响片剂溶出度的因素探讨作者:李芳美
孟凡秋,任职于上海博志研新药物科技有限公司制剂研究员。上海博志研新药物技术有限公司起步于2007年,是一家专门从事药物发现、研究、技术服务的高科技企业。业务范围主要聚焦于高端仿制药的委托开发、仿制药一致性评价、临床试验开展、创新药物发现,高质量药物中间体生产和销售,同时开展全球药品引进业务。
更多干货尽在药事纵横网站,地址:www.pharmaguider.cn,可点击原文链接一键直达。

药事纵横是一个开放,由自愿者组成的团体,现有成员13名,分别为 Voyager88(魏利军),雷诺岛,三分话,Herman,Mzwinsunny,文竹,duke,巉巉之石,占小兵,ISAL,海角边,yhqqqqq,鲁礼
炎,欢迎有志之士加入我们团队。投稿、加专业微信群【合成、制剂、分析、注册、BD、一致性评价】请加微信442015666,QQ群:22711679




