整理:赵旭锋
来源:蒲公英(发表于2017-09-29)
一、前言
我们收集了FDA2017财年,除编号320-17-50警告信外的其它50封警告信。所以,除表1外,其它的表格将不对320-17-50进行统计,而是按照50封警告信的数量进行分析。
我们在对警告信内容进行进行分类之后,进行了一些些统计和总结,这些不同角度分析和总结我们将分批进行发布,希望对看到的各位有所帮助!
二、FDA警告信初始资料分析
2.1 FDA警告信初始资料
我们对所收集的FDA警告信中的初始资料进行了统计,内容包括:被通报公司、公司所在地及被通报公司的产品类别(API或(和)制剂),结果见表1:FDA警告信的初始资料统计表。
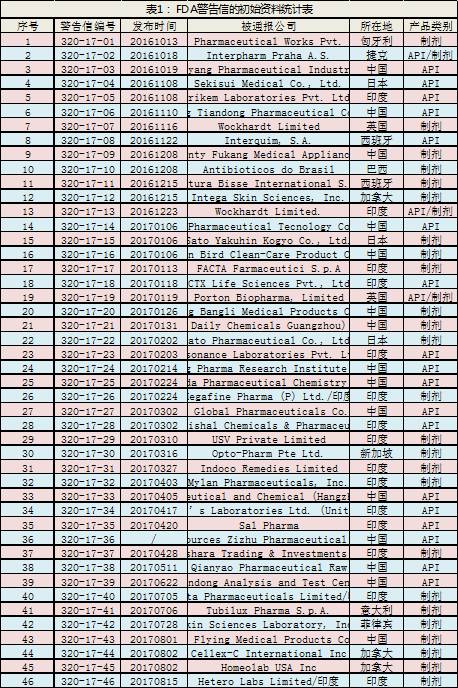
2.2 警告信涉及公司所在国分析
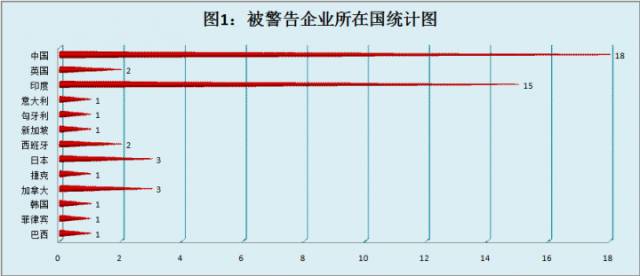
2.2.1 我们对被警告公司的所在国进行了汇总,可知被警告企业来自13个国家,其中以中国18次最多,其次为印度15次,再次为日本和加拿大,分别为3次。分析见图1:被警告企业所在国统计图。
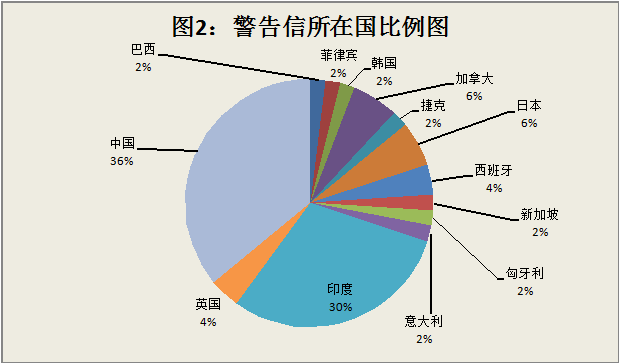
2.2.2 通过分析,可知中国收到的警告信占所有警告信的36%,印度为30%,日本和加拿大分别为6%,所以排名前二国家收到的警告信数量占2017财年警告信总量的66%。前三的4个国家收到的警告信数量占总量的78%,其余9个国家占省下的22%。分析见图2:警告信所在国比例图。
2.3 警告信涉及公司的产品类别分析
我们对被警告的50家企业的产品按照API或制剂,进行了分类,当企业的产品同时涉及API和制剂时,将其分开进行计算。
2.3.1 制剂企业
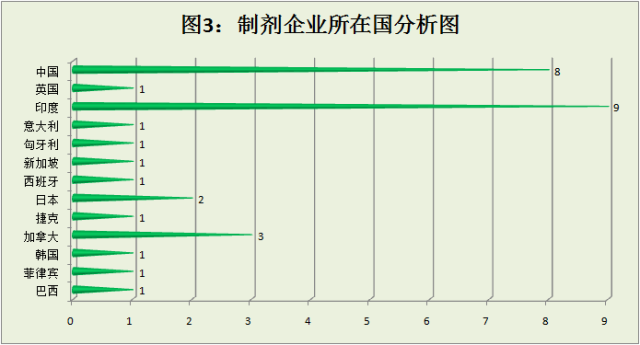
被警告的企业中制剂企业为31家,占所有50家企业的62%。其中以印度(9家,29%)最多,其次为中国(8次,26%),再次为加拿大(3次,10%)。分析见图
3:制剂企业所在国分析图;图4:制剂企业所在国比例图
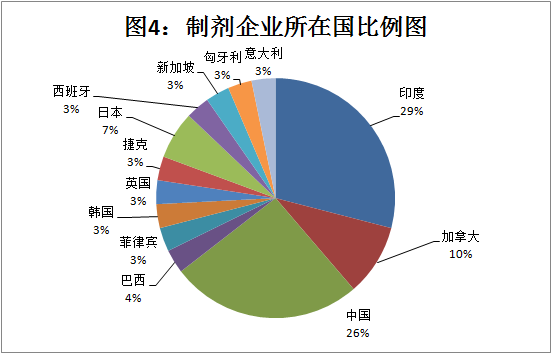
2.3.2 API企业
被警告的企业中API企业为22家,占所有50家企业的44%。其中以中国(10家,45%)最多,其次为印度(7次,32%),再次为英国(2次,9%)。中国和印度占所有API生产企业的77%。分析见图5:API生产企业所在国分析图;图6:API生产企业所在国比例图
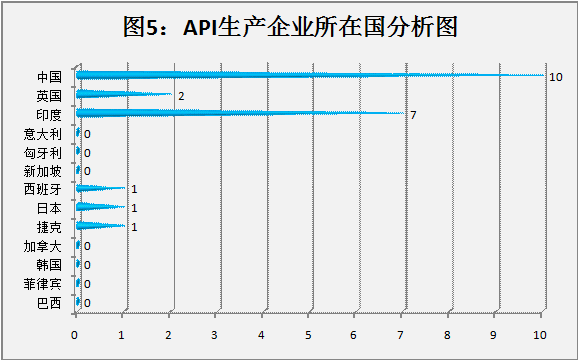
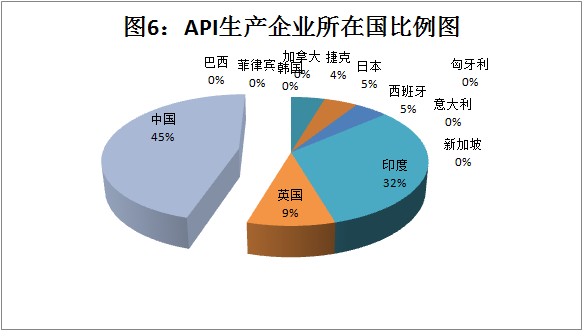
三:结论
3.1 在FDA即将结束的2017财年(本文统计日期截止为9月27日)发布的警告信51封,涉及13个国家,其中被警告企业在中国的最多为18次、36%;其次为印度15次、30%。
3.2 警告信中涉及制剂企业31次,其中在印度最多9次,29%;其次为中国8次,26%; 警告信中涉及API企业22次,其中在中国最多10次,45%;其次为印度7次,32%。通过以上数据可知,17财年警告FDA发出的警告信多集中的中国和印度两个。
3.3 通过警告信数量虽然说明以上两国在药品质量管理还需要进行很大的改进,但也说明美国在中国和印度进行了大量的药品采购。
3.4 但是通过API和制剂企业的比例也说明,API的生产基本已经从西方发达国家转移到了欠发达地区,其中以中国最多,但制剂却是印度最多。所以我们的制剂还要继续努力才行。
3.5 制剂和API的数量之和大于50,是因其中有几家同时生产API和制剂的企业;文中提到的国家为被警告企业生产工厂所在国,不代表生产企业为该国企业。
四、感谢
感谢此次为FDA资料收集与分析付出大量工作的朱玉娇娇姐、帅哥唐晓宇和北重楼。
…………………………………………………………………………
本文在蒲公英首发,如转载请于论坛或作者联系。
汉佛莱医药专注于为客户提供新药·仿制药·生物药FDA注册开发相关的技术支持、法规咨询服务,也为客户提供医药产品产业化开发、市场开发、投融资、项目转让/并购相关的商业咨询服务。本公众号归汉佛莱医药顾问所有,因此文章重点关注制药工业领域的技术、法规、市场等方面的选题,并尽可能保持客观、公正和中立,若其中可能存在的商业利益相关的不客观不真实,敬请批评指正!
专注FDA注册
国内最大的FDA法规团队
中美两地的办公室协同办公
多名前FDA审评官员全职加盟
国内首家实现美国FDA电子申报
独立的咨询数据库·丰富的外部顾问资源















