
就在今天,准确的说是美国当地时间 7 月 12 日,FDA 肿瘤药物咨询委员会(ODAC)以 10:0 的全票通过表决结果,一致建议批准诺华公司的一款 CAR-T 治疗产品——CTL019 上市。
该产品的适用人群是罹患急性淋巴细胞白血病的复发性或难治性儿童患者和年轻患者。如果完成审批流程,这将是全球首个被批准用于临床的 CAR-T 治疗产品。
CAR-T,实际上是一种经过特殊改造的 T 细胞,中文名是嵌合抗原受体 T 细胞,英文全称为 Chimeric Antigen ReceptorT-Cell Immunotherapy 。用它进行肿瘤治疗的这种方法,就称之为「CAR-T 疗法」,大致通过以下步骤进行:
从患者体内提取 T 细胞
↓↓
利用基因工程技术将其改造为 CAR-T 细胞
↓↓
大量扩增 CAR-T 细胞
↓↓
将其输回至患者体内展开治疗
从它「原材料」T 细胞可以看出,这款世人瞩目的肿瘤治疗手段正是脱胎于免疫疗法。
2013 年,Science 杂志曾将肿瘤免疫治疗列为年度十大科学突破的首位,其中特别提到了 CAR-T 细胞。
CAR-T 疗法其实总计有 300 多项正在进行的研究,其中涉及 CTL019 的有 33 项,此次获批就是基于前期临床试验结果。
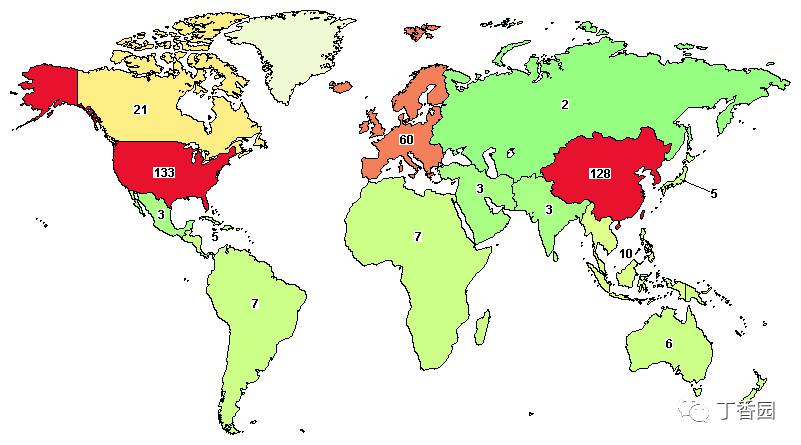
300 多项正在进行的 CAR-T 临床试验中
就有 120 多项来自中国
CTL019 最早源自宾夕法尼亚大学布鲁斯 · 莱文领导的课题组。
2010 年,莱文教授利用 CTL019 令 3 名已被宣判无药可医的白血病患者获得临床治愈,因而引起公众与业界的极大关注。
基于 CTL019 的临床试验(ELIANA 研究)的数据显示,在接受 CTL019 治疗的 3 个月后,高达 82%(n = 41/50)的患者实现完全缓解或伴有不完全血液计数恢复的完全缓解。
之后的 JULIET 研究发现,全球范围内有 51 名患者参与了临床试验,总缓解率达 45%(n = 23/51),其中 37%的病人完全响应(CR),8%的病人部分响应(PR)。
这些振奋人心的结果使之在今年 3 月底和 4 月下旬分别获得 FDA 授予的优先评审资格和突破性疗法认定,并最终迎来了如今的一致推荐,获得 FDA 咨询委员会全票通过。
以 CAR-T 为代表的免疫疗法,令很多人萌生出攻克癌症的曙光就在前方的憧憬。但可以说,这距离「攻克肿瘤」还有很长的距离。主要原因有 3 个:
1. 适应证局限于血液肿瘤
虽然从理论上讲,通过改变 CAR-T 的胞外抗原结合区,可以令其瞄准其他类型的肿瘤,但目前人们发现的肿瘤特异抗原少之又少,而且实体瘤的微环境相对复杂,这使得 CAR-T 疗法尚难于在实体瘤领域发挥用武之地。
我们都还记得魏则西,他当时患的是滑膜肉瘤,一种在国内尚未证实细胞免疫治疗的恶性肿瘤,而其接受的是另外一种细胞免疫疗法(DC-CIK)。最后魏则西因治疗无效离开人世。
而其逝世后,整个国内的细胞免疫治疗领域都受到重大影响。2016 年 5 月初,国家卫计委在视频会议中重申,自体免疫细胞治疗技术仍然属于临床研究,不能进入医疗临床应用。
2. 脱靶效应
这是指在治疗过程中的「误伤」正常细胞。
CAR-T 细胞的杀伤对象是所有表达靶标抗原的细胞,如果一些正常细胞也表达这种抗原,那么就会在治疗过程中被一并杀伤。
譬如,有研究者在进行 CAR-T 细胞治疗转移性肾癌的临床试验时,因为肾癌细胞与胆道细胞表达同样的靶标抗原,导致患者出现了严重的肝中毒。
3. 细胞因子释放综合征
在使用 CAR-T 治疗的过程中,病人会出现发热、疲乏、头痛、癫痫、恶心、寒颤、呼吸困难、急性呼吸窘迫综合征、低血压、急性血管渗漏综合征、心动过速、肝功能损害和肾功能衰竭等症状。
好在人们在对付这类副作用已经有了相当的经验,通过严密的监测和处理,可以实现良好的控制。
尽管有重重困难,但是,这仍旧是肿瘤治疗发展的重要里程碑。这次 Car-T 新药的专家批准,就是其上市前最关键的一步,其前景不可估量。
本文来源:丁香园
责任编辑:lightningwing、汪小鱼
题图来源:视觉中国


参考文献:
1. Determine Efficacy and Safety of CTL019 in Pediatric Patients With Relapsed and Refractory B-cell ALL (ELIANA) https://clinicaltrials.gov/ct2/show/NCT02435849
2. Study of Efficacy and Safety of CTL019 in Adult DLBCL Patients (JULIET) https://clinicaltrials.gov/ct2/show/NCT02445248














