
恩美曲妥珠单抗(T-DM1)是全球首个获批上市的乳腺癌抗体偶联药物(ADC)。
2018 年,发表于 New England Journal of Medicine 的 Ⅲ 期开放标签试验 KATHERINE 的主要分析显示,与曲妥珠单抗相比,恩美曲妥珠单抗辅助治疗可使新辅助治疗后仍残留侵袭性病灶的早期乳腺癌的进展或死亡风险降低 50%[1]。
基于 KATHERINE 的 iDFS 数据,恩美曲妥珠单抗已先后在美国食品药品监督管理局(FDA)和中国国家药品监督管理局(NMPA)获得批准,用于既往接受过以紫杉烷类联合曲妥珠单抗为基础的新辅助治疗后,仍残留侵袭性病灶的 HER2 阳性早期乳腺癌患者的辅助治疗。
2025 年 1 月 15 日,KATHERINE 研究携 iDFS 最终分析数据和总生存期(OS)第二次期中分析数据再度亮相 New England Journal of Medicine,证实恩美曲妥珠单抗辅助治疗可显著延长 HER2 阳性早期乳腺癌患者(新辅助治疗后仍有残留浸润性病灶)的 OS,并持续改善 iDFS[2]。
 图 1.KATHERINE 研究最新数据(来自 NEJM 官网)
图 1.KATHERINE 研究最新数据(来自 NEJM 官网)
ADC 辅助治疗早期乳腺癌,3 年 iDFS 率显著提升
既往研究数据表明,尽管 HER2 阳性早期乳腺癌患者在接受新辅助系统治疗后的初期疗效较好,但仍面临较高的复发与死亡风险。同时,45%-66% 的早期乳腺癌患者接受新辅助治疗后仍存在浸润性病灶,其预后普遍较差,亟待更为高效的辅助治疗方案以改善患者生存获益[2]。
KATHERINE 研究的主要分析数据发表在 New England Journal of Medicine,结果显示恩美曲妥珠单抗组 3 年无侵袭性疾病生存(iDFS)率显著高于曲妥珠单抗组(88.3% vs. 77.0%;侵袭性疾病或死亡的风险比为 0.50;P < 0.001),且安全性与之前的研究一致[1]。
此次公布的 KATHERINE 研究 iDFS 最终分析结果以及 OS 第二次期中分析结果,将进一步证实恩美曲妥珠单抗在治疗早期乳腺癌患者中的长期疗效与安全性[2]。
KATHERINE 研究再度探索 ADC 辅助治疗长期疗效
KATHERINE(BO27938)是一项随机、多中心、开放标签 III 期临床试验,共招募了 1486 例 HER2 阳性的早期乳腺癌患者。这些患者在入组前均接受基于紫杉烷类联合曲妥珠单抗的新辅助治疗,但治疗后在乳腺和/或腋窝淋巴结中检测到浸润性肿瘤残留病灶。在参与研究治疗期间,患者可根据当地治疗指南选择性地接受放疗和/或内分泌治疗。患者被按 1:1 的比例被随机分配至两组,分别接受恩美曲妥珠单抗或曲妥珠单抗治疗。
 图 2.KATHERINE 研究设计(来自 NEJM 官网)
图 2.KATHERINE 研究设计(来自 NEJM 官网)
分层因素包括患者的临床分期、激素受体状态、术前是否接受过 HER2 靶向治疗(曲妥珠单抗单独使用或联合其他 HER2 靶向药物)以及新辅助治疗后的淋巴结病理状态。
治疗方案为:每 21 天(每个周期)的第 1 天,静脉输注 3.6 mg/kg 的恩美曲妥珠单抗,或同个周期的第 1 天静脉给予 6 mg/kg 的曲妥珠单抗。患者将持续接受治疗,直至完成 14 个周期的治疗周期,或因疾病复发、撤回知情同意或出现不可耐受的毒性反应而终止治疗。
该研究的主要疗效评估指标是无侵袭性疾病生存期(iDFS),其他次要终点包括将第二原发癌(非乳腺癌)纳入考虑的 iDFS、无病生存期(DFS)、OS 以及无远处复发间期(DRFI),以全面评估两种治疗方案的长期疗效与安全性。
7 年 iDFS 率提升 13.7%,7 年 OS 率提升 4.7%
截至临床截止日期(2023 年 10 月 5 日),恩美曲妥珠单抗组与曲妥珠单抗组的患者试验参与和生存情况如下:
恩美曲妥珠单抗组:
存活且仍在试验中的患者数:521 例(占比 70.1%)
因侵袭性疾病事件或死亡而退出试验的患者数:105 例(占比 14.1%)
曲妥珠单抗组:
存活且仍在试验中的患者数:461 例(占比 62.0%)
因侵袭性疾病事件或死亡而退出试验的患者数:159 例(占比 21.4%)
恩美曲妥珠单抗组的 7 年 iDFS 率提升 13.7 个百分点
 图 3. 研究主要终点 iDFS
图 3. 研究主要终点 iDFS
中位随访时间达到 8.4 年,恩美曲妥珠单抗组在 iDFS 方面展现出了持续的改善,恩美曲妥珠单抗组 7 年 iDFS 率的估计值为 80.8%,而标准辅助治疗组则为 67.1%,即恩美曲妥珠单抗组的 iDFS 率相较标准辅助治疗组显著提高了 13.7%(HR:0.54;95% CI:0.44-0.66)。进一步的亚组分析显示,恩美曲妥珠单抗组在不同患者群体中均展现出持续的优势。无论患者的激素受体状态、新辅助治疗的选择、手术时病理淋巴结的状态、年龄、种族或是疾病的严重程度如何,恩美曲妥珠单抗组均能显著降低侵袭性疾病事件或死亡事件的风险,整体风险降低幅度大约为 50%。
恩美曲妥珠单抗组的 7 年 OS 率提升 4.7 个百分点
 图 4. 研究关键次要终点 OS
图 4. 研究关键次要终点 OS
恩美曲妥珠单抗组报告了 89 例死亡事件(占总人数的 12.0%),而曲妥珠单抗组则报告了 126 例死亡事件(占总人数的 17.0%)。在 7 年 OS 率估计值方面,恩美曲妥珠单抗组和标准辅助治疗组分别为 89.1% vs. 84.4%,前者比后者的 7 年 OS 率高出 4.7 个百分点,同时恩美曲妥珠单抗组患者的死亡风险显著降低 34%(HR:0.66,95%CI:0.51-0.87,P = 0.0003)。
OS 的亚组分析结果显示,恩美曲妥珠单抗对于初始治疗时不可手术的患者以及新辅助治疗后腋窝淋巴结仍为阳性的可手术患者均显示出获益。然而,在激素受体阴性且经过新辅助治疗后腋窝淋巴结转为阴性的可手术患者中,并未观察到恩美曲妥珠单抗带来的明显获益,尽管这一亚组中的死亡病例数量相对较少。
在包括将第二原发癌(非乳腺癌)纳入考虑的 iDFS、DFS 以及 DRFI 等其他次要终点方面,恩美曲妥珠单抗的表现也均优于曲妥珠单抗。
恩美曲妥珠单抗组和曲妥珠单抗组治疗相关不良事件(AE)的总体发生率较低,安全性可控。在整个试验期间,恩美曲妥珠单抗组的 ≥ 3 级 AE 发生率为 26.1%,而曲妥珠单抗组中这一比例为 15.7%,两组最常见的 ≥ 3 级 AE 均为血液毒性(9% vs. 5%)。此外,恩美曲妥珠单抗组和曲妥珠单抗组分别有 12.7% 和 8.1% 的患者报告了严重不良事件。针对与试验治疗或试验设计相关的不良事件进行分析的结果显示,两组的心血管事件和其他毒性效应均较为罕见。
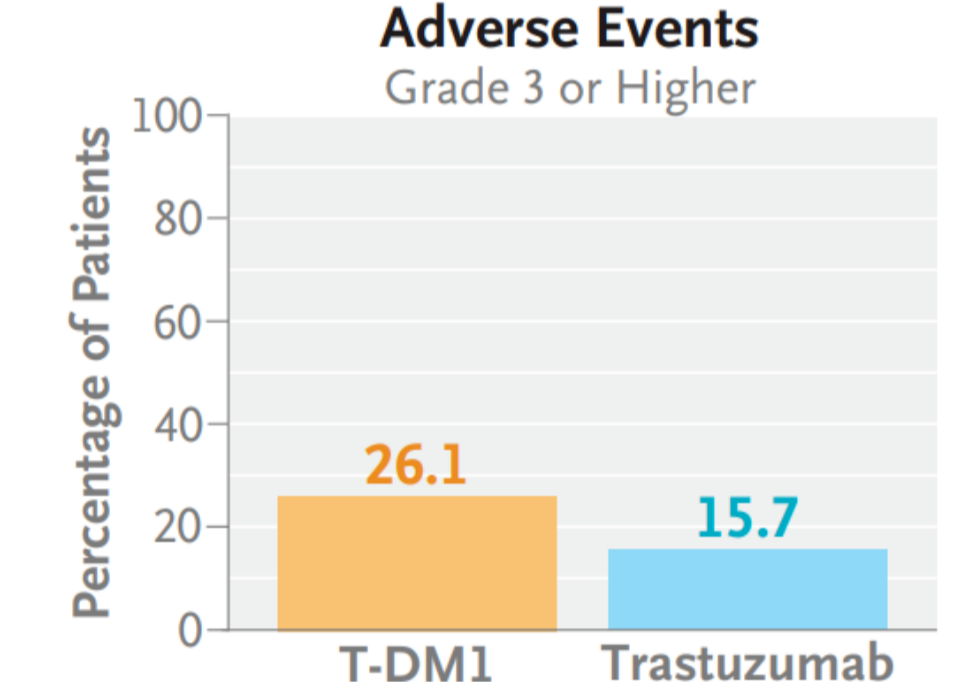 图 5. 恩美曲妥珠单抗组和曲妥珠单抗组的 ≥ 3 级 AE 发生率
图 5. 恩美曲妥珠单抗组和曲妥珠单抗组的 ≥ 3 级 AE 发生率
KATHERINE 试验的长期随访分析显示,恩美曲妥珠单抗在 iDFS(7 年 iDFS 率:恩美曲妥珠单抗组 80.8% vs. 曲妥珠单抗组 67.1%)和 OS(7 年 OS 率:恩美曲妥珠单抗组 89.1% vs. 曲妥珠单抗组 84.4%)方面均显著优于曲妥珠单抗,且安全性表现良好。此外,恩美曲妥珠单抗还在其他次要疗效终点上展现出优势。值得注意的是,尽管恩美曲妥珠单抗有效降低了非中枢神经系统(CNS)的远处复发风险,但 CNS 复发风险并未显著降低,这提示我们需进一步探索其他疗法,以优化早期高危乳腺癌患者的治疗策略。目前,已有多项临床试验正致力于研究恩美曲妥珠单抗与其他药物的联合应用,以期改善这些患者的预后。[1] von Minckwitz G, Huang C-S, Mano MS, et al. Trastuzumab emtansine for residual invasive HER2-positive breast cancer. N Engl J Med 2019;380:617-628.[2] Geyer CE Jr, Untch M, Huang CS, et al. Survival with Trastuzumab Emtansine in Residual HER2-Positive Breast Cancer. N Engl J Med. 2025;392(3):249-257. doi:10.1056/NEJMoa2406070.















