北京大学生命科学学院、北大-清华生命科学联合中心徐成冉课题组在《Cell Metabolism》(《细胞▪代谢》)杂志上发表了题为“Deciphering Pancreatic Islet β Cell and α Cell Maturation Pathways and Characteristic Features at the Single-Cell Level”的研究论文。首次在单细胞水平上分析了胰岛β和α细胞成熟、增殖和异质性建立等重要问题。
同日,
在《Hepatology》(《肝脏学》)杂志上发表了题为“
A single-cell transcriptomic analysis reveals precise pathways and regulatory mechanisms underlying hepatoblast differentiation
”的研究论文。该研究揭示了双潜能的成肝细胞分化为肝实质细胞和肝内胆管细胞的分子路径及调控机制。
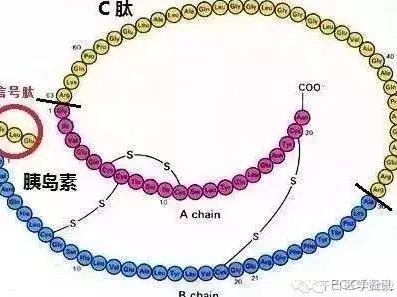
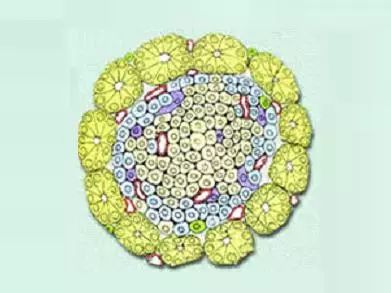
胰岛
β和α细胞在机体血糖平衡和代谢稳态维持中具有重要作用。对胰岛细胞增殖和成熟的体内调控机制以及细胞异质性的研究对糖尿病细胞水平的治疗有重大意义。
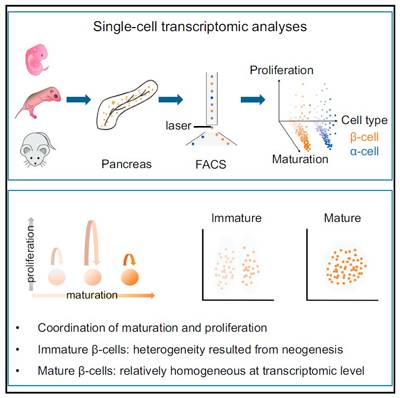
该工作利用遗传标记的小鼠,通过流式细胞技术分选出不同发育
/成熟阶段的β和α细胞并进行单细胞转录组分析,确立了β和α细胞成熟路径。进一步分析发现,β和α细胞在成熟过程中采用不同的调控策略。本研究通过在单细胞水平上对增殖和静息细胞的表达谱比较分析,发现增殖和分化两大互斥事件可以在β细胞成熟过程中得以协调,表现为增殖细胞与静息细胞的分化/成熟进程基本同步。另外,该研究还发现β和α细胞的异质性主要发生在发育早期,成熟期的胰岛细胞在基因表达水平基本均质,因此作者提出假说认为胰岛细胞的异质性的调控主要发生在转录后。在此基础上,该项研究创新性的整合了单细胞和大量细胞表达谱分析,确定了β细胞成熟过程重要转折点,为后续的功能研究提供了重要信息。本研究对胰岛成熟过程的深刻理解将促进体外干细胞定向诱导分化产生成熟胰岛细胞,或对如何促进糖尿病患者的胰岛细胞通过增殖恢复胰岛的生理功能提供思路。
北京大学徐成冉研究员为本文的通讯作者。北京大学生命科学学院博士研究生邱伟林、张雨薇、冯烨为第一作者。北京大学生命科学学院博士后李林宸、北大
-清华生命科学联合中心博士研究生杨柳为本研究做出了重要贡献。该项研究得到了国家科技部,国家自然科学基金以及北大-清华生命科学联合中心项目经费的支持。
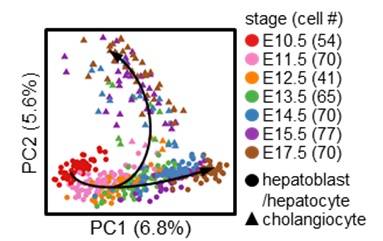
肝胆细胞分化发育
“默认-调控”路径
肝脏是重要的代谢调控及药物解毒器官,其结构组成和功能实现主要依赖于两类表皮细胞
——肝实质细胞和肝内胆管细胞。这两类细胞是在早期肝脏发育中由双潜能的成肝细胞分化形成。然而,我们对这个分化过程的特征及调控机制并不清楚。在该研究中,课题组建立了小鼠胚胎肝脏不同发育阶段肝胆细胞的富集方法,并通过单细胞测序技术系统地绘制了肝胆细胞分化发育图谱。分析发现,早期刚形成的成肝细胞已经开启了向肝实质细胞的分化方向,开始表达肝实质细胞分化发育相关的转录调控因子,这表明成肝细胞向肝实质细胞的命运转变是一个“默认”的过程。并且,每个发育时期的成肝细胞或肝实质细胞具有发育同步性,其沿着一条“线性”路径逐步推进。与之相反,肝内胆管细胞的分化发育“分支”于成肝细胞向肝实质细胞的转变过程,受到多种转录因子及信号通路分子的调控。并且,由于特化形成的时间不同及分布位置的差异,每个发育时期的肝内胆管细胞是高度异质的。因此,对于成肝细胞的分化过程,该研究描绘了一个全新的“默认-调控”发育方式。伴随着“默认-调控”发育方式的差异,肝实质细胞和肝内胆管细胞采取不同的机制控制细胞的增殖与分化。