
通过国际知名咨询机构Informa/Citeline公司的Pharmaprojects数据库,可以帮助我们全面了解2017年全球在研新药市场的一些新变化,及时发现新药研发的一些新趋势。
Pharmaprojects数据库收录的在研药品信息,特指目前处于在研状态的药品研发项目,包括处于临床前研究阶段的项目、处于不同临床研究阶段的项目、处于注册阶段的项目,以及增加新适应症的已上市药物。
根据Pharmaprojects最新数据,截至2017年1月,全球在研新药数量为14,872个,与2016年数据13,718相比,同比增幅高达8.4%。
从2001~2017年数据来看,全球在研新药数量保持稳定增长态势,尤其是2011年以来,全球在研新药数量呈现增长势头,且增幅明显。
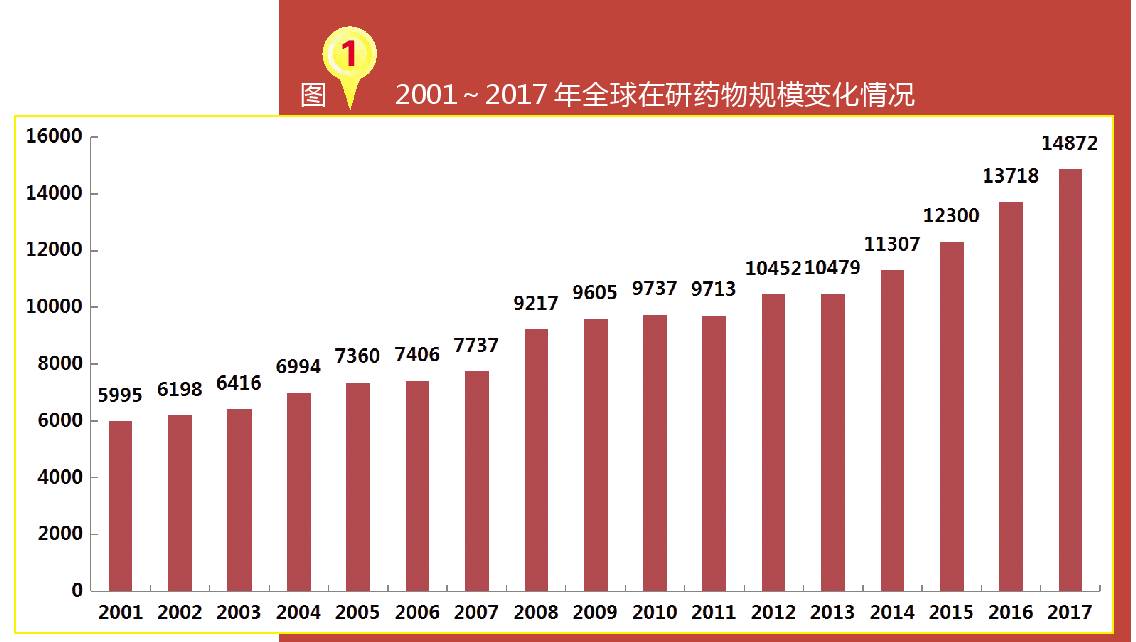
(数据来源:Pharmaprojects数据库)
然而需要注意的是,
2017年全球在研新药数量增速(同比增幅为8.4%)有所放缓,2016年和2015年全球在研新药数量增幅分别为11.5%和8.8%。
从在研药物数量的变化情况来看,2017年在研药物数量增加了1154个,较2016年数量(1418)有所下滑。
但是,如果说全球在研药物规模目前已达峰值,仍为时尚早。2017年统计数据所呈现出的增速放缓,并不能表明资源因素已对全球在研药物规模的扩张产生了影响。这也使得下一年数据更加值得期待,并将成为预判全球在研药物市场未来发展趋势的重要参考。
尽管全球在研新药数量呈现持续增长的态势,但由于化学合成小分子药物开发难度逐年增加,全球在研药物市场增长的可持续性仍存在一定的不确定性。对于制药行业,“上市的新药”就像是这个行业的“后代”。如果这个行业不能持续产生新的创新性实体药物,那么这个行业很有可能正在逐渐走向衰亡,并会影响整个社会对行业创新研发能力的支持力度。
需要注意的是,产品管线扩张速度下滑在一年前即已出现。
2015年,全球上市的NAS数量已从2014年的63个(含新分子实体NMEs 57个,疫苗6个)下降至46(含NMEs 43个,疫苗3个),这也是自2011年以来NAS数量出现的首次下滑。2016年,全球上市的新活性物质(NAS)数量继续呈现下滑态势。
从制药研发流程来看,新药研发大概可以分为三个阶段:首先,通过临床前研究发现并确认候选药物;其次,通过临床研究验证候选药物的有效性和安全性;最后,顺利通过注册及上市环节,最终实现候选药物的临床价值。
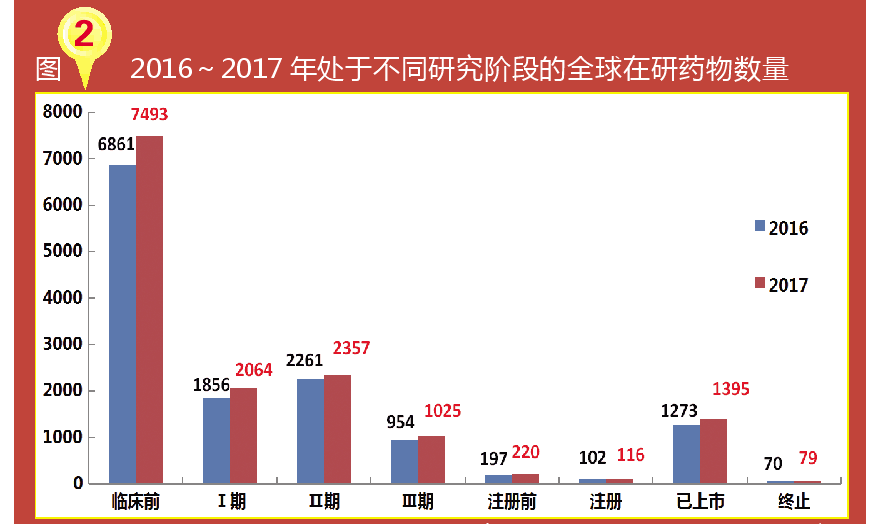
(数据来源:Pharmaprojects数据库)
通过对比2017年和2016年处于不同研发阶段的在研药物规模后不难发现,
几乎所有阶段的在研药物数量,均呈现稳定增长态势。
其中,处于临床前研究阶段的药物数量变化尤为明显,2017年处于该阶段的药物数量为7493个,较2016年数量(6861个)增加了632个候选药物,同比增幅为9.2%。此外,处于临床研究阶段(包括Ⅰ期、Ⅱ期和Ⅲ期临床阶段)、注册前、注册和上市阶段的在研药物数量也呈现出稳定增长势头,在研药物数量分别为5446、220、116和1395个,同比增幅分别为7.4%、11.7%、13.7%、9.6%。这些统计数据均表明,产品管线整体上呈现出蓬勃发展的势头。
从2007~2017年临床数据来看,临床研究各期的药物数量均呈增长态势。2017年处于Ⅰ期临床研究阶段的药物数量增幅最为明显,增幅为11.2%,该数字几乎为2007年数据的两倍。2017年处于Ⅱ期和Ⅲ期临床研究阶段的药物数量增幅分别为4.2%和7.4%。
从2007~2017年临床数据来看,临床研究各期的药物数量均呈现增长态势。2017年处于Ⅰ期临床研究阶段的药物数量增幅最为明显,增幅为11.2%,该数字几乎为2007年数据的两倍。2017年处于Ⅱ期和Ⅲ期临床研究阶段的药物数量增幅分别为4.2%和7.4%。
















