主要观点总结
文章介绍了NOVA DES®颅内药物洗脱支架的相关信息,包括其特点、研究背景、方法、结果等。
关键观点总结
关键观点1: 全球首款无神经毒性安全性的颅内药物支架
NOVA DES是首个无神经毒性安全性的颅内药物支架,具有治疗ICAS的潜力。
关键观点2: 研究背景
亚洲人群中ICAS缺血占比高,现有药物治疗仍存在卒中复发风险,尤其是重度ICAS患者。支架置入术是治疗的一种手段,但既往存在并发症和再狭窄问题。
关键观点3: 方法
共纳入24例症状性重度ICAS患者,使用NOVA支架进行治疗,评估其安全性、技术可行性及ISR发生率。
关键观点4: 结果
所有患者均成功植入NOVA支架,残余狭窄均小于30%,无出血并发症或死亡率。手术过程中和术后发生较少的并发症,如穿支闭塞和远端栓塞。NOVA支架在减少再狭窄和促进内皮愈合方面表现出优势。
关键观点5: NOVA支架的优势
NOVA支架具有专门的涂层技术以促进内皮化过程,药物释放周期与血管损伤愈合时间窗相匹配,并进行了严格的神经毒性测试,证明其安全性。
正文

精准治疗 持久安全
1年再狭窄6.66%,同裸支架比降低73.4%,从而降低再发卒中88.4%;
血管内皮愈合导向,28天药物峰值,60天吸收完毕。
亚洲人群中ICAS缺血占比高,尽管药物治疗仍然是首选治疗方法,但即使在强化药物治疗后,仍有一定的卒中复发风险存在,尤其是在重度ICAS(≥70%)的患者中。
对于
重度
I
CAS
(
≥
70
%
)的患者
,仍有
较高的卒中复发风险
。
因此有必要通过介入的方式,应用支架置入术进行治疗。
既往支架置入并发症和支架内再狭窄(ISR)发生率较高,限制了其发展。
随着神经介入技术和器械的发展,围手术期并发症似乎得到了令人满意的控制(WEAVE2.6%和AIRE-CHINA4.3%)。
然而,支架植入后由平滑肌增生引起的ISR高达33%,这是一个仍待继续解决的主要问题。
冠脉使用DESs已被证明可显著降低ISR的发生率。DES可通过抑制平滑肌细胞的迁移和增殖来减少支架植入后的ISR。在既往的一些研究中,使用冠状动脉DESs治疗颅内狭窄显示出良好的安全性和有效性的临床结果。然而,很少有关于使用颅内专用DESs治疗ICAS的报道。
2022年,缪中荣教授首次报道了在症状性sICAS患者中应用NOVA的结果。
NOVA支架
是首款专用于治疗ICAS的球扩DES,也是首款愈合导向的颅内支架。专利的eG™电子接枝涂层技术能够在内皮修复窗口内快速修复和覆盖内皮,降低ISR的发生率和缺血性事件复发的风险。
为了获得更多DES治疗ICAS的经验和证据,这项研究报道了NOVA支架治疗ICAS的单中心临床经验,旨在确定其安全性、技术可行性以及ISR发生率,为颅内DES的临床应用提供更多经验。
共纳入从2021年12月到2022年5月,我院接受
NOVA支架
置入的症状性重度ICAS患者24例。
入选标准:
(1)重度颅内动脉粥样硬化狭窄,根据WASID标准进行DSA确认狭窄程度≥70%;(2)颅内动脉粥样硬化狭窄引起的缺血性卒中;(3)NCCT或MRI显示脑分水岭梗死,CT或MRI灌注显示相关病变上低灌注;(4)HR-MRI-显示不稳定斑块;(5)强化药物治疗后仍有持续、加重或复发的缺血性神经功能缺损。
排除标准:
(1)梗死区严重出血转化;(2)靶血管严重成角(>45),或近端路径严重迂曲,使其不适合使用球扩支架。
术前准备:
所有患者在支架置入术前至少5天接受100 mg/天阿司匹林和75 mg/天氯吡格雷治疗≥。然后进行TEG试验,以排除耐药性。对于对氯吡格雷耐药的患者,我们将药物改为替格瑞洛(90 mg bid)。患者的胆固醇、血糖、血压等血管危险因素均得到了满意的控制。术前1天进行NCCT检查,排除脑卒中患者脑梗死区出血转化。
NOVA置入:
全麻,静脉注射肝素(70 U/kg),6F长鞘位于颈总动脉远端或
锁骨下动脉,靠近椎开口。通过长鞘将5F中间导管送至狭窄近端。在路图下,将0.014”的微导丝通过狭窄段。使用病变直径的80%的
LPS
球囊
对狭窄段进行预扩张,选择直径略小于相邻正常血管直径,长度覆盖狭窄段两端超出3mm的NOVA支架,为了避免血管夹层和破裂,需15-30s/atm的缓慢充盈。
术后管理:
术后所有患者均转入神经重症监护病房进行观察,并持续进行动脉血压监测,使SBP保持在100~120mmHg之间。立即行脑部CT检查以排除术后出血。如果患者的症状恶化或出现新的症状,将进行头部MRI检查,以确定原因是否由远端栓塞引起。术后患者继续服用双重抗血小板药物至少6个月,然后根据随访影像学结果决定是否停用一种药物。
共纳入24例患者(男性18例,女性6例),平均年龄62岁。从发作到DES置入的中位时间为24天。所有患者均有TIA和/或中风病史。表1、2总结了患者的基线特征。
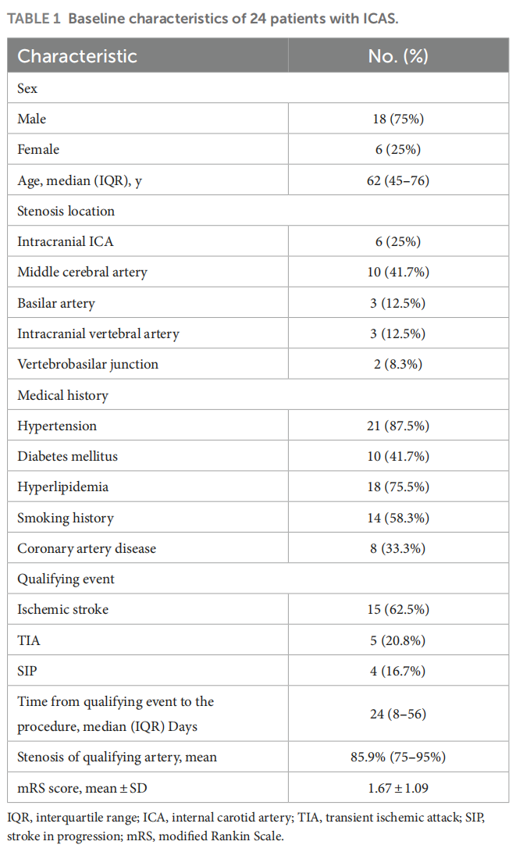
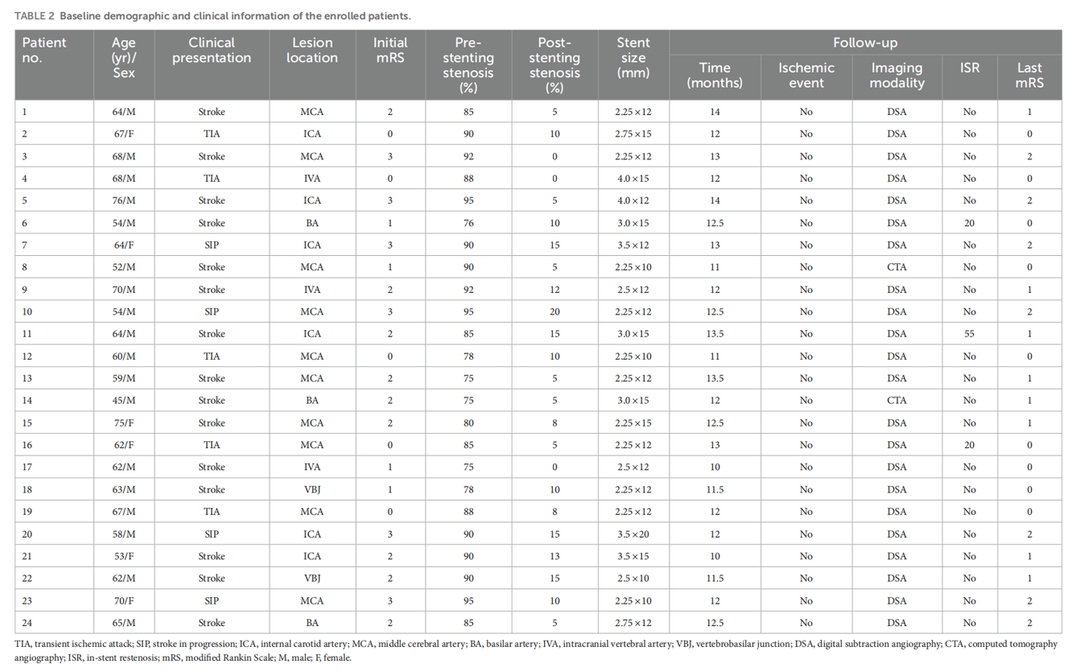
24例患者均成功植入
NOVA支架
,残余狭窄均小于30%,无出血并发症或死亡率。狭窄程度从平均85.9%降为平均8.6%。在手术过程中,1例因“雪犁”效应导致穿支闭塞,随后使用微导丝和替罗非班成功再通,术后未出现相关临床症状(图3)。1例出现症状性远端栓塞,术后观察为构音障碍和肌力下降,随后的头部MRI显示为脑桥梗死。在手术过程中和术后,没有发生血管夹层、支架移位、HPS或出血性转化。在24例接受NOVA放置的患者中,23例患者在术后1周保持稳定(n= 12)或出现症状改善(n = 11)。只有发生远端栓塞并发症的患者出现症状加重。所有患者的主要手术结果汇总见表2、3。
在我们的系列病例中,较低的围手术期并发症发生率取决于严格的患者选择标准和支架置入方案。在我们的研究中,我们对重度狭窄合并低灌注的患者行支架置入。事实上,如果低灌注是缺血性卒中的主要原因,那么通过PTAS恢复灌注将有助于预防卒中的复发。然而,由动脉粥样硬化斑块引起的血栓栓塞或穿支阻塞引起的缺血性中风可能最好使用药物治疗。
为了减少手术相关的并发症,可以考虑一些技术,包括在PTAS手术过程中应用长鞘和中间导管来提供稳定的支持。此外,考虑到球扩输送系统比自膨支架系统更硬,建议将中间导管尽可能放置在病变段附近,以便在支架输送过程中获得稳定的支持。
为了减少血管夹层或破裂的风险,球囊和支架的直径应该选择一个略小于邻近正常血管的直径,支架应缓慢扩张。
为降低高灌注或脑出血损伤的风险,球囊应缓慢泄压,患者SBP严格控制在低于120 mmHg或低于基线SBP 20 mmHg以下。
得益于这些方法,我们取得了100%的技术成功和0%的血管损伤和HPS发生率。
关于DESs的另一个主要问题是这些药物的神经毒性。一般来说,DESs使用的药物是抗癌药物(紫杉醇或雷帕霉素),它们缓慢释放到脑血管系统,影响脑组织。
NOVA支架
是一款快交球囊搭载的雷帕霉素洗脱支架系统,使用
eG™
电子接枝技术以共价键的形式和药物紧密连接在一起。
NOVA支架
雷帕霉素载药量为1.3μg/mm2。在动物实验中没有发现神经毒性,在随后的RCT临床试验和我们的系列病例中,证明
NOVA支架
在颅内血管内使用是安全的。
NOVA DES
是全球首款专门用于治疗ICAS的球扩DES,也是全球首款愈合导向的颅内支架。
与目前的冠脉DESs相比,
NOVA支架
具有以下优点:
首先,支架的材料不同。
NOVA支架
由316 L不锈钢制成,而冠状动脉DESs主要由钴铬合金制成。考虑到脑动脉比冠状动脉更曲折,不锈钢在支架植入后的屈服强度低于钴铬合金,贴壁性更好。虽然钴铬合金可以使支架更薄,但会增加支架血栓形成和再狭窄发生率,植入后通常需要支架后扩张,以确保完全贴壁。
其次,NOVA支架具有更好的涂层技术,以促进支架的内皮化过程。
它采用eG™涂层技术,可以促进内皮细胞的愈合和减少再狭窄。药物释放和药代动力学研究表明,药物释放周期与血管损伤愈合“时间窗”相匹配,支架放置后28天药物完全释放,符合平滑肌细胞增殖时间曲线,实现同步抑制血管壁平滑肌细胞和减少再狭窄。药物水平在60天内降至有效浓度以下,促进内皮细胞愈合,并在90天内几乎完全代谢,消除了该药物潜在的神经毒性安全隐患。追踪内皮细胞动力学,eG™涂层支架的内皮愈合速度是裸金属的2.5倍。与大多数冠状动脉DESs,如XIENCE DES相比,
NOVA
在减少支架后炎症、促进支架后内皮愈合和减少再狭窄方面更有效。
最后,在上市前,对该药物的神经毒性进行了严格的测试。
动物实验神经毒性研究评估
NOVA颅内药物洗脱支架
放置后,MRI结果显示各时间点的受试动物均没有远端脑组织出血或梗死;特殊染色结果显示神经纤维着色正常,无轴索变性,均未见明显空泡,未见明显的星形胶质细胞增生、小胶质细胞活化、神经退行性病变及轴突变性,药物支架组和裸支架组没有显著差异。然而,大多数冠脉DESs尚未在动物身上进行神经毒性测试。















