靶点的发现和确认,对于药学工作者而言,是一项既重要又艰巨的任务,通常,药物作用的新靶点一旦被发现,往往会成为一系列新药发现的突破口。于是,在寻找新的药物靶点上,各国科研人员不遗余力,各大药企纷纷投入重金进行各种试验,以期能够通过找到一个新的药物靶点而研发出超越对手的新药竞品。然而,失败的教训告诉我们,并非每一个功能型的生物大分子,都可以当做药物靶点去进行开发,生物大分子只有具有一定的特点,才可以被我们锁定继而开发成靶。所以,药物靶点的学习、理解和感悟,对于每个新药研发人员,就显得格外重要。
早在1891年,Paul Ehrlich(抗生素方面贡献突出)当时正在尝试用染料染色细菌细胞,期间提出,“细胞可能是一个‘大分子’,这种‘细胞-分子’存在‘侧链’来接收外部的营养”,并将其命名为“侧链受体”。Paul Ehrlich相信,细菌存在受体并可与染料分子发生化学反应,随后在接下来的试验中,又相继提出了“化疗”以及“药物是通过作用于靶点分子而发生作用”等概念和假说。如今,这一概念仍然存在,牛津生物化学词典将“药物靶点”定义为“与特殊化合物相互作用并被调节的生物实体,通常为蛋白或基因”。在那之后,一系列与之相关的学说相继产生,其中存在一定误导性的便是“一个药物对应一个靶点,且这个靶点是特殊且唯一的”......随着科学的不断进步,尤其是药理学的不断发展,大部分假说不攻自破。
随着科学的不断发展,如今药物靶点基本可定义为“能够与特定药物特异性结合并产生治疗疾病作用或调节生理功能作用的生物大分子或生物分子结构”。由此可知,药物靶点往往是生物大分子,并具有和一些特殊化合物能够“结合的部位”,当相应化学物质与之发生结合后,结构会发生适当的变化,且这个变化最好是“可逆的”。结构变化后的这个生物大分子,会发挥一定的生理病理作用,即表现出“药效”,且在机体复杂体系中占有主导作用。而病理条件下,该物质的表达、活性、结构或特性可以发生变化,这种变化可以是原发性,也可以是继发性的。此外,在体内可能存在内源性也可能存在外源性的能与该分子或结构结合的物质,这个结合的物质可以作为药物用于防治疾病。以上可以说,是一个生物大分子作为药物靶点最为基本的条件,当然,必然条件自然是存在相应的、合适的药物。
由于药物靶点的重要价值和作用,近年来,随着分子生物学、人类基因组、蛋白质组等生命科学和技术方法的发展,人们对药物靶点的研究热情空前高涨,药物靶点的发现和确证己经成为生命科学领域研究热点。且根据人类基因组研究结果预测的细胞内药物分子能作用的靶点,据保守估计,能够成为药物靶点的约有5000~10000个,这些靶点足够科研人员闷头研究一段时间了。
2016年,《Nature Reviews Drug Discovery》的两篇文章分析了2016年靶点的研究情况,其中一篇共涉及661个靶点(人类蛋白),285个为经过验证的靶点,376个为新靶点;另一篇共涉及893个人类和病原体衍生的生物分子(统计FDA批准的1578个药物),包括667个人类基因组衍生蛋白,这些靶点当中,G蛋白偶联受体、离子通道、激酶、核受体的研究相对较多。
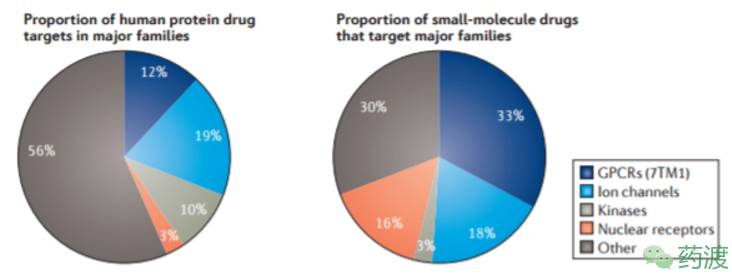
今天,探索药物靶点的方法已经有很多很多,而由于靶点在药物发现过程中的地位和价值,人们逐渐将关注点聚焦在了靶点的确认上。而靶点的确认自然离不开一些合适的分子,通过“基于靶点的筛选策略”和“表型筛选策略”可以先筛出一些感兴趣的候选药物,随后对靶点进行确认、验证,使之成为真正意义上的“药物靶点”。
对于靶点的验证过程,简要介绍如下:首先,确认靶点在细胞实验中是否具有调节化合物的生物活性,这可通过RNA干扰技术沉默某一基因(小鼠),观察是否具有药物作用后的症状,若药物没有引起效应,说明药物是通过这一特定靶点作用的。因此,候选靶点的同系物也要被纳入考虑范围,即使其在最初的筛选中并没有被识别。此外,一个物质可能具有功能性获得的活性,靶点的缺失亦会抑制此物质的活性。除了RNA干扰技术,也可以用cDNA过表达来建立药物-靶点作用关系,这种方法类似于酵母中的拷贝数抑制现象,靶点的过表达可能会抑制药物的活性,这种方法对于验证膜靶点极为重要。一旦假定的靶点通过功能实验的验证,就需要对小分子物质及靶点的亲和力进行量化。这一过程可以通过表面等离子共振或者等温量热法技术完成,如果假定的靶点是一种酶,则要通过酶动力学实验衡量此物质的酶活力。最后,需要通过NMR或共结晶实验进行更为严格的验证,进而得到药物-靶点复合物的三维结构。这些信息不仅可以验证物理上的关联性,也可以提供后期药物优化中结合模型的鉴定标准。
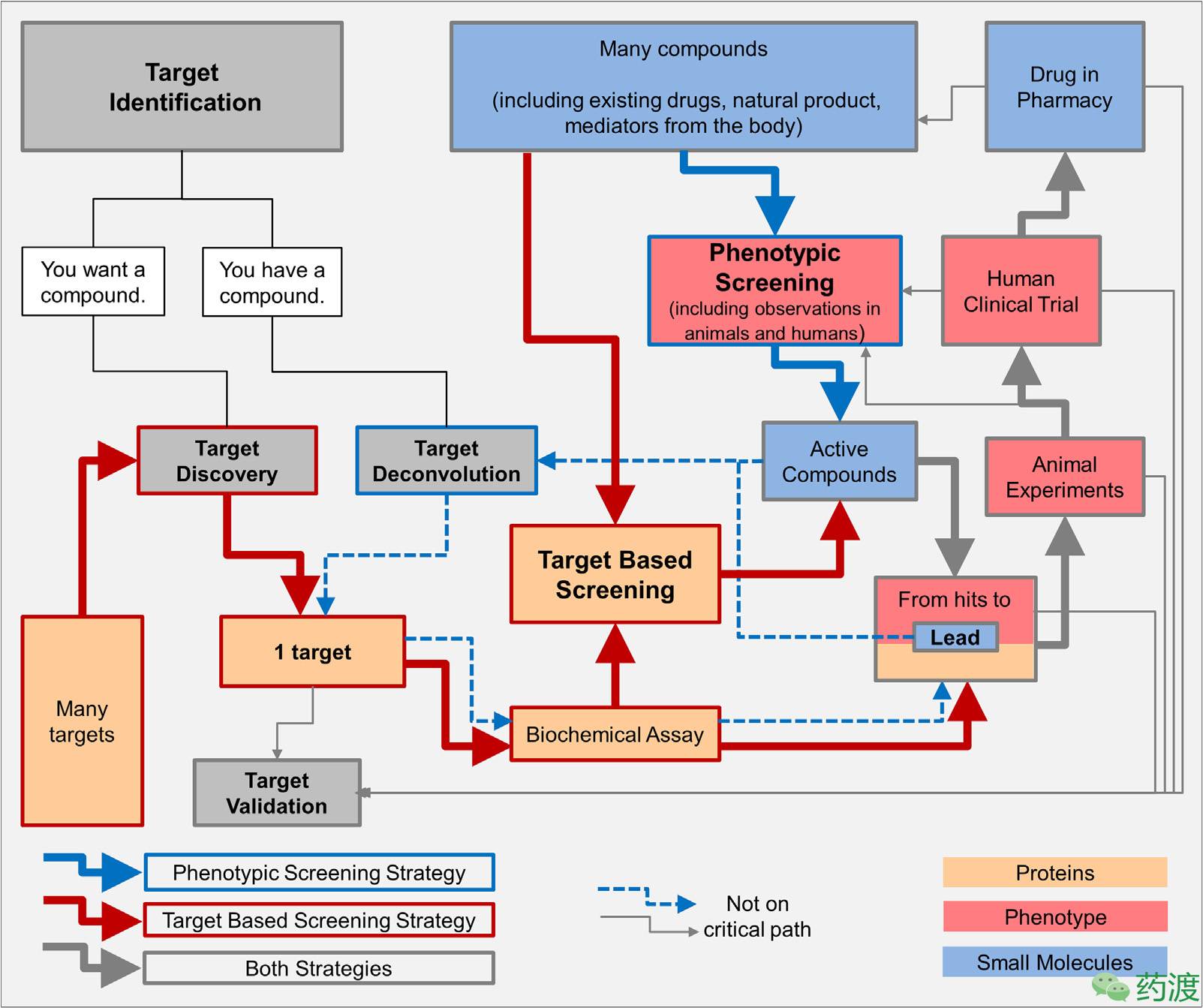
4. 靶点分类~“药物、候选药物、潜在药物靶点” & “特异、主导、优势药物靶点”
通过药物靶点的特点,很多人将药物靶点分成三类,即“药物靶点、候选药物靶点、潜在药物靶点”。所谓药物靶点,通常是指那些已经确认了的特定药物的作用靶点;当然,如果相应药物还没有研发成功、上市,也不能说就不是药物靶点,这些已具备了药物靶点基本特征的生物大分子或分子结构,尚需不断的研究、评价,故称之为候选药物靶点;而潜在药物靶点,是指那些仅发现了部分药物靶点的特征,但尚不具备药物靶点的多数条件,比如说有些具有重要功能的蛋白质,具备部分药物靶点的特征,可以作为一个潜在的药物靶点。还有一些蛋白质,虽然发现了一些功能,但尚没有认识到药物靶点相关的更多的特征,这些物质被称为药物靶点就太早点了,充其量就是一个功能蛋白。
而根据作用于靶点上的药物的作用特点,又可以将药物靶点分为“特异药物靶点、主导药物靶点、优势药物靶点”。所谓特异药物靶点,便是指作用于这类靶点上的药物可以发挥很好的药理作用,达到理想的防治疾病的效果(其中包含选择性、靶向内容);而主导药物靶点,就是该靶点的生理、病理、药理学功能在机体调节中占有主导地位;还有一类可以称为优势药物靶点,是指在生理病理条件下对机体的调节具有优势地位,作用该靶点的药物在发挥药理作用的同时,可能受到机体整体因素的影响,而表现出来的作用亦可能被干扰,这类药物靶点可以称为优势药物靶点。
首先,候选化合物能够与待开发的生物大分子结合,并不代表该生物大分子即为药物靶点。许多生物制药公司和研发机构在未取得科学的统计研究数据的情况下,仅根据少数几个粗略的实验结果就认为该靶点具有很好的开发前景,从而大规模地开展创新药物的研发工作。
相对容易开发的靶点,往往会得到一窝蜂的扎堆研究,很容易研究过头,而剩下的一些开发难度较大的生物大分子,则得不到优势研发实力的进入,如分布于多组织或与多个调节通路有关的靶点,使得研发资源存在浪费。
组合化学、高通量筛选被寄予了太大的希望,许多制药公司认为在进行人体试验之前充分地利用这些先进的技术来弄清药物与靶点的作用机制和可能产生的毒理学、药动学问题,从而实现药物优选的最大化,这样也就无形地增加靶点开发的时间并降低了新药上市的速度。
待开发的生物大分子是否能成为药物靶点,是需要候选化合物来证实的,而有些化合物天生就存在一些“残疾”,如体内代谢较快、含基因毒结构等,导致潜在的药物靶点也同步的被坑掉了。
大数据环境之下,药物靶点研究亦在其中,数据资源的挖掘和利用,已成为发现药物靶点的重要途径。随着生命科学和生物信息学的发展,越来越多的靶点结构得到解析,使药物靶点数据库的构建具有必要性及可能性。功能基因组学、蛋白组学、系统生物学、多向药理学、网络药理学等理论的提出,以及计算机辅助药物设计,计算机虚拟筛选等计算机技术的应用,对药物靶点数据库提出了更高的要求,推动药物靶点数据库进一步发展。药物靶点数据库收集和整理的药物靶点信息不尽相同,但主要有2类,一是针对已证实的药物靶点进行整理及管理,比如 Drug Target Database。二是除了证实的药物靶点外,还包括潜在的药物靶点的数据库,比如TTD。
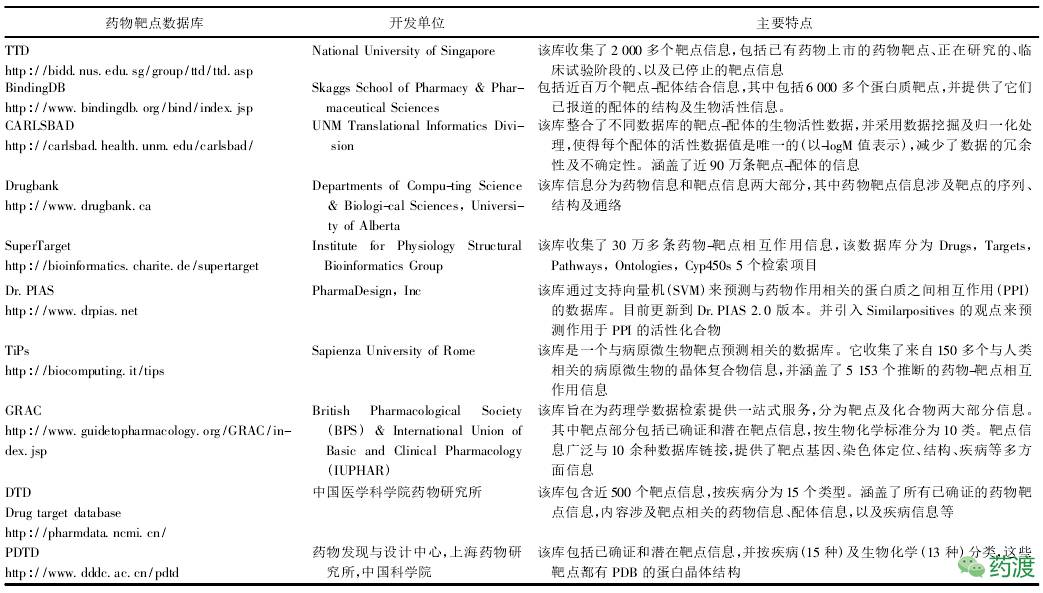
点击上图放大查看
“大众创业、万众创新”,制药行业虽为传统,但创新步伐亦不可或缺。在国家鼓励、支持创造我们自己的“新药”之时,各大科研院所、高校、药企亦改变研发方向,在新药的创制方面加大投入,层层加注。对于从事新药研发的科研人员来说,也许最早的“新药”概念,离不开三个字“化合物”,而程序自然就是查文献、了解靶点、设计母核、铺天盖地的化合物数量、发现先导、结构优化......等等等等,更多的精力可能会放在做化合物、期盼药理数据的“报晓”等方面。而今天,我们的研发程序可能改变不大,但要强调的是,对靶点的“怀疑”可谓时刻不敢掉以轻心,要知道,技术上的错误可以逐渐弥补,但方向上的错误,绝对是致命的。故而,药物化学的工作也就更多的要去学习药理学、分子生物学等相关学科的内容,只有多学科的进行杂糅,并形成一定的太极,也许才能更好的领悟“靶点”、领悟“新药”!
参考文献:
1. ZC Li,WQ Zhong,ZQ Liu,etal. Large-scale identification of potential drugtargets based on the topological features of human protein-protein interaction network [J]. Analytica Chimica Acta, 2015, 871: 18-27.
2. P Kumari,A Nath,R Chaube. Identification of human drug targets using machine-learning algorithms [J].Computers in Biology &Medicine,2015,56 (56C) :175-181.
3. CM Pichler,J Krysiak,R Breinbauer. Target identification of covalently binding drugs by activity-based protein profiling [J]. Bioorganic & Medicinal Chemistry,2016,24 (15) :3291.
4. R Breinbauer. Target identification of small molecule drugs and chemical probes [J]. Bioorganic & Medicinal Chemistry,2016,24 (15): 3231.
5. T Katsila,GA Spyroulias,GP Patrinos,et al. Computational approaches in target identification and drug discovery [J]. Computational& Structural Biotechnology Journal,2016,14: 177-184.
6. WMMVD Broeck. Chapter 3-Drug Targets,Target Identification,Validation,and Screening [J]. Practice of Medicinal Chemistry,2015: 45-70.
7. 杜冠华.药物靶点的发现和确证研究[C]. 中国药理学会药学发展前沿论坛, 2008:24-26.
8. 张音,王松俊,刁天喜.药物靶点的发展前景及需要解决的关键问题 [J]. 中国新药杂志,2009 (19): 1834-1837.
9. 崔大明.药物靶点筛选的研究 [J]. 中国卫生产业,2013 (14): 187-187.
10. 庞晓丛,刘艾林,杜冠华.药物靶点数据库的应用进展[J].中国药学杂志,2014,49(22): 1969-1972.
声明:
本文由药渡头条投稿作者撰写,观点仅代表作者本人,不代表药渡头条立场,欢迎交流补充。联系方式:010-82826195 转8048
如需转载,请务必注明文章作者和来源
投稿详情请点击“4月-5月 | 王牌写手获奖名单”