2018年7月5日,卫材(Eisai)与百健(Biogen)宣布,其抗β-淀粉样原纤维(anti-amyloid beta protofibril)的抗体BAN2401在一项II期临床试验BAN2401-G000-201中,最终早期
阿兹海默病
患者18个月研究结果达研究终点,显著延缓了阿兹海默病的进展评分,也减少了大脑中淀粉样蛋白的积聚。
值得注意的是,去年底Biogen曾发布了BAN2401在12个月分析结果未达首要临床研究终点的公告,一度加深了大家对Aβ假说的悲观情绪。回到18个月的次要研究终点上,由之前12个月时的贝叶斯分析变为设定的传统分析方法。最高剂量组结果呈现出统计学意义,包括ADCOMS(Alzheimer’s disease Composite Score )量表评分改善以及淀粉样蛋白累积减少,而这在之前的后期临床研究是没有过的。
因此BAN2401
此次
积极临床试验结果不仅是自己的救赎,更是对阿尔兹海默症Aβ假说的续命,是阿尔兹海默症治疗药物研究前行道路少有的亮光。
阿尔茨海默症是一种神经退行性疾病,临床上以记忆障碍等为主要症状。目前全世界每年导致死亡人数最多的十大疾病中,阿尔茨海默症是唯一仍不能治愈或有效控制病情的疾病。
据国际2015年世界
阿尔茨海默症
报告(World AD Report 2015)统计,全世界已有4680万
阿尔茨海默症
患者。每3.2秒就有一个新病人出现,并且预计2050年将达到1.3亿。
阿尔茨海默症
对全世界造成的经济损失2015年是8180亿美元,到2018年将达到1万亿美元。
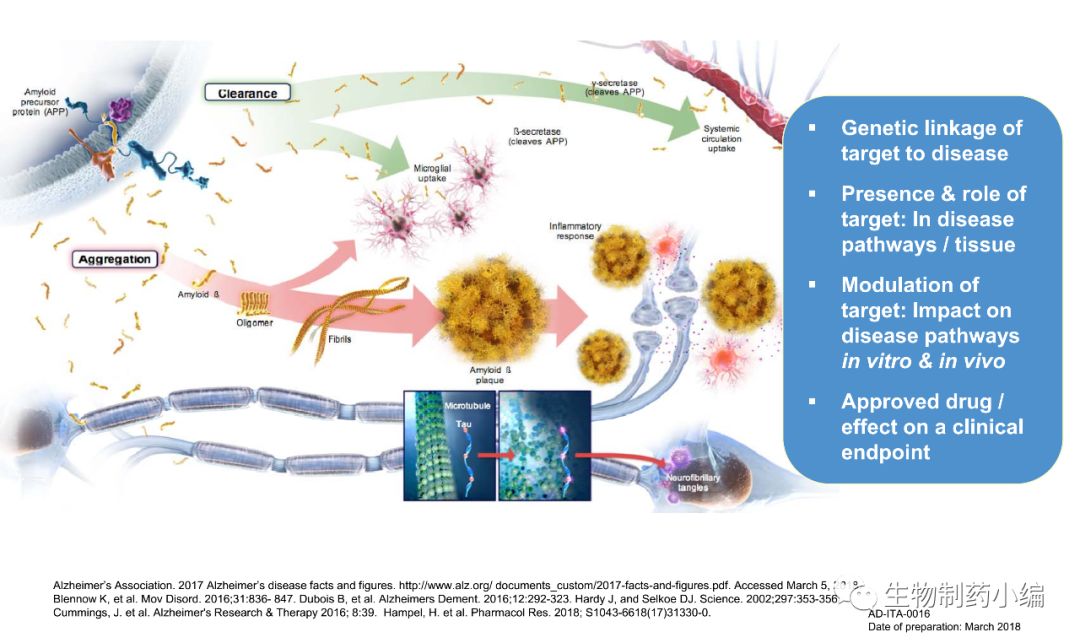
▲阿尔兹海默症的疾病机理(来源于Biogen官网)
阿尔茨海默症的发病机制极为复杂,至今尚未明确其确切的发病机制。β-淀粉样蛋白(Aβ)、Tau蛋白、ApoE4、突触核蛋白(α-synuclein)等被广泛认为与阿尔茨海默症的发病相关,但确切的机制仍有待更多临床试验的支撑。
(更多可参考前文:
【原创】阿尔茨海默症在研药物统计
)同时近十几年来,这一领域的药物研发几乎没有任何突破性进展。阿尔茨海默病就像是药物临床试验的百慕大——100多项临床试验在此折戟沉沙,在机制研究上可谓停滞不前。
1984年,科学家在阿尔兹海默病患者大脑中发现了由39-43个氨基酸组成的β-淀粉样蛋白(amyloid-β,Aβ)。研究发现Aβ是由一种广泛存在并集中表达于神经元突触部位的膜蛋白质(淀粉样前体蛋白,APP)经β-分泌酶和γ-分泌酶的蛋白水解作用而产生。
Aβ的积累导致突触功能减弱、影响相关的信号转导、改变神经元活性、引发神经胶质细胞释放神经毒性调节剂等。而当这种损伤达到一定的程度(一般可以持续10-30年),就会出现阿尔兹海默病的相关的临床表现。基于这个假说,人们显而易见地认为清除细胞外、外周血里面的β-淀粉样蛋白就可以达到治疗阿尔兹海默病的目的。
然而如果说阿尔茨海默病就像是药物临床试验的百慕大,那么Aβ假说就是阿尔茨海默病的黑洞,30年来无数药物前赴后继进入此靶点的研究,浮浮沉沉,该假说让人们在希望中收获绝望,又从绝望中寻找希望。
 ▲各
Aβ抗体与
Aβ的结合位点
(来源于Biogen官网)
▲各
Aβ抗体与
Aβ的结合位点
(来源于Biogen官网)
β-淀粉样蛋白最常见的亚型是Aβ1-40和Aβ1-42。而Aβ1-42具更容易聚集,形成Aβ沉淀的核心。虽然针对此靶点的药物众多,同时该假说也反复遇挫,但是前期药物结果反映结合Aβ1-42不同的部位还是会很大的临床差异。
从目前来看,结合Aβ N端的抗体更多,结合聚体状的Aβ在提高药效的同时可以显著减少副作用,结合Aβ更少氨基酸的抗体对于原纤维的Aβ清除作用更强,如BAN2401。
辉瑞/杨森的Bapineuzumab作为第一波Aβ假说探路者
,于2007年11月进入Ⅲ期临床试验。2012年,由于在两项后期临床中,相关于安慰剂并没有显著改善病情,辉瑞/杨森宣布终止Bapineuzumab的研发。
辉瑞的另一款可溶性的
Aβ结合抗体
Ponezumab随后也被放弃。
礼来也算是Aβ假说的坚定探路人。
2012 年,Solanezumab 的前两个Ⅲ期临床试验,远征1(EXPEDITION 1)和远征 2(EXPEDITION 2)的研究表明,1000名轻中度阿尔兹海默症患者服用Solanezumab18个月后治疗组和对照组没有明显差异。但礼来的科学家们并没有就此丧失信心,他们对EXPEDITION 1和EXPEDITION2的亚组数据进行了分析,推断Solanezumab可能对轻度阿尔兹海默症患者具有明显的认知及功能改善作用,并于2013年启动了第三个Ⅲ期临床试验EXPEDITION3,预计在2016年底完成。
2016年11月23日,礼来公司公布了EXPEDITION3的结果:Solanezumab并没能达到预期的理想效果,该日礼来公司股票也随之下跌14%,
礼来公司先后为此药的研发投入30亿美元,
但赢得了所有人的尊重。
就当人们以为礼来公司会彻底退出Aβ假说探索时,2016年12月9日,礼来与阿斯利康宣布达成一项全球合作协议,共同开发处于I期阶段的选择性β淀粉样蛋白42(Aβ42)抗体MEDI1814。
罗氏也广泛参与了
Aβ假说
的探索。
Gantenerumab在轻度AD临床试验失败后再度增加剂量重启III期临床;另一个与Solanezumab相似度较高的Crenezumab在轻中度AD临床2期未达主要终点的情况下增加剂量继续推进III期临床。罗氏在
Aβ假说的坚定程度与礼来相比有过之而不及,发表过
“dose is the problem”和“This isn't the end for beta amyloid”的豪情壮志。
百健的Aducanumab是目前最寄予厚望的
Aβ抗体
。
尽管2016年公布的Aducanumab的1期临床数据揭示能够有效减缓早期AD病人的认知功能减退,但如何控制副作用和进行中的2个
III期
临床是否能重复仍是个问题。但目前结构上看,
Aducanumab跟前期的
Aβ抗体还是有明显差异的,对于聚集化得
Aβ具有选择性清除的功能。
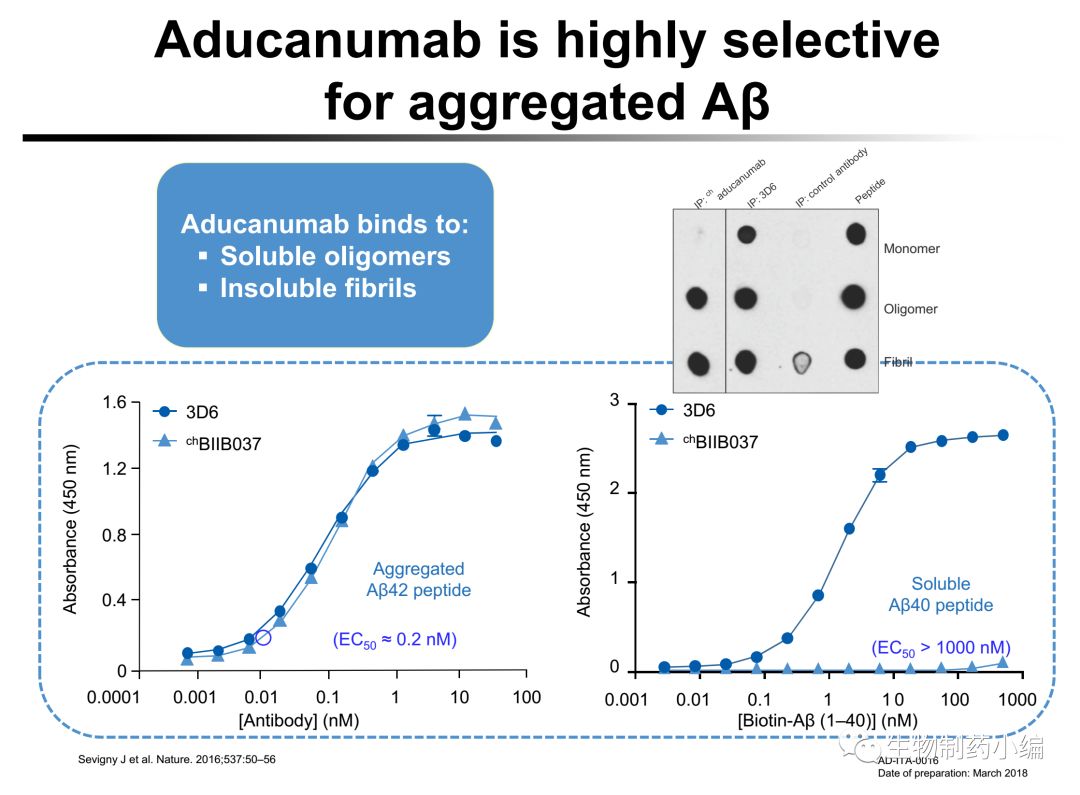 ▲
Aducanumab对于
Aβ聚体具有选择性的清除能力
(来源于Biogen官网)
▲
Aducanumab对于
Aβ聚体具有选择性的清除能力
(来源于Biogen官网)
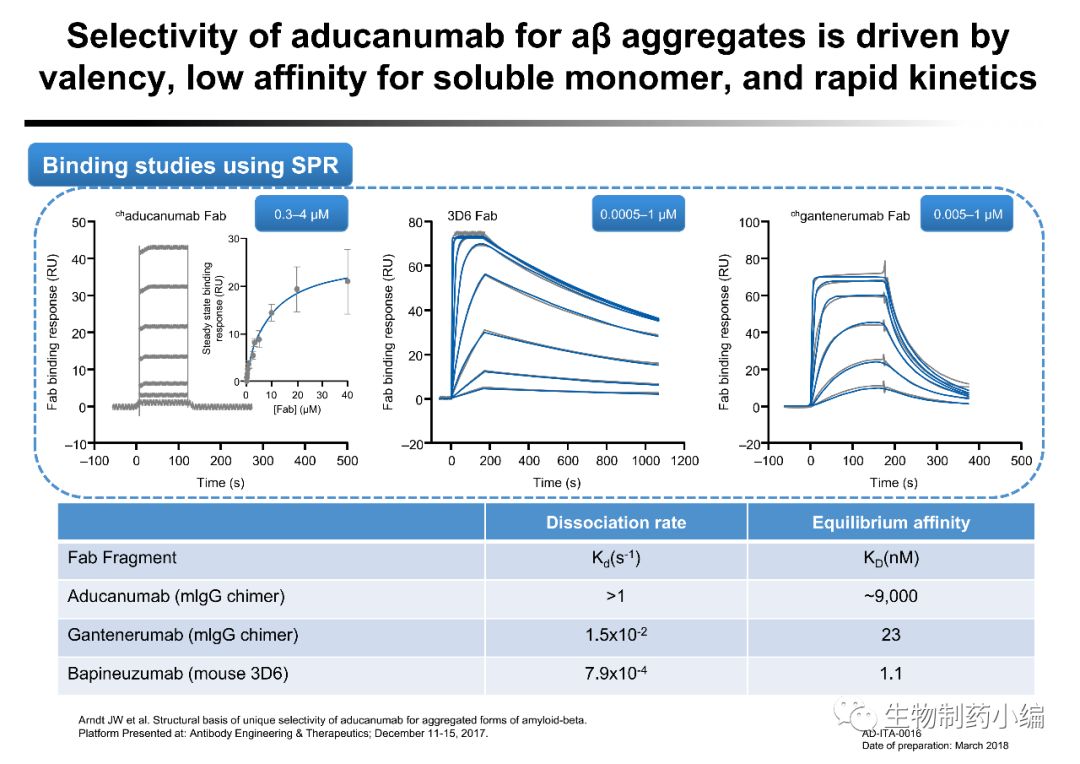
▲
Aducanumab相对于其他抗体,对于Aβ单体亲和力更低
(来源于Biogen官网)
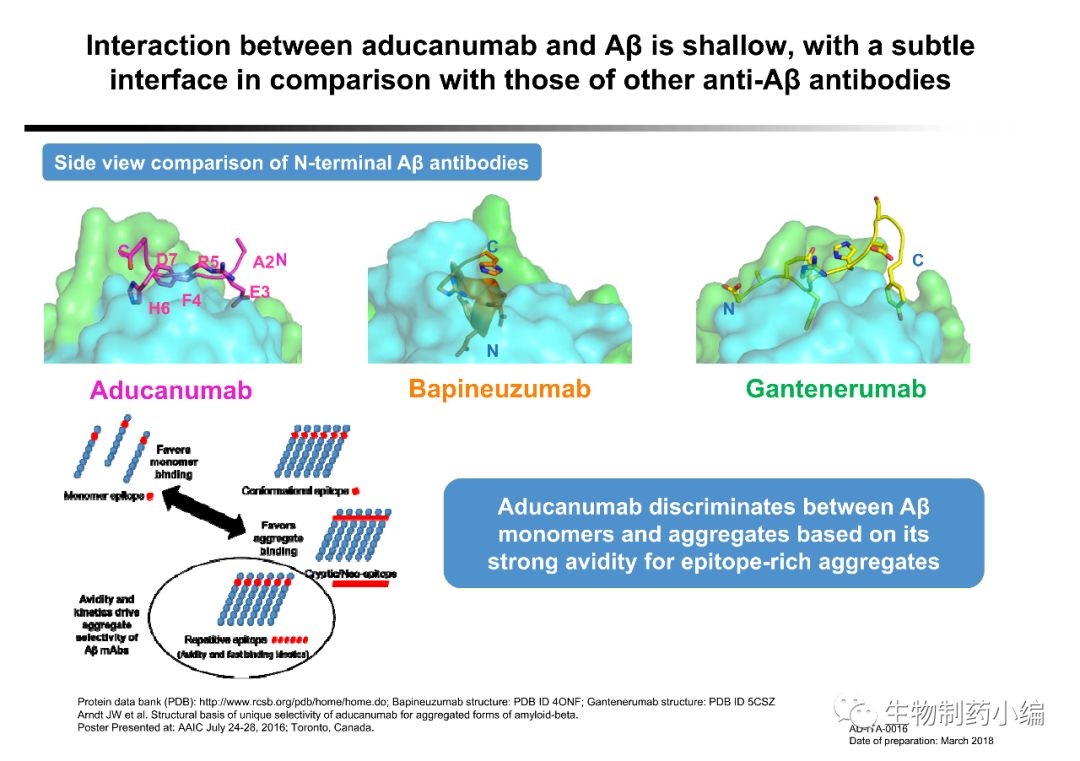
▲
Aducanumab基于价键特性,对于抗原决定簇富集的
Aβ聚体结合能力更强
(来源于Biogen官网)
最后,不得不提一下本文前面提到的明星药物BAN2401,该药物是目前结合Aβ氨基酸位点最少的抗体药物,可能由于此特性在对于原纤维状的Aβ清除作用更强,算得上是
Aducanumab的加强版
。
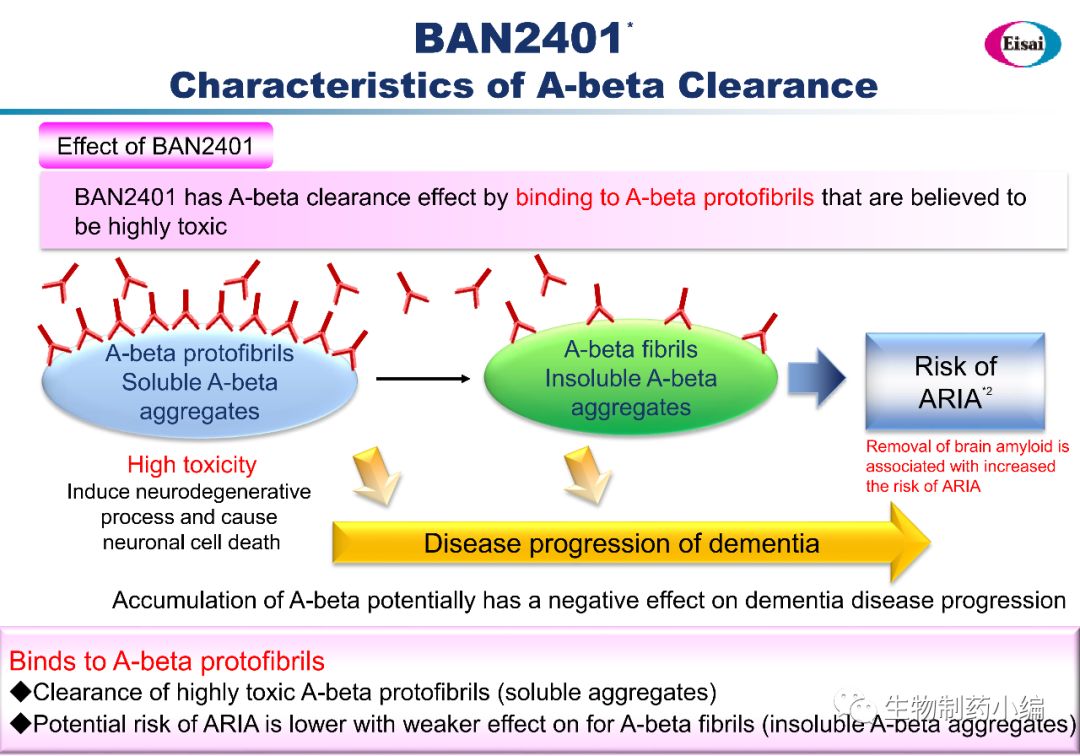
▲
BAN2401基于更少的氨基酸结合位点,对于
原纤维状的Aβ
结合能力更强
(来源于
Eisai
官网)
半年多前,这款充满潜力的新药却在一项名为Study 201的临床试验中败下阵来。这项研究招募了856名患者,他们均因阿兹海默病而出现了认知能力上的缺陷。研究人员们期待BAN2401能够改善他们的病情,但初步的临床结果却事与愿违——在12个月的节点上,该试验未能在临床终点上达到统计学意义上的显著性,因此曾被认为是阿兹海默病新药研发道路上的又一场失利。
但卫材与百健不这么看。尽管在12个月的节点上遭遇失利,但他们依旧决定继续观察半年,在18个月的节点上再做一次综合的评估。
最新的试验数据表明,在18个月时,与对照组相比,最高剂量的实验组患者(每公斤体重接受10mg的BAN2401治疗,每两周治疗1次)彰显出了疾病进展上的显著缓解。而PET分析结果也表明,患者大脑中的淀粉样蛋白水平有显著下降。
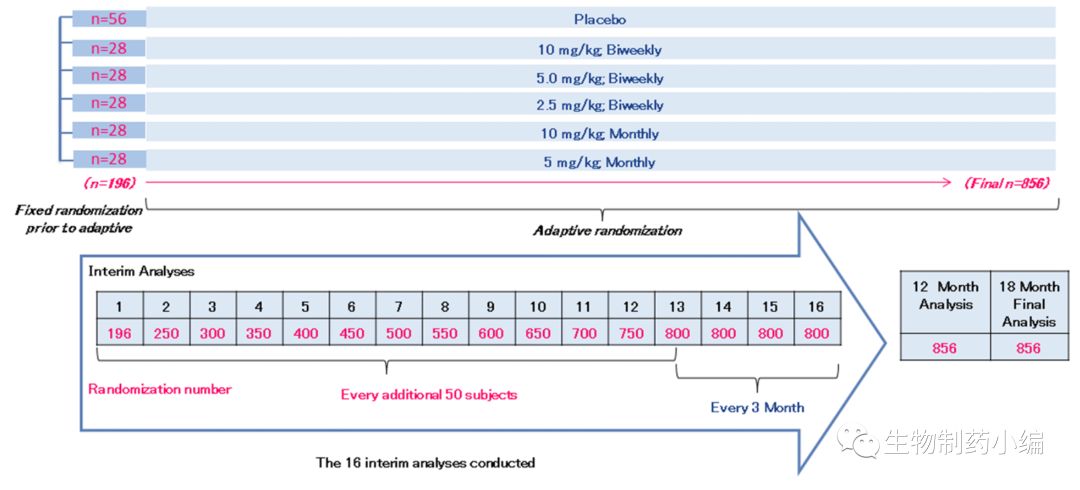 ▲
BAN2401的
Study 201临床试验设计
(来源于
Eisai
官网)
▲
BAN2401的
Study 201临床试验设计
(来源于
Eisai
官网)
对于阿尔兹海默症,或许是目前撰写评论文章最多的领域之一。特别是基于其曲折的研发道路,居高不下的研发失败率,很多文章可以写得很宏伟。此外最近几天《我不是药神》影片的热播,让更多人从患者和药企两端体味到了药物研发的迫切和艰难。
然而站在“胜者为王,败者为寇
”
的药物开发现实面前,没有同情,我们当然不认为BAN2401一个药物可以改变整个
阿尔兹海默症Aβ假说的研发格局,更多地只能算是一种
续命。因为从某种意义上讲,多一种疾病治疗途径的存在,跟世界多一个超级英雄或许是同一个道理。
世界总需要光,你说是吗?
文末彩蛋
“
2017生物制药小编精选文章汇编
”限量印刷150本,最后数本留给线上同仁,每本200元包邮,后台回复“汇编+微信号
”
,将有工作人员联系您,机会有限,先到先得。
欢迎加入小编团队成为小编一员
请加小编微信号:wuwenjun7237
如有技术解读、行业洞见愿意分享
欢迎投稿到小编邮箱:
[email protected]












