
蛋白质和多肽药物以其高亲和力、高特异性和低毒性的特点,彻底改变了各种慢性和急性疾病的治疗格局。然而,大多数获批的治疗性蛋白质和多肽半衰期短,且只能通过持续的皮下注射给药。例如,常规胰岛素(INS)的作用时间通常在4到8小时之间,这使得重症糖尿病患者每天需要注射2到4次INS来有效管理血糖水平(BGLs)。不幸的是,每日重复这些注射会导致身体疼痛和心理压力,这对于慢性糖尿病患者来说可能是难以忍受的。特别是,非标准的药物管理可能会导致血糖控制不佳,甚至增加心血管疾病的风险。为了解决传统INS的短暂效果,研究人员已尝试对INS进行结构修饰,以延长药物的作用时间。INS glargine和INS degludec因其长效基础INS供应和平稳的时间-作用特征而受到认可,成功将INS的作用时间延长至36小时以上,并降低了低血糖的风险。然而,尽管有所有这些进展,但对于患者来说,与持续注射相关的疼痛问题仍未得到解决。因此,开发具有长效基础INS释放动力学和非侵入性、高生物利用度的INS递送系统至关重要。
来自武汉大学中南医院的田间等团队
报告了一种简单却高效的口服制剂,该制剂基于叶酸偶联的Zr-MOF纳米颗粒,能够选择性地在糖尿病患者体内实现胰岛素的持续释放,并具有极高的生物利用度。这种耐酸的Zr-MOF纳米载体能够在恶劣的胃肠道环境中保护胰岛素免受酸和酶的降解。通过利用功能性叶酸分子占据Zr-MOF金属簇中的空缺配位点,MOF纳米载体不仅能实现特异性的肠道转运,还能在体内高度控制胰岛素的释放行为,降低低血糖风险,避免快速崩解和突发式药物释放。基于MOF的口服蛋白/肽类药物递送纳米系统的延长药物作用时间和提高疗效,为长期有效的血糖管理提供了转化机会。相关工作以题为
“Efficient oral insulin delivery with sustained release by folate-conjugated metal-organic framework nanoparticles”
的文章发表在2025年01月14日的期刊
《Matter》
。

【基于MOF的缓释纳米系统制备与表征】
PCN-777纳米粒(NPs)、叶酸(FA)偶联的PCN-777 NPs(F-P NPs)、胰岛素(INS)封装的PCN-777 NPs(I@P NPs)以及INS封装的F-P NPs(I@F-P NPs)的制备过程如图1A所示。在以往的报道中,PCN-777的粒径通常大于500纳米,这不利于其穿越肠道屏障。因此,通过优化的溶剂热法合成了粒径分布约为220纳米的PCN-777 NPs。透射电子显微镜(TEM)图像和流体力学直径结果显示,基于PCN-777的纳米系统由均匀的规则八面体组成(图1B和1C)。由于FA在室温下不溶于水,且考虑到蛋白质在有机溶剂中的不稳定性,在逐步合成过程中先在PCN-777上安装FA后再封装INS。经过FA修饰和INS封装后,纳米粒的颜色变为黄色,表面从光滑变为粗糙,粒径略有增加。基于PCN-777的纳米系统在连续的偶联和封装过程中也表现出不可忽视的zeta电位变化,最初由于FA的负电荷性质从+33 mV降至+30 mV,随后在INS负载后增至+36 mV(图1C)。根据zeta电位的变化,我们推测INS以最小的静电相互作用与MOF内部结合。此外,考虑到PCN-777纳米载体具有显著的疏水性内表面,INS的封装主要是通过疏水相互作用促进的。
为了进一步确认FA和罗丹明异硫氰酸酯(RITC)标记的INS(R-I)在PCN-777 NPs中的修饰和固定情况,本文接下来进行了荧光光谱和紫外可见(UV-vis)光谱测量。F-P NPs的荧光光谱显示了FA在约450纳米处的特征吸收峰(图1D),表明FA的成功偶联。同样地,在RITC-INS@FA-PCN-777(R-I@F-P NPs)中,R-I的特征发射峰位于约580纳米处,而其在UV-vis光谱中约560纳米处的吸收峰提供了INS封装的预期证据(图1E)。值得注意的是,与R-I@P NP和R-I@F-P NP组相比,R-I的吸收峰红移了4-5纳米。这是由于R-I分子在PCN-777 NPs中的聚集所致,进一步证明了大量的INS被包裹在PCN-777 NPs内部而非分散在其表面。I@P NPs和I@F-P NPs的粉末X射线衍射(PXRD)图谱与PCN-777 NPs基本相同(图1F),表明PCN-777 NPs在FA修饰和INS封装过程中保持了良好的结晶度。能谱(EDS)元素映射分析显示,经过FA修饰的PCN-777不含硫元素。
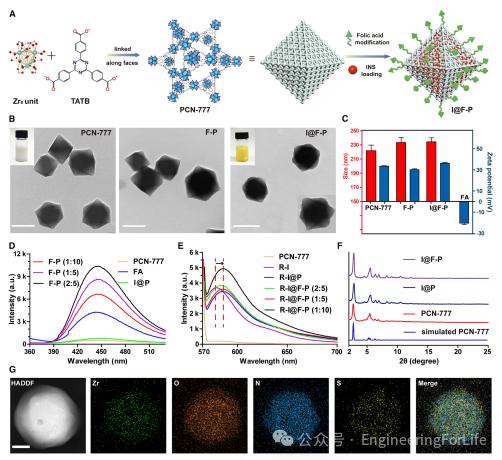
图1 基于PCN-777纳米系统的制备及表征
【I@F-P NPs的持续且受控的药物释放动力学】
接下来,本文测试了基于PCN-777的纳米系统在不同生理条件下的稳定性和释放曲线(图2D)。可以观察到,在模拟胃液(FaSSGF)和模拟肠液(FaSSIF)环境中,I@P NP组在8小时内释放的INS不到10%(48小时内小于35%),而I@P NPs在PBS中持续且缓慢地释放INS,48小时内累计释放量达到93%。值得注意的是,48小时内,I@F-P NPs中INS的累计释放量明显低于I@P NP组,这归功于FA改性的PCN-777具有更高的PBS稳定性。为了进一步研究这一现象,探索了不同FA/PCN-777投料比下I@F-P NPs在含磷酸盐条件下的释放曲线。如图2D所示,在PBS环境中,随着FA修饰量的增加,I@F-P NPs中INS的累计释放量显著减少,当FA与PCN-777的投料比增加到2:5时,I@F-P NPs在48小时内的INS累计释放量降低到67%。结果发现,由于FA和PCN-777之间的空间位阻极大地阻碍了磷酸盐对Zr6簇的攻击,因此通过增加FA修饰量可以显著减轻磷酸盐触发的释放,从而创建了一个相当特定的过程,导致PCN-777分解时间的延迟。

图2 FA修饰的PCN-777纳米系统的体外释放性能
【I@F-P纳米粒的生物相容性分析】
安全性是慢性病长期用药的先决条件。本文首先使用急性溶血试验评估了基于PCN-777的纳米系统在体外血液中的安全性。当给药浓度为500 μg/mL时,溶血率为4.1%(图2F),这表明基于PCN-777的纳米系统对细胞膜和细胞内蛋白的损伤很小。在细胞水平上,本文进行了MTT(3-[4,5-二甲基噻唑-2-基]-2,5-二苯基溴化四氮唑)试验和活/死细胞成像试验。如图3A所示,基于PCN-777的纳米系统在不同细胞系中表现出低细胞毒性,即使在500 μg/mL的给药浓度下,细胞存活率也高于85%,这与活/死细胞染色结果一致(图3B)。在健康和糖尿病动物模型水平上,本文对基于PCN-777的纳米系统的长期生物安全性进行了全面评估,包括对血液参数、生化指标、促炎细胞因子和组织形态变化进行彻底检查,以评估其连续口服给药后的潜在影响。结果表明,除了尿酸(UA)外,在常规血液分析、生化指标或血清促炎细胞因子方面,基于PCN-777的纳米系统组与对照组之间没有显著差异,即使在治疗1个月后也是如此(图3C和3D)。尽管不同组之间UA水平存在显著差异,但小鼠的UA水平具有相当大的变异性,从0.1到760 μM不等,所有这些值均在文献报道的正常生理范围内。此外,主要器官和肠道结构完整,与对照组相比没有显著差异,从而证实了该纳米系统具有优异的生物相容性,以及对肝脏、肾脏和心脏功能没有不良影响。
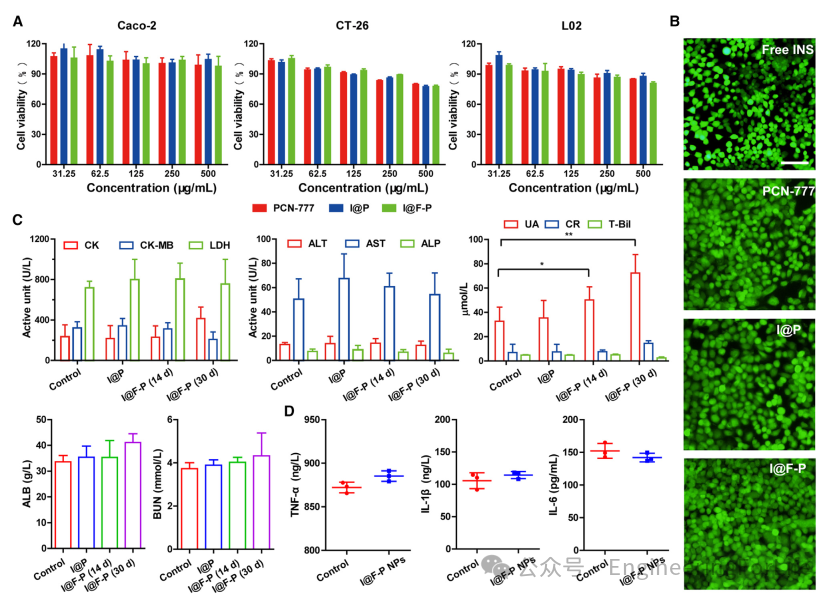
图3 基于PCN-777纳米系统的生物相容性
【I@F-P NPs的PCFT介导的内吞作用研究】
高表达PCFT的人结肠腺癌(Caco-2)细胞系作为主要的药物转运细胞模型,其可用于预测I@F-P NPs的肠道吸收效率。根据文献报道,杨梅素可以抑制PCFT的表达。因此,本文通过蛋白质印迹分析(western blot analysis)评估了杨梅素干预后Caco-2细胞中PCFT表达的变化。结果表明,杨梅素显著降低了这些细胞中的PCFT表达。因此,在后续实验中,将通过杨梅素抑制PCFT表达的Caco-2细胞作为对照组,以研究PCFT表达水平对I@F-P NPs内吞作用的影响。基于PCN-777的纳米粒子在Caco-2细胞单层中的定性和定量摄取通过激光共聚焦荧光显微镜(CLSM)和流式细胞仪分析进行可视化(图4A)。与其他组相比,I@F-P NPs表现出增加且具有时间依赖性的细胞内化。此外,从z轴的红色荧光分布来看(图4A和4B),I@F-P NPs在Caco-2细胞单层中的转运深度更靠近基底侧。根据流式细胞仪获得的定量结果,I@F-P NPs的细胞摄取量分别是游离INS和I@P NPs组的9.9倍和2.1倍。值得注意的是,在PCFT表达受抑的细胞中,I@F-P NPs的内化与I@P NP组相当,并且随着FA密度的增加,I@F-P NPs的内化逐渐增强,这证实了I@P NPs组的细胞内化是由PCFT途径介导的。
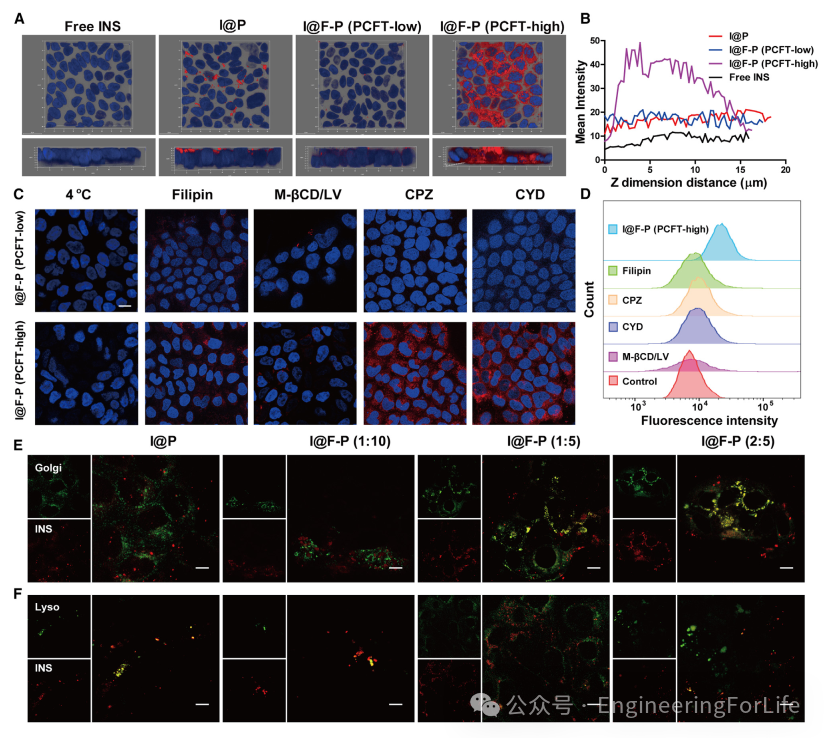
图4 I@F-P NPs通过PCFT介导的选择性内吞作用
为了验证I@P NPs是否能够通过高尔基体途径有效地进行胞吐作用,本文随后研究了基于PCN-777的纳米系统在Caco-2细胞单层中的跨细胞渗透性。首先,本文检测了在基于PCN-777的纳米系统处理期间,Caco-2细胞单层的跨上皮电阻(TEER)值。与对照组相比,TEER没有显著降低,这确认了紧密连接的完整性(图5A)。在高PCFT表达的细胞中,I@F-P NPs在48小时内的INS累计渗透量达到了62%,与低PCFT表达细胞中的I@P NPs、游离INS和I@F-P NPs相比,分别是它们的2.1倍、2.7倍和6.8倍(图5B)。正如补充图S22B所示,INS制剂在细胞顶端和基底层的荧光分布与上述结果一致。I@F-P NPs在高PCFT表达的Caco-2单层中的表观渗透系数(Papp)为20.6 ×
10
−7
cm/s(图5C),这表明在高表达组中,I@F-P NPs的渗透性显著提高。接下来,在24小时时取基底侧的培养基进行离心处理,并对沉淀物进行TEM分析。结果表明:在PCFT高表达组中,I@F-P NPs保持了完整的形态结构,而在PCFT低表达组中,则无法观察到I@F-P NPs的八角形结构,这可能是由于它们通过网格蛋白介导的内吞作用在溶酶体中被破坏所致。随后,本文根据文献报道计算了不同制剂在Caco-2细胞单层中的INS降解率。如图5D所示,在孵育48小时后,游离INS组中摄入的INS几乎完全降解,而I@P NPs和I@F-P NPs组则显著抑制了PCFT高表达和低表达细胞中INS的降解速率。与I@P NPs组相比,FA略微阻碍了溶酶体降解,并将PCFT低表达细胞中的降解率从60%降低到48%。相反,在PCFT高表达细胞中,只有约15%的INS发生降解,这不仅归因于F-P NPs的保护作用,还归因于I@F-P NPs通过高尔基体介导的途径发生内化,避免了被溶酶体吞噬,从而减少了INS的降解。
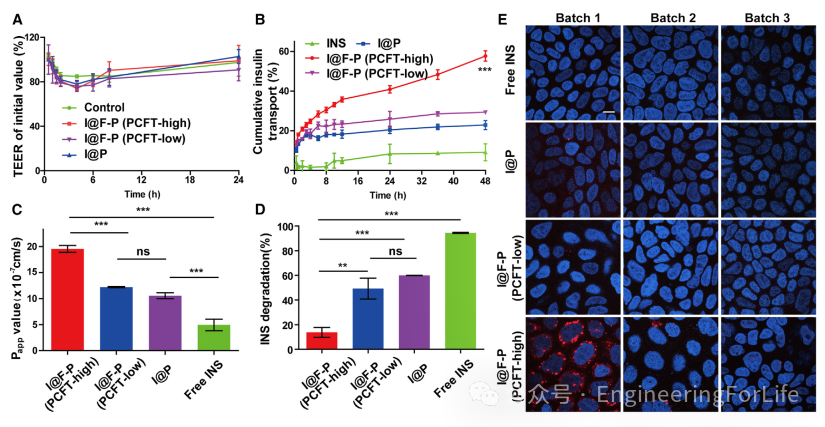
图5 在高表达和低表达PCFT的Caco-2细胞单层模型中,I@F-P NPs的跨膜运输
【体内生物分布和肠道吸收】
本文利用 TEM、Maestro 体内成像系统和 CLSM 详细绘制了基于 PCN-777 的纳米系统进入和离开生物体的时空分布图,直观地研究了其跨过上皮层的潜在途径和分布情况。在灌胃 4 小时后处死大鼠,取小肠进行 TEM 成像(图 6B)。结果表明,只有 I@F-P NPs 大量定位于上皮细胞中,这表明 PCFT 介导的内吞作用增强了 I@F-P NPs 进入肠道上皮的渗透效率。接下来,在 48 小时内获取了正常小鼠和糖尿病小鼠体内游离 INS、I@P NPs 和 I@F-P NPs 分布的体内图像。结果显示,在 I@F-P NPs 治疗的糖尿病小鼠中,高达 48 小时的强烈且持续的荧光信号被观察到,而其他组的荧光信号较弱,并且在 48 小时内持续减弱(图 6C),这为 I@F-P NPs 在糖尿病小鼠体内的高效肠道转运和长期功效提供了确凿证据。值得注意的是,正常小鼠中观察到的 I@F-P NPs 荧光信号与 I@P NPs 组几乎相同,这表明正常小鼠中的 PCFT 表达水平相对较低,从而导致药物吸收效果不佳。
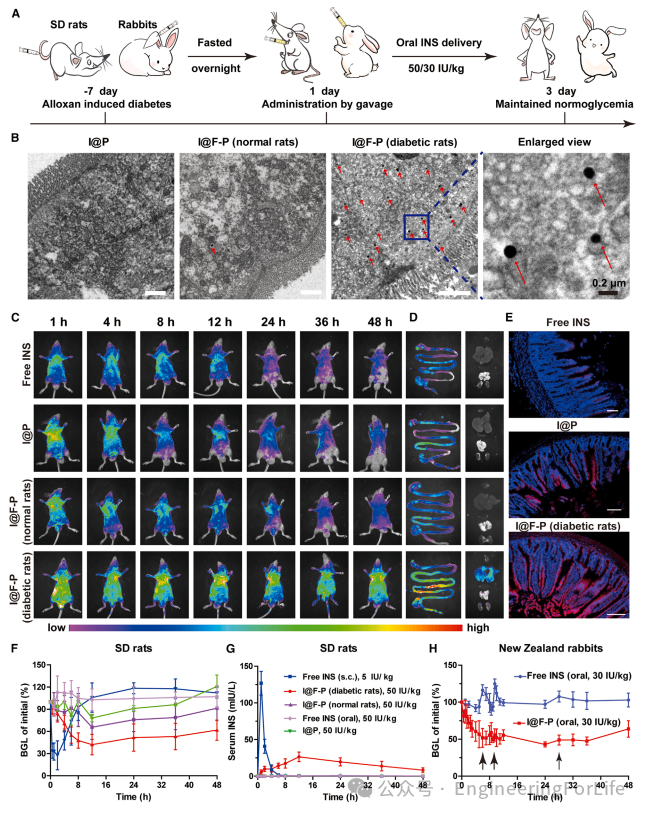
图6 FA修饰的PCN-777纳米系统在动物体内增强和持久的降糖效果验证
【总结与展望】
口服蛋白/肽类药物递送系统由于其为患者带来潜在巨大益处而受到全球关注。然而,其临床转化因肠道渗透性差、酸不稳定以及蛋白/肽类药物半衰期短等挑战而受阻。在此,我们报道了一种简单、高效且具有缓释功能的口服胰岛素递送系统,该系统基于叶酸(FA)偶联的耐酸金属有机框架(MOF)纳米颗粒,具有高药物负载能力。MOF(PCN-777)纳米颗粒上的FA偶联不仅通过上调肠道FA转运蛋白介导的内吞作用选择性地提高了糖尿病动物的肠道转运效率,而且还调节了PCN-777在富含磷酸盐的血流环境中的分解,以在狭窄的治疗范围内维持长效基础胰岛素的释放动力学。在糖尿病动物模型中,FA-PCN-777口服胰岛素递送纳米系统显示出长达48小时的平稳降糖效果,生物利用度高达35.5%,这代表了一种潜在长效口服制剂,具有降低低血糖风险的优势。
参考资料:
https://doi.org/10.1016/j.matt.2024.101948
来源:
EngineeringForLife
声明:仅代表作者个人观点,用于研究用途,作者水平有限,如有不科学之处,请在下方留言指正!






