小编见过组织活检、液体活检,但还没听说过“气体活检”。2017年7月11日JTO 在线发表了来自以色列学者Nir Peled研究,利用纳米矩阵感受器对肺可疑结节患者进行呼气分析,鉴别肺良恶性结节、EGFR突变准确性较高,均在80%以上。目前“气体活检”在肺癌良恶性判断、早期发现、组织学类型判断及EGFR是否突变具有不错的前景?
新诊断肺癌中局限期仅占15%,尽管美国国家肺癌筛查试验(NLST)证明低剂量CT可降低20%肺癌死亡率,但假阳性率高达96%。CT发现肺结节可能需要有创检查,病人对癌症及化疗毒性充满担忧。需要生物标志物来鉴别肺结节良恶性,且最好是无创方法。呼出的挥发性有机化合物(VOCs)是发现肺癌潜在的新型临床检测手段。
VOCs可来自机体细胞生化反应,或吸入、摄入或通过皮肤吸收的物质。VOCs与氧化应激、细胞色素P450、碳水化合物及脂肪代谢等生化反应有关。有机化合物难以溶于血液,通过肺泡进行气体交换。呼气样本中存在3000多种不同的有机化合物,但浓度较低(万亿分之一到十亿分之一)。使用可视化矩阵感受器,从其他肺部疾病中鉴别NSCLC的敏感性73.3%、特异性72.4%。Molina教授利用5种不同代谢产物,从健康人群和高危人群中鉴别肺癌的敏感性77.9%、特异性67.5%。
目前呼气分析面临挑战有鉴别同一器官不同来源肿瘤、区分癌症不同分期。目前已有呼气分析可准确的区分肺良恶性结节、肺鳞癌和腺癌、早期和晚期肺癌。但是该技术能否用于基因检测还没有报道。
该项目在以色列希巴医学中心进行,纳入可疑肺结节患者。良性肺结节规定为病理确诊或影像学随访2年稳定。在治疗前收集呼气样本。为避免影响,要求采集样本时禁食1小时以上、饮酒12小时以上、吸烟半小时以上,使用专门呼吸装置呼吸3分钟后采集呼气样本。
患者分为良性结节与早期肺癌、EGFR突变和无突变肺癌、重度吸烟和轻度/无吸烟。使用纳米材料为基础矩阵感受器进行呼气分析。
1.2012年1月至2014年5月,共纳入患者119例,其中,良性结节30例,肺癌89例(早期肺癌16例、晚期73例)。较肺癌患者,良性肺结节年龄更小、吸烟少、肿瘤体积小。30例良性(或可能良性)中肉芽肿3例、炎症1例、活检无特异3例、未活检23例。89例肺癌中腺癌73例、鳞癌9例、SCLC7例(均为广泛期)。
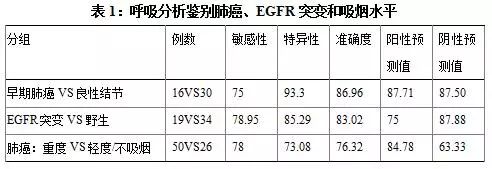
2.呼吸分析可较好区分早期肺癌和良性结节,感受器的准确度为87%,敏感性相对低为75%,特异性较高为93%,阳性预测值(PPV)和阴性预测值(NPV)分别为87.7%和87.5%。EGFR突变与野生型患者19例和34例,使用五种不同感受器,纳米矩阵技术可区分肺癌EGFR是否突变,准确度83%,敏感性79%,特异性85%,PPV和NPV分别为75%和88%。在肺癌患者中,感受器可区分重度吸烟(≥30包年)和轻度/不吸烟,准确度76.3%,敏感性78%,特异性73%。具体数据见表1。
呼吸分析可鉴别肺癌EGFR是否突变及肺良恶性结节。在缺乏足够样本用于突变检测时,呼吸分析EGFR突变可考虑用于指导治疗。
使用高度敏感的纳米矩阵感受器及应用强大统计工具鉴别函数分析,建立起不同疾病的“呼吸印记”。该技术判断肺癌患者EGFR突变准确性可达83%,研究者使用含40个感受器的设备来保证在临床中可准确发现EGFR突变。该研究鉴别肺癌和肺良性结节与既往研究类似。纳米矩阵感受器还可以鉴别肺腺癌和肺鳞癌,甚至早期和晚期肺癌。本研究从肺良性结节分辨早期肺癌敏感性、特异性和准确性分别为75%, 93% 和 87%,阳性和阴性预测值较高(约88%),提示该检测高效性和实用性。
这是第一项在临床中使用呼气分析鉴别EGFR突变研究,可对EGFR检测阴性患者进行组织检测。在组织学样本不足时,呼吸检测发现EGFR突变可用于指导治疗。呼吸分析可鉴别肺癌患者吸烟程度,区分重度吸烟与轻度/不吸烟。
该研究局限性:第一样本量有限,特别是早期肺癌、EGFR突变患者数较少;第二,良性结节定义为影像学随诊2年稳定替代组织学活检,第三,吸烟史资料可能存在回顾性偏移。期待更大样本研究提供更准确结果。使用“呼气印记”检测呼出的挥发性有机化合物可作为发现肺癌标志物,且携带方便、不昂贵且检测迅速。
Shlomi D,et.al.Detection of Lung Cancer and EGFR Mutation by Electronic Nose System. J Thorac Oncol. 2017 Jul 11.
19个肿瘤相关临床试验招募患者
点击下方图片即可查看详情















