作者 l
放翁是水货
编辑
l
细胞房间
Genentech的乳腺癌治疗研究获得积极进展
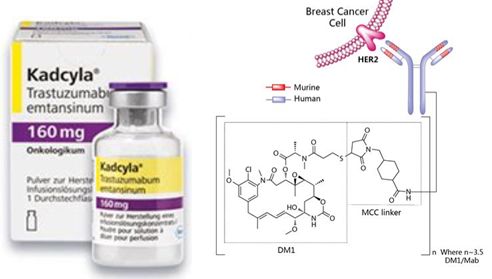
10月15日,美国,基因泰克今日宣布治疗乳腺癌的III期临床KATHERINE研究达到了主要终点。KATHERINE研究是一项国际多中心、双臂、随机、开放标签的III期临床研究,其评估了Kadcyla和Herceptin作为早期乳腺癌术前辅助治疗的有效性和安全性。这项研究的主要终点是疾病复发或患者死亡风险,在这项研究中,其被定义为从随机化到浸润性乳腺癌复发或患者死亡的时间,次要终点包括无进展生存周期和总体生存率。初步的数据分析已经证实Kadcyla(
Ado-Trastuzumab emtansine
)作为术前辅助治疗,相比于Herceptin(T
rastuzumab
)的术后辅助治疗,显著降低了HER2阳性早期乳腺癌患者的疾病复发或死亡风险,完整的结果将于今年12月在全球乳腺癌专题研讨会上公布。
Kadcyla是一种抗体药物偶联物,能够特异性靶向HER2阳性癌细胞并增强化疗疗效,目前该药是唯一被批准用于治疗HER2阳性转移性乳腺癌的ADC药物。
Satralizumab治疗视神经脊髓炎的临床研究达到主要终点
10月15日,日本,Chugai制药今日在2018年欧洲多发性硬化治疗和研究大会上公布了Satralizumab治疗视神经脊髓炎(
NMOSD
)的最新研究结果,其中Satralizumab是一种用于人源化抗IL-6受体的单克隆抗体。视神经脊髓炎是一种罕见的中枢神经系统持续衰弱和损伤的自身免疫性疾病,其特征是视神经和脊髓神经发生炎性病变。疾病的反复发作导致累积性的神经损伤,并最终诱发视力障碍、运动障碍,显著降低患者的生活质量。
SAkuraSky研究是一项III期多中心、随机、双盲、安慰剂对照研究,旨在评估在NMOSD患者标准疗法中加入Satralizumab治疗的有效性和安全性,主要终点是疾病复发的间隔时间,次要重点包括患者视力评分等。SAkuraSky研究的结果显示:在免疫抑制治疗的基础上,Satralizumab能够显著降低62%的复发风险 ,48周和96周的无复发比例分别为88.9%和77.6%。在大约2年的平均治疗期间,Satralizumab显示出良好的安全性。治疗组和安慰剂组患者经历严重不良事件的患者比例相似,没有观察到死亡或过敏反应事件发生。
Dupilumab在慢性鼻窦炎伴鼻息肉的两个III期试验中显示出积极的临床疗效
10月16日,美国,Sanofi对外宣布Dupilumab治疗慢性鼻窦炎的两项关键III期临床研究均达到主要和次要重点。SINUS-24和SINUS-52研究旨在评估与安慰剂相比Dupilumab在未得到充分控制的慢性鼻窦炎伴鼻息肉疾病中的有效性和安全性。目前此两项研究均达到主要终点,试验数据证实在24周治疗后,Dupilumab联合标准疗法皮质类固醇治疗,患者鼻充血/阻塞严重程度相比于安慰剂组分别改善了51%和57%,Dupilumab治疗的患者鼻息肉评分分别降低了27%和33%。这两项试验同样也达到了所有次要终点,包括对全身皮质类固醇或手术治疗的需求显著减少,嗅觉和慢性鼻窦炎症状有所改善,在一组共患哮喘的亚组患者中, Dupilumab显著改善了肺功能和哮喘控制。
慢性鼻窦炎伴鼻息肉是一种慢性呼吸道相关疾病,该疾病的持续性炎症常导致息肉阻塞鼻窦和鼻腔,引发严重充血、流鼻涕、面部疼痛或压力,并降低嗅觉和味觉。
Amgen的生物类似药AMGEVITA将在欧洲上市用于系列炎症性疾病的治疗
10月16日,美国,Amgen今天宣布Aadalimumab生物类似药AMGEVITA将于2018年10月16日开始在欧洲市场推出。AMGEVITA是第一个获得欧盟委员会批准的Adalimumab生物类似药,可用于治疗中度至重度类风湿性关节炎、银屑病关节炎、严重活动性强直性脊柱炎、严重的轴性脊柱关节炎、中度至重度慢性斑块状银屑病、中度至重度克罗恩病和中度至重度溃疡性结肠炎等,同时该药也获批用于儿童相关适应症的治疗。
CStone新药CS1001在美国获批开展临床研究
10月16日,中国,CStone制药公司今天宣布,FDA已经批准了CS1001的新药研究申请,这标志着CS1001进入了的全球化研发阶段。CS1001是CStone独立开发的一种全人源化抗PD-L1单克隆抗体,此次计划在美国开展的临床试验旨在确认CS1001在实体肿瘤患者中的合适给药剂量,以期为后续的II期研究提供数据支持。
Innovent
开启新的临床研究推进肺癌和肝癌的治疗
10月16日,中国,Innovent公司今天宣布其Sintilimab联合IBI305(B
evacizumab
生物类似药
)治疗非小细胞癌和肝癌的临床试验申请已经获得国家局的批准,信达此次推进的组合疗法旨在以评估其在非小细胞肺癌和肝细胞癌患者中的安全性和有效性。Sintilimab目前处于有限审查阶段,IBI305也在同期完成了III期临床研究,相信这一新的组合疗法有可能为肺癌和肝癌患者提供一种新的治疗策略。
Alphamab的双特异性抗体KN026获批在美国开展临床试验
10月16日,中国,Alphamab Oncology今日宣布它已经获得了美国FDA对其专有的双特异性抗体(
KN026
)的临床试验申请,预计不久之后KN026将在美国顺利开展临床研究。根据产品的研发计划,Alphamab Oncology最近将在中国启动了该药的I期临床试验。KN026是该公司专有双特异性抗体开发平台研发的能够靶向HER2两个独立表位的双特异性抗体。有数据证明KN026在亲和力、功效、安全性和药代动力学方面表现出良好的特征,其对于HER2阳性肿瘤表现出比Trastuzumab和Pertuzumab更突出的抗肿瘤活性。
ASLAN制药公司开展的特应性皮炎试验已经招募了第一位受试者接受评估
10月18日,美国,ASLAN制药公司今天宣布评估其在研新药ASLAN004作为特应性皮炎潜在治疗药物的I期临床已经有第一位受试者接受治疗。这是一项在美国、新加坡、澳大利亚等多个中心开展的I期临床研究,旨在评估ASLAN004在特异皮炎患者的药代动力学特性和潜在的合适给药剂量。ASLAN004是一种全人源化单克隆抗体,能够特异性靶向IL-13受体α1亚基,其临床前研究的数据证实该药能够稳定抑制IL-4和IL-13介导的信号转导。
Glenmark公司在今年的皮肤病年会上公布了GBR830治疗特应性皮炎的最新研究结果
10月19日,美国,Glenmark制药公司今日在皮肤病学年会上公布了GBR830治疗中度至重度特应性皮炎(AD)IIa期临床试验的详细数据。该研究招募了40名患者接受两次重复剂量的GBR830或安慰剂治疗,并在第29天和第71天评估疾病应答情况。数据显示与安慰剂相比,GBR830治疗的患者某些疾病相关生物标志物特征相对于基线显著降低。GBR830治疗的患者在第29天和第71天的湿疹面积和严重程度指数50(EASI)与安慰剂相比表现出更明显的缓解效果。在该研究中,GBR830安全且耐受良好,最常见的治疗引起的不良事件是头痛和特应性皮炎。
Rozanolixizumab治疗重症肌无力的概念验证性研究获得积极进展
10月19日,比利时,UCB今天公布了一项Rozanolixizumab治疗重症肌无力(MG)的概念验证性II期临床研究。这是一项II期随机,安慰剂对照,概念验证试验,共招募了43名MG患者,经过一个给药周期的治疗之后,患者QMG的基线校正增量为-0.7,MGC评分的基线校正增量为-1.8,基线MG-ADL评分中的校正增量为-1.4,显著优于安慰剂组的校正量。与此同时,QMG应答率为38.1%,而安慰剂组为22.7%;MGC应答率为47.6%,安慰剂组为27.3%;MG-ADL应答率为47.6%,安慰剂组为13.6%。在Rozanolixizumab治疗两个周期后,血清IgG浓度降低了56%,总IgG和抗乙酰胆碱受体抗体从基线降低了68%。基于现有的积极结果,UCB打算在2019年下半年开始对MG进行疗效确证研究,以加速Rozanolixizumab的开发工作。
Merrimack公司中止了MM-121治疗肺癌的II期SHERLOC临床研究
10月19日,美国,Merrimack公司今天宣布终止II期临床SHERLOC研究,该研究评估了MM-121联合多西紫杉醇对Herigulin阳性非小细胞肺癌患者的治疗效果。研究数据显示,在该患者群体中,与单独用紫杉醇相比,联合疗法没有改善患者无进展生存周期。
Pembrolizumab联合Axitinib治疗显著改善肾细胞癌患者的生存周期
10月19日,美国,默克公司今天宣布KEYTRUDA的III期临床KEYNOTE-426研究显示,Pembrolizumab联合Axitinib作为晚期或转移性肾细胞癌患者的临床一线治疗,能够显著提高患者的总生存率(OS)和无进展生存期(PFS)。在试验过程中,KEYTRUDA和Inlyta联合用药的安全性与先前报道的单一疗法安全性一致。
小编点评:
晚期肾细胞癌患者的5年生存率不到10%,临床迫切需要改善疾病进展的新疗法,KEYTRUDA与Inlyta联合使用的积极数据标志着抗PD-1疗法在攻克晚期肾细胞癌中迈出关键性的一步。
Innovent公司的抗CTLA-4单抗正式开启I期临床研究
10月19日,中国,Innovent公司今日宣布已经正式启动了针对晚期实体肿瘤患者的抗CTLA-4单克隆抗体(
IBI310
)的I期临床试验。该研究的Ia期阶段着重评估IBI310单一疗法在晚期恶性肿瘤患者的耐受性和安全性。在Ib期阶段则进一步评估IBI310与Sintilimab联合治疗晚期黑色素瘤患者的耐受性和安全性。
欢迎加入小编团队成为小编一员
请加小编微信号:wuwenjun7237
如有技术解读、行业洞见愿意分享
欢迎投稿到小编邮箱:
[email protected]













