俗话说,龙生九子,种种不同。细胞也一样,虽说是来自于同一细胞卵,一样的娇生惯养,但是各自的性格脾气却是大不相同。因而,在生命谢幕之际,细胞们会以不同的姿势走向最终的归宿,或优雅老死,或粗暴惨烈死去,来定格生命消逝时最后的瞬间。
其实,大多数细胞个性都是从容淡然,素来笑看人生,无畏生死。在死亡来临之时,会顾全大局,打包于无形,消匿于免疫,凋亡联自噬,回收再利用,维持体内稳态。真可谓轻轻地我走了,挥一挥衣袖,不带走一片云彩。
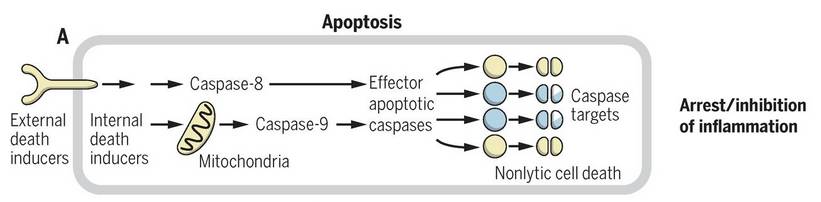
而一些脾气暴躁、个性刚烈的细胞,每每在遇到异常的物理、化学及生物因素的影响之时,这宁为玉碎不为瓦全的倔脾气即刻不受控地发作,分分钟自爆而亡,细胞的全面崩解也会立刻敲响免疫系统的警钟,瞬间就开启了炎症反应,因而也搅得机体不得安宁。
当然也有些细胞超级恋“家”(细胞外基质),且是个死宅,属于出门太久就会死的类型,换言之,就是失巢凋亡(anoikis)。举个栗子,当正常的贴壁细胞离家出走后,就会以悬浮状态四处流浪,最终因为找不到回家的路,只能郁郁而终。然而,心硬如铁、毫不恋家的肿瘤细胞却能凭着旁分泌机制抵抗凋亡,在机体内四处扎根,遍地开花。
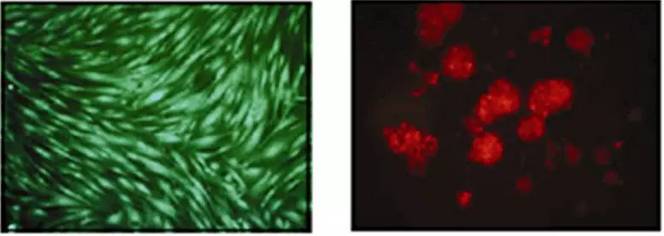
正所谓,细胞固有一死,或死于自杀,或死于他杀。当红细胞寿终正寝,会有吞噬细胞陪它走完最后一段路程。而当怀有异心的细胞与病毒、微生物沆瀣一气时,就引起免疫系统的雷霆之怒,随后则会被先锋部队(T细胞、B细胞和NK细胞)缉拿归案,认罪伏法。
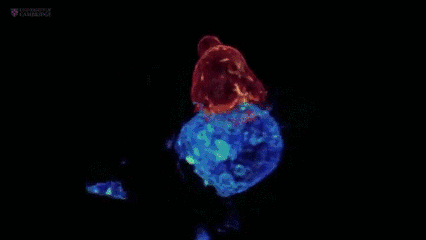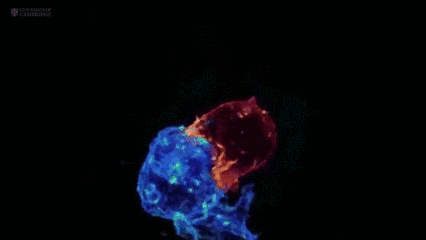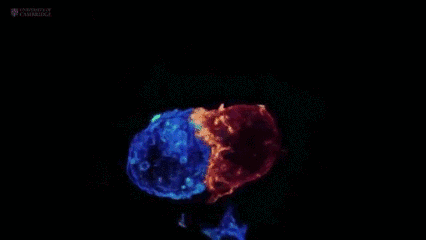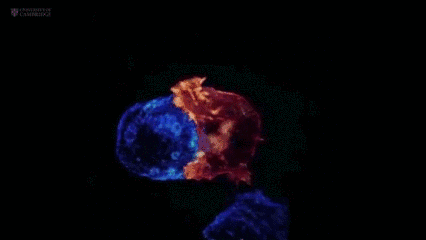
就在先锋部队缉拿“罪犯”的过程中,也会有不少白细胞壮烈牺牲。可即便如此,它依旧不忘本身职责,垂死之际会从细胞内“喷”出一长串“柱状凋亡足”(Beaded apoptopodia),其长度最大可达宿主细胞大小的8倍,进而向周围细胞发出威胁警报,进而增强免疫反应。
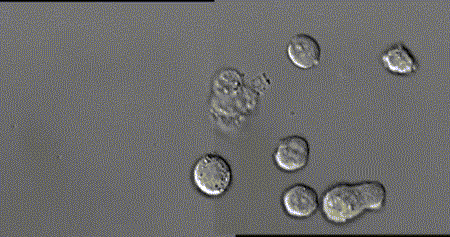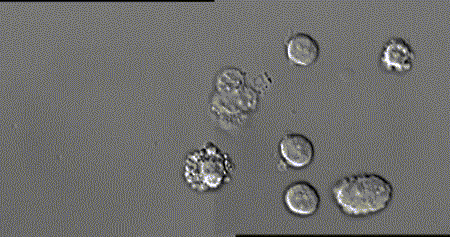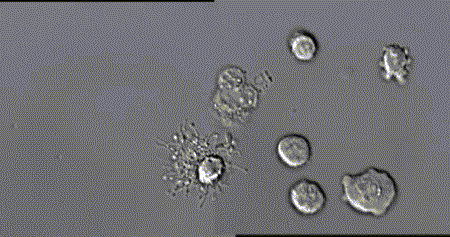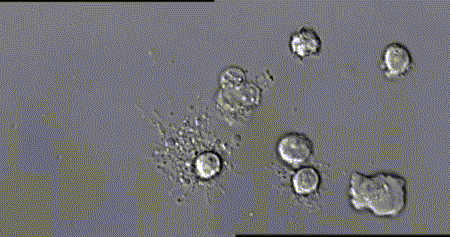
白细胞的英勇就义,加深了机体对外源病原体的厌恶之情,因而,将外来入侵者彻底消灭就成头等大事。
好在目前合体已经不是异性恋的专利了,从孙悟空贝吉塔到葫芦娃七兄弟,一经合体,战斗力瞬间飙升几个数量级。而这么拉风酷炫的事情,细胞自然也是不肯屈居人后,这不,当坏死与凋亡进行合体后,坏死性凋亡(Necroptosis)就横空出世了。

而坏死性凋亡作为脊椎动物特有的针对病原体的二重防御体系,当细胞凋亡失效时,坏死性凋亡就启动了“自动防故障机制”,大显神威地将感染病毒的细胞纷纷扑杀。
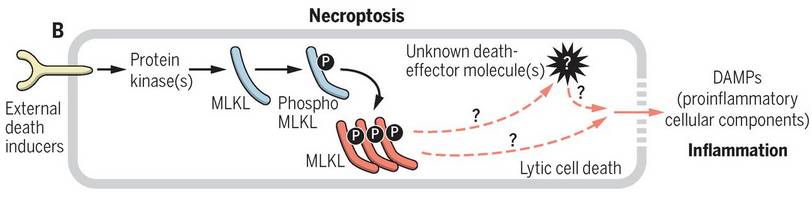
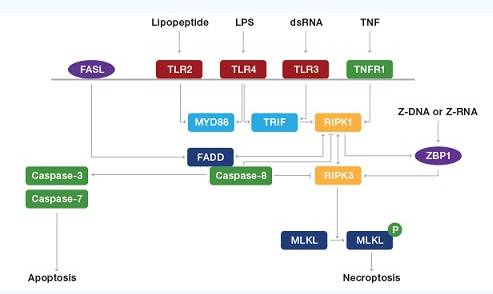
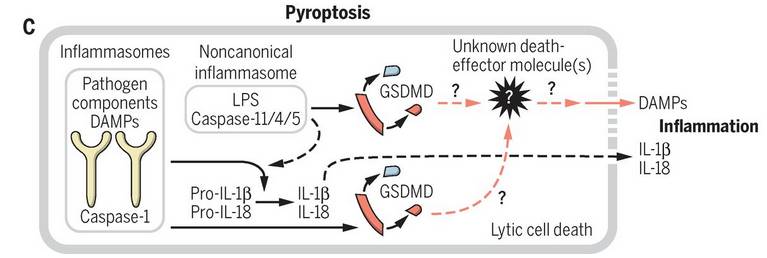
另外,细胞作死之所以能玩出新花样,细胞焦亡(Pyroptosis )也居功至伟。它将半胱天冬酶(caspase-1)和大量促炎性因子等化为熊熊火焰,一把点燃机体的天然免疫,然后被病原微生物感染的细胞也就只能被无情地“烧焦”了。
常言道,看热闹不嫌事大。肿瘤细胞也来横插一脚,为了彰显自己独一无二的特质,硬是开创一种属于它自己的细胞新死法——细胞自食(Entosis,细胞侵入性死亡),并以此来加速肿瘤细胞群体内部的淘汰过程。
通常肿瘤细胞这个浪子最是不喜像正常细胞一样被细胞外基质(extracellular matrix)所形成的蛋白质网络所束缚。因而肿瘤内部细胞在逃离基质之后,就开始肆意妄为并变得越来越无法无天了。
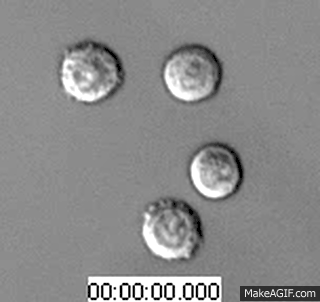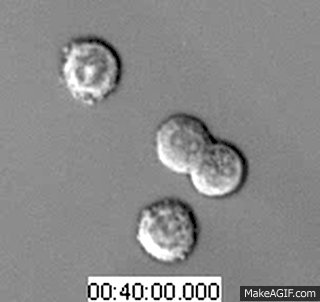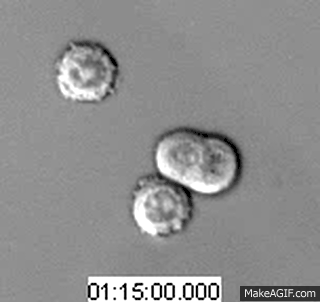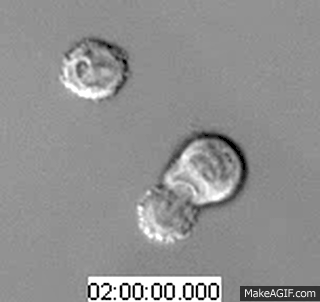
常言道,穷山恶水出刁民,这话在肿瘤内部细胞中也体现的淋漓尽致。肿瘤细胞的疯狂增殖所造成的僧多粥少局面,也使得彼此间互相残杀成为了一件常有的事情。
尽管细胞自噬(Autophagy)能暂缓细胞这份饥饿之感,但终究不能从根本上解决问题。为此,丢军保帅成为了肿瘤细胞存活的不二法宝。
最先处于葡萄糖饥饿的细胞,其能量感受AMPK信号通路很快就被活化,细胞的可塑性也发生改变。同时该细胞也会在胞内活化的Rho GTPase、ROCK蛋白的怂恿蛊惑下变得又圆又硬,随后又在钙黏着蛋白牵线搭桥下结识了活力满满的肿瘤细胞。
该细胞原以为会遇到一个雪中送炭的同类,没成想却被落井下石的同类以内化形式吞入腹内,并在溶胞体酶系的作用下一命呜呼。就这样,即便是在营养状态匮乏的情况下,凶残的肿瘤细胞依然可以靠着吞噬着孱弱同类来进行增殖存活,进而成为肿瘤内部的真正“赢家”。
如此乍一看,Entosis与细胞吞噬(Phagocytosis)就似双胞胎般完全相同。然而傲娇系肿瘤细胞明明白白告诉大家,NO! 我们与酷爱吞噬死细胞的巨噬细胞不同,我们更喜欢生吞活剥。换言之,被内化的细胞在未遇到溶胞体酶系之前,仍是处于或活着的状态,甚至还可以进行细胞分裂呢!