 投资要点
投资要点
前言
随着国内创新药政策环境逐步与欧美接轨,国内创新药估值体系将有望逐步趋同海外,实现从PEG向Pipeline转变。同时,我们对创新药的研究也在追本溯源,通过从海外创新药适应症获批、上市销售等发展历程进行全面研究。本篇报告是基于我们前期创新药系列报告的整体框架,进行更为细化而深入的探讨。
本报告亮点有三:
1、通过大量查阅相关中英文文献等资料,确保数据真实性和可靠性。
2、对贝伐珠单抗(安维汀)海外临床数据进行深入挖掘,并对国内贝伐珠单抗用于治疗转移性结直肠癌和非鳞状非小细胞肺癌的市场空间分别进行预测,并估算了每个适应症的治疗渗透率。
3、精要剖析了国内贝伐珠单抗的研发策略和方案。
此外,我们后续还将对常用的单抗靶点药物市场进行详实的研究和分析,敬请关注!
报告正文:
1、VEGF靶点简介
根据Wikipedia的定义,血管内皮生长因子(Vascular Endothelial GrowthFactor,VEGF),是细胞内刺激血管生成的信号蛋白,具备促进血管新生和再生的功能。根据VEGF分类介绍(见附注),细胞内VEGF通过结合并活化细胞表面的血管内皮生长因子受体(Vascular Endothelial GrowthFactor Receptor,VEGFR,又称酪氨酸激酶受体),最终导致血管生成。
VEGF/VEGFR靶点抗体通过特异性的结合VEGF/VEGFR,从而抑制下游信号通路,实现抑制血管生成。目前国内外已上市的VEGF/VEGFR靶点抗体药物主要有5个,其中VEGF靶点有4个。
贝伐珠单抗(Bevacizumab)是第一个针对VEGF靶点的人源化的单克隆抗体
,具备高亲和力且特异性地结合 VEGF,达到抑制肿瘤血管增生的作用。
下文以贝伐珠单抗(安维汀)为例进行重点阐述。
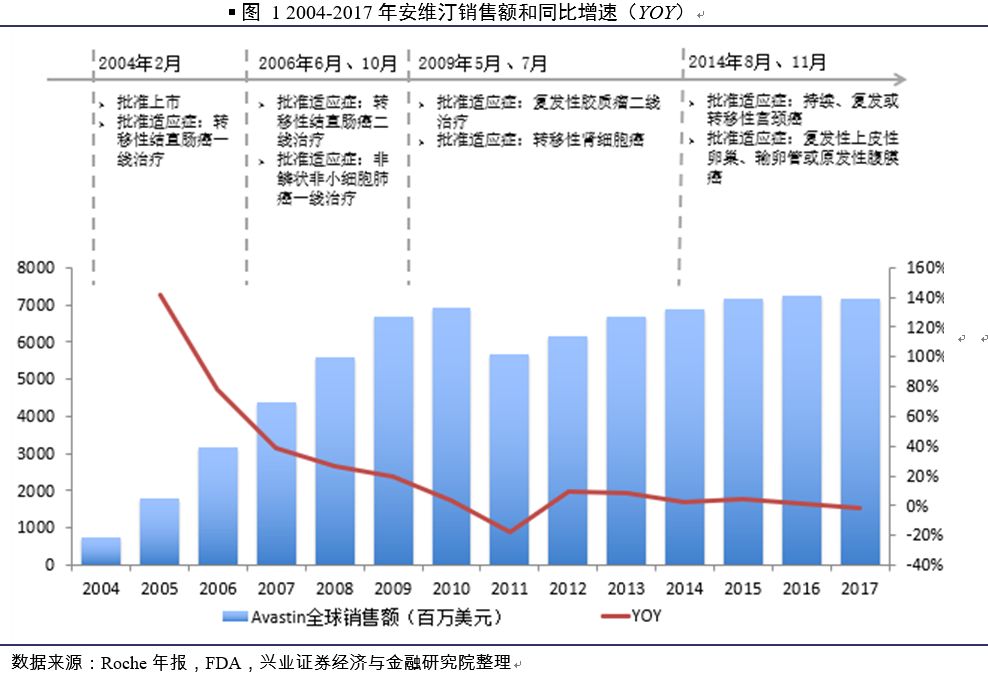
2、多个适应症驱动,安维汀全球销售规模已超过70亿美元
2.1 多个适应症获批,安维汀保持较快增长
根据美国FDA官网信息,安维汀(Avastin)是由基因泰克(罗氏的子公司)研发, 2004年2月26日,FDA批准该产品的第一个适应症,联合化疗用于转移性结直肠癌的一线治疗。随后陆续获批非鳞状非小细胞肺癌(2006年)、复发性胶质瘤(2009年)等多个适应症,直接驱动安维汀销售额实现快速增长。

目前该产品全球销售峰超过70亿美元,成为罗氏的第二大重磅产品。从销售来看,主要可以分为三个阶段:第一阶段(2004年-2006年),2004年转移性结直肠癌适应症(一线治疗)获批上市当年就达到7亿美元的规模, 2004-2006年均复合增长率(CAGR)为107%,2006年销售额超过30亿美元。第二阶段(2006年-2009年),随着非鳞状非小细胞肺癌(一线治疗)等适应症获批,安维汀持续放量, 2006-2009年CAGR为28%,2009年销售规模达到66亿美元。第三阶段(2010年-2017年),随着后续适应症持续获批,该产品维持平稳增长。
2.2
安维汀是转移性结直肠癌的一、二线用药
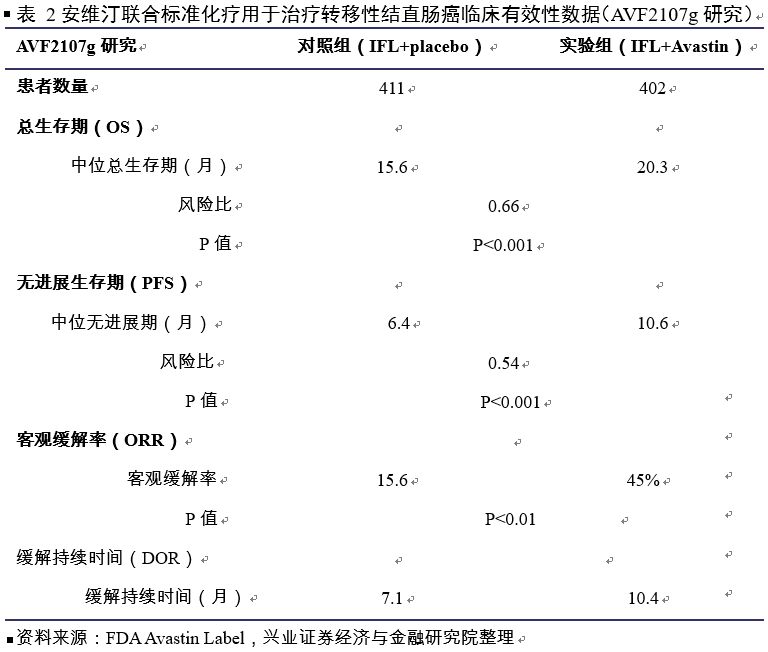
2004年,FDA
批准安维汀联合标准化疗用于转移性结直肠癌的一线治疗
。
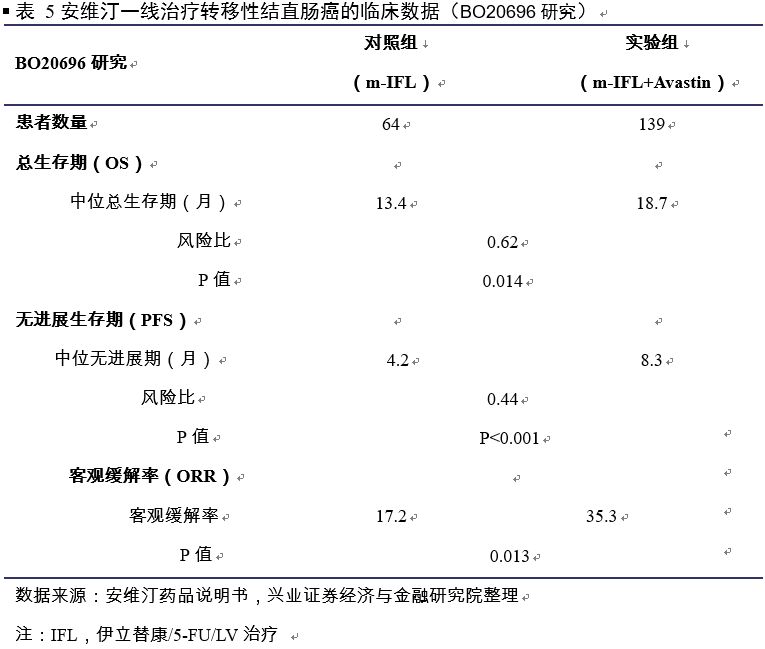
根据FDA Avastin label,基于一项双盲、活性控制的临床试验数据显示,与接受化疗药物(对照组)相比,接受安维汀联合化疗(实验组)的转移性结直肠癌患者中位总生存时间(mOS,主要终点)延长4.7个月(20.3 vs 15.6个月),显著优于对照组。中位疾病进展时间(mPFS,次要终点),实验组显著延长4.2个月(10.6 vs 6.4个月),总缓解率(ORR,次要终点)显著提高(45% vs 35%)。
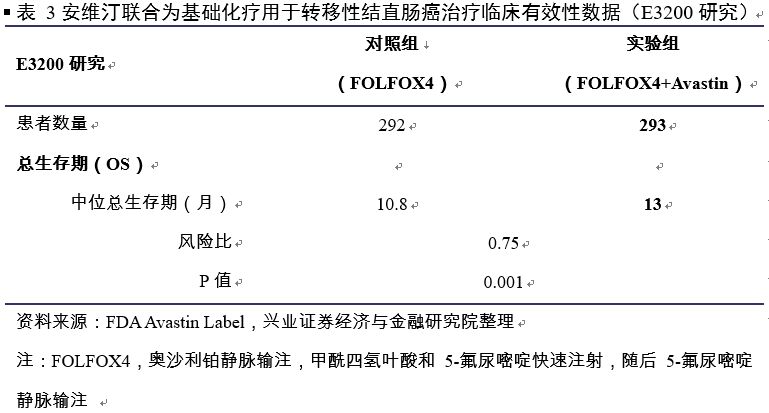
2006年,FDA批准安维汀联合5氟尿嘧啶为基础的化疗用于转移性结直肠癌的二线治疗。
主要基于E3200临床试验研究结果,接受安维汀联合化疗(实验组)的转移性结直肠癌患者中位总生存时间(mOS,主要终点)为13个月,显著优于化疗组(对照组)。
2.3
安维汀是
非鳞状非小细胞肺癌
一线用药
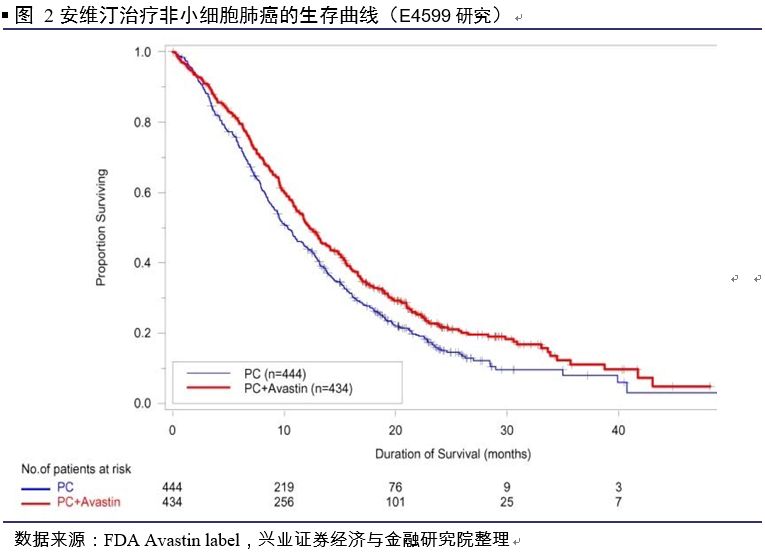
2006年, FDA批准安维汀联合化疗用于非鳞状非小细胞肺癌的一线治疗。
根据FDA Avastin label,基于一项随机、活性控制、开放标签、多中心临床试验研究(E4599)表明,与接受化疗药物(对照组)相比,接受安维汀联合化疗(实验组)的局部晚期、转移、复发非鳞状非小细胞肺癌患者中位总生存时间(mOS,主要终点)延长2个月(12.3 vs 10.3个月),显著优于对照组。同时在安全性方面,实验组的安全性特性与已知的不良事件一致。

3、
医保驱动+低渗透率,未来贝伐珠单抗国内市场空间广阔
3.1
安维汀国内市场保持快速增长,规模已超过10亿元
安维汀国内市场保持快速增长。
根据PDB国内样本医院数据显示, 2016年安维汀在国内样本医院销售额为4.3亿元,按照1:2-1:3放大测算,估计安维汀在国内销售额达12亿元左右。
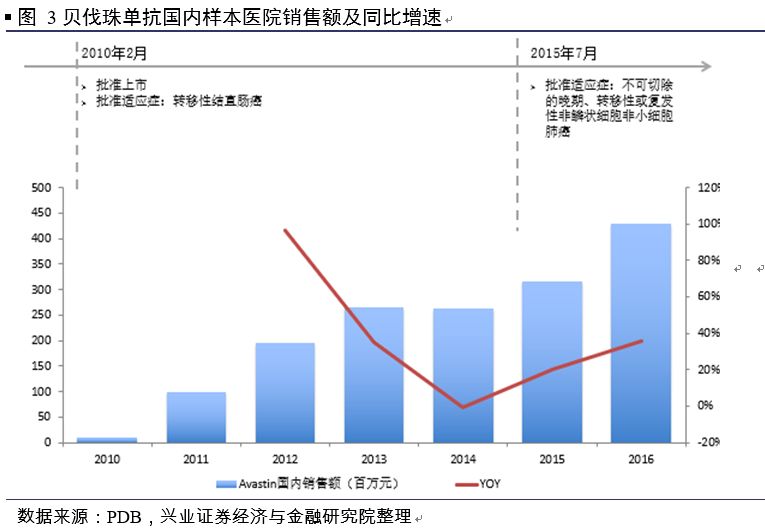
安维汀转移性结直肠癌适应症在国内2010年获批上市。
根据国内CFDA官网信息,2010年2月26日, CFDA批准安维汀上市,比美国获批时间晚6年,获批适应症为转移性结直肠癌。一项随机、开放的临床试验(BO20696研究)结果显示,实验组中一线治疗中国转移性结直肠癌患者主要终点中位无进展生存期显著受益(8.3 vs 4.2个月),且安全性评价已确定的安全性特征一致;
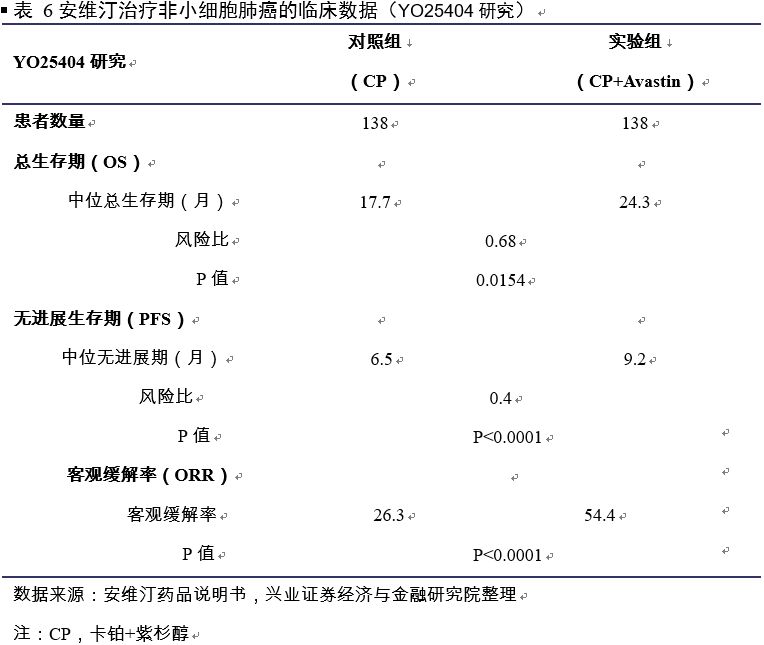
基于中国 YO25404 研究,
2015年7月,批准贝伐珠单抗用于联合卡铂与紫杉醇用于不可切除的晚期、转移性或复发性非鳞状细胞非小细胞肺癌患一线治疗。
随机、双盲、安慰剂对照、多中心 III 期临床研究(中国 YO25404 研究)表明,晚期、转移性或复发性非鳞状非小细胞肺癌主要终点中位无进展生存期显著受益(9.2 vs 6.5个月),且安全性评价已确定的安全性特征一致。
3.2
国内贝伐珠单抗用于转移性结直肠癌的潜在市场可达54亿元
结直肠癌是国内第五大肿瘤。
根据《Cancer Statistics in China, 2015》报告,2015年预计中国新增结直肠癌患者37.63万人,因结直肠癌死亡人数为19.1万人,为仅次于肺癌、胃癌、食道癌和肝癌的第五大癌症。2012年,David L. Bartlett等在Oncology Journal报道,约60%的结直肠癌患者最终会发生转移。根据2016年D. P. Modest等在Annals of Oncology文献中报道,在转移性结直肠癌患者中约50%伴有KRAS和NRAS 基因突变,5%–10%伴有BRAF V600E突变。
贝伐珠单抗联合化疗可用于转移性结直肠癌患者的一、二线治疗。
根据中国结直肠癌诊疗规范(2015 版),治疗晚期或转移性结直肠癌使用的药物:5-FU/LV、伊立替康、奥沙利铂、卡培他滨和靶向药物,包括贝伐珠单抗和西妥昔单抗(推荐用于 Ras 基因野生型患者)。
根据中国临床肿瘤学会(CSCO)结直肠癌诊疗指南(2017版)
,对于所有拟接受全身系统治疗的初始不可切除转移性结肠癌患者可根据转移灶是否有潜在根治性切除可能分为:潜在可切除组和姑息治疗组。
贝伐珠单抗联合化疗可用于RAS或BRAF突变型的转移性结直肠癌患者的一、二线治疗
。
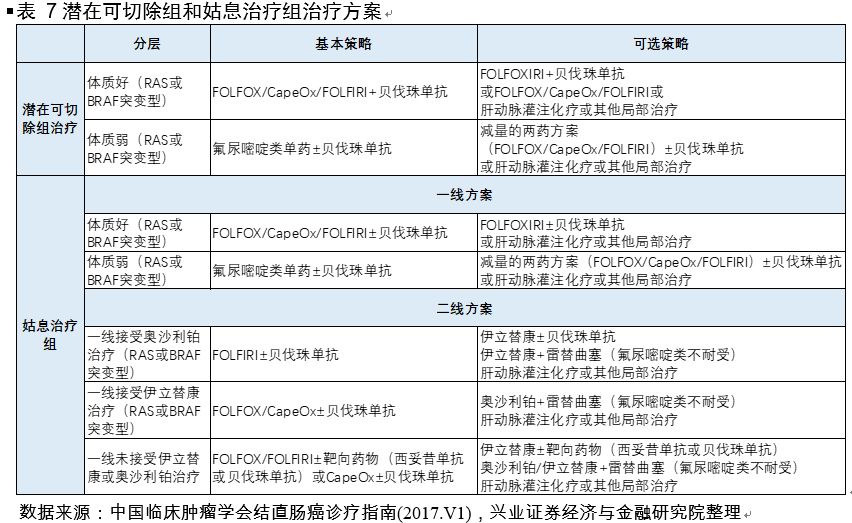
国内贝伐珠单抗转移性结直肠癌适应症潜在市场空间达54亿元。
测算过程-基本假设如下:
1)参考上文所述,2015年预计国内新增结直肠癌患者37.63万人(考虑到PFS等因素,仅计算新增患者,存量患者不在统计范围内);
2)转移性转移性结直肠癌占比60%;
3)RAS和BRAF突变型占比50%
4)参考推荐剂量5 mg/kg 体重,每两周给药一次,以60kg为例,人均用量48支(100mg,4ml规格),考虑赠药的话,人均付费用量24支;
5)按照降价后单支1998元/100mg,则年均用药费用为9.6万元。
基于上述假设来测算,国内RAS或BRAF突变型的转移性结直肠癌的潜在市场空间达108亿。按照中性的渗透率来测算,用于RAS或BRAF突变型的转移性结直肠癌适应症,贝伐珠单抗在国内市场空间可达54亿元。

3.3
国内贝伐珠单抗用于非鳞状非小细胞肺癌市场有望达44亿元
肺癌是国内第一大肿瘤。
根据《Cancer Statistics in China, 2015》报告,2015年预计中国新增肺癌患者73.33万人,因肺癌死亡人数为61.02万人,为国内第一大癌症。2010年,Pao W等在The Lancet Oncology报道,超过80%肺癌患者是非小细胞肺癌(NSCLC)。非小细胞肺癌可以进一步分为鳞状细胞癌和非鳞状细胞癌(腺癌、大细胞癌等),其中非鳞状非小细胞肺癌占比2/3以上。
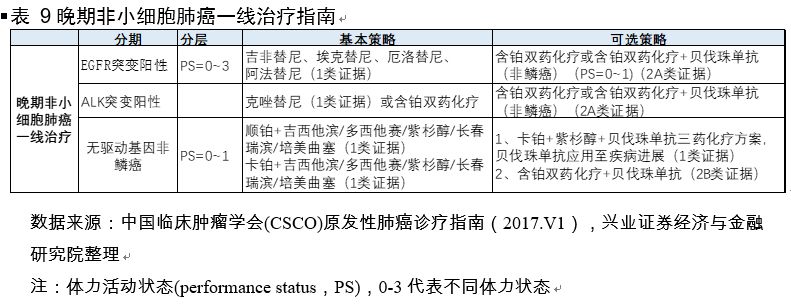
贝伐珠单抗被推荐用于晚期非鳞状非小细胞肺癌患者一线治疗的可选策略
。根据中国临床肿瘤学会(CSCO)原发性肺癌诊疗指南(2017.V1),考虑成本效益和改善患者生存,指南推荐贝伐珠单抗用于晚期非鳞状细胞非小细胞肺癌患一线治疗作为可选策略。随着贝伐珠单抗谈判价格大幅下降,未来有望成为首选策略。此外,免疫治疗药物(抗 PD-1 抗体
Nivolumab
和Pembrolizumab,针对PD-l高表达且EGFR、ALK、ROS1为阴性等患者)为非鳞非小细胞肺癌患者提供了新的治疗选择,该类药物在后续报告将详细来分析。
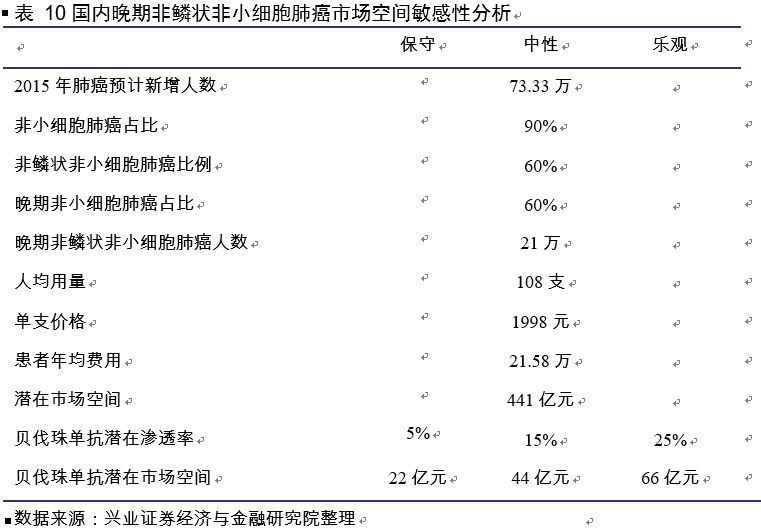
贝伐珠单抗用于国内晚期非鳞状非小细胞肺癌的潜在市场空间可达44亿元。
测算过程-基本假设如下:
1)参考上文所述,2015年预计国内肺癌患者73.33万人(考虑到PFS等因素,仅计算新增患者,存量患者不在统计范围内);
2)按照非小细胞肺癌占比80%;
3)非鳞状非小细胞肺癌占比60%;
4)晚期非小细胞肺癌占比60%,则晚期非鳞状非小细胞肺癌人数达21万;
5)参考推荐剂量为 15 mg/kg 体重,每 3 周给药一次,以60kg为例,以9个月来算,人均用量108支(100mg,4ml规格),考虑赠药的话,人均付费用量27支;
6)按照降价后单支1998元/100mg,则年均用药费用为21.58万元。
基于上述假设来测算,国内晚期非鳞状非小细胞肺癌适应症潜在市场空间达441亿。按照中性的渗透率来测算,用于晚期非鳞状非小细胞肺癌适应症,贝伐珠单抗在国内市场空间可达44亿元。
3.4
医保扩容,未来渗透率有望持续提升。















