连载文章:墨菲的幽灵
目录
前言
第一章 新世界
第二章 幽灵魅影
第三章 荷塘春晓
第四章 柳暗花明
第五章 光荣与梦想
后记
本次推送为第二章:幽灵魅影。前文请点击阅读:
墨菲的幽灵(一)。
进入
20
世纪后,不仅德法两国,乃至整个欧洲的核物理研究都提升到了一个新的高度。这段时期,欧洲的物理学巨匠们在核物理领域获得了一系列载入史册的成果。
1905
年,爱因斯坦初步描绘了物质释放射线时的质能等价猜想,即著名质能方程的雏形,从而把一个全新的核能时代展示在人类眼前。

▲爱因斯坦,1879-1955. 图片来自wikipedia
就在科学家们为一个新时代而激动不已时,萨拉热窝的枪声无情地中断了欧洲物理学的发展脚步。
1914
年至
1918
年的四年间,混乱的欧洲战场吞噬了成千上万优秀青年学者的生命。战争的冲击,以及战后的经济困难与疫病流行几乎摧毁了欧洲的核物理学界,而放射生物学的研究进展甚至完全停滞。
与此同时,战争红利使得美国的科学研究发展驶入了快车道。美国多所大学抓住了历史性的发展机遇,大举吸纳欧洲和美国本土的青年学者,成为了现代生物学研究最为活跃的热土。
自从科学家发现放射线的生物效应开始,就有观点认为这些生物效应可能与遗传物质受到损伤有关。
20
世纪初,人们对遗传物质的本质尚存争议。在
1900
年学术界重新发现孟德尔遗传定律后,美国杰出的遗传学家托马斯·摩尔根
(Thomas Hunt Morgan
,
1866-1945)
使用果蝇作为模式生物,在哥伦比亚大学建立了专注遗传分析的研究中心。自
1908
年至
1915
年期间,他与同事通过一系列实验证明了染色体就是遗传信息的载体。因其研究工作奠定了现代遗传学的基础,托马斯摩尔根荣膺
1933
年诺贝尔生理学与医学奖。

▲托马斯·摩尔根
,
1866-1945,图片来自诺贝尔奖官网
同一时期,美国另一位杰出的遗传学家赫尔曼·穆勒
(Hermann Joseph Muller
,
1890-1967)
把全部的热情投入到了探寻放射线如何影响生物遗传特性的研究中。青年时期的穆勒就读于哥伦比亚大学,得以直接了解到摩尔根教授的果蝇遗传学研究,并对此产生了浓厚兴趣。自
1914
年开始,穆勒在美国辗转多地开展研究,并逐渐把自己的研究重心放在研究影响遗传突变率,尤其是致死突变的因素上。
1918
年,因为实验室的学生和研究人员将被征召奔赴欧洲战场,摩尔根教授的实验室出现了严重的人员短缺,于是他邀请穆勒回到哥伦比亚大学开展研究工作。两年后,穆勒因故未能继续在摩尔根实验室的工作,随后开始了他在德克萨斯大学的独立研究。在这里,他终于有机会使用镭和
X-ray
探究放射线对遗传变异的影响。

▲赫尔曼·穆勒,1890-1967. 图片来自wikipedia
然而,在德克萨斯的最初几年,穆勒没能做出任何有意义的成果,因为绝大多数果蝇在放射线照射后就绝育了。这使得穆勒无法拿到能够用于进一步分析的突变果蝇。经过多年尝试和优化后,穆勒终于在
1926
年拿到了他期待已久的致死突变品系,从而证明放射线能够有效地诱导遗传突变。他的研究成果很快被同行们重复,并推广到其他模式生物中。基于一系列的研究成果,穆勒确定染色体是放射线造成细胞损伤过程中的主要靶点。此后,穆勒作为当时声望颇高的科学家,开始积极地在公共媒体发表文章,宣传放射线诱导遗传突变的危害,尤其是诱发癌症的风险。在他的不懈努力之下,科学家们通过动物实验评估了放射线诱导癌症的风险,并最终推动
FDA
于
1943
年对包括风靡一时的
“
镭补
”
在内所有添加放射性物质的食品下达了禁令。

此外,在学术研究方面,得益于长期积累的实验数据,穆勒在科学史上率先建立了放射剂量与诱导有害突变之间的量化关系,从而奠定了
“
线性无阈值模型
”
的理论基础,并在随后数十年被放射生物学界奉为圭臬,用于评估暴露在放射线下的生物效应危害。
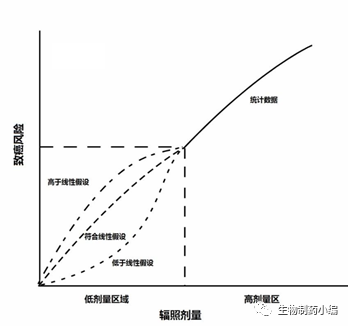
▲
放射线照射与效应关系的线性无阈值模型
本图概念性地描述了线性无阈值模型,用以评估照射剂量与致癌风险之间的剂量效应关系。其中,在低剂量区,实验数据与线性假设存在高于
/
符合
/
低于三种关系。
图片来自于彭宇博士学位论文。
正当穆勒的研究工作蓬勃开展时,高度繁荣的美国突然遭遇了人类历史上最严重的经济危机。大萧条重创了穆勒正在快速扩张的实验室,他不得不缩小实验室规模。穆勒眼里的美国瞬间从天堂跌入了地狱,这使得他对资本主义的未来持悲观态度,并开始通过他实验室几位来自苏联的学者接触共产主义。他的政治倾向给他在美国的发展带来了空前麻烦。此后
10
年间,他曾移居苏联开展工作,因为不能接受李森科的遗传学观点而再次返回美国。

▲
经济大萧条中的美国,1931年,芝加哥。图片来自wikipedia
1941
年
12
月
7
日,日本偷袭珍珠港,美国正式卷入第二次世界大战。在收到爱因斯坦等科学巨匠联署的建议信后,美国政府启动了著名的
“
曼哈顿计划
”
,开始大规模进行核反应堆与核武器测试的研究工作。作为放射生物学的泰斗级人物,穆勒应邀成为
“
曼哈顿计划
”
的顾问,参与评估放射性防护等工作。因为他对放射线伤害的高度关注,以及他的社会主义者身份,他并未被允许参与
“
曼哈顿计划
”
的核心工作。

▲
曼哈顿计划成员,从左至右:
Kenneth Bainbridge, Joseph Hoffman,
Robert Oppenheimer, Louis Hempelmann, Robert Bacher, Victor Weisskopf and Richard Dodson
图片来自Nature Physics 11, 201 (2015)
自
20
世纪
30
年代开始,穆勒一再警示核战争以及核试验中产生的放射性尘埃会带来长期危害,推动公众加强对核试验的监督。因为癌症发生机理的复杂性,在当时,虽然放射线诱导突变的现象已被认可,但穆勒关于放射线致癌的观点被部分学者认为过于激进,而且有些动物实验的结论并不支持他的学术观点,这导致他遭受了不少批评,被认为是在
”
夸大危险,耸人听闻
”
。然而,人们不久就发现穆勒的警告并非杞人忧天。
1945
年,两枚原子弹分别在日本广岛与长崎落下,在造成巨大伤亡的同时,也让很多幸存者遭受高剂量放射线照射。自
1950
年开始,美国和日本的科学家对两地核爆幸存者的癌症发病情况进行了跟踪。多项研究发现年轻时(
<20~30
岁)遭受核爆辐射的人群中,部分恶性肿瘤的发病风险明显高于平均水平。
这些研究成果主要在
70
年代陆续发表于各类临床医学杂志,为科学界提供了大剂量放射线照射诱发癌症的临床证据。至此,放射线的致癌效应完全被科学界所认可。
赫尔曼穆勒晚年所致力宣传的放射性尘埃的致癌危害,终于在他离世后获得权威机构的承认。例如,在美国的《放射线暴露赔偿法案》中规定,所有处于核试验下风口范围内的居民出现任何与放射线有关的癌症时,都将获得
5
万美元的补偿。
然而,仅仅只在
1945
年
-1962
年期间,欧美和苏联就进行了
500
余次大当量的地面核试验,已经导致大量放射性尘埃散布到全球的环境中。放射性尘埃在地球大气中的广泛散布稀释了尘埃密度,降低了单位密度的放射线照射量,但同时也造成更多人群暴露于放射线环境中。长期暴露于低剂量辐射会带来怎样健康危害,是冷战时期放射生物学界新的研究焦点。
作为一代科学名家,赫尔曼·穆勒的科研工作奠定了现代放射生物学的理论基础,并极大地拓展了现代遗传学的研究领域与研究方法;同时,他作为一位社会主义者与和平主义者,广泛联系欧美学术界的和平力量,终生致力于推动核裁军、终止核试验,以及提升公众对于放射线危害的安全防护意识。他的学术成就与他的社会活动都为人类的发展做出了不可磨灭的贡献。
然而,就在科学巨星穆勒的耀眼光芒之下,一位杰出学者的发现被悄然遮蔽。这就是詹姆斯·墨菲(
James Bumgardner Murphy
,
1884-1950
)与他的
X-ray
系列实验。
相比于托马斯·摩尔根与赫尔曼·穆勒,詹姆斯·墨菲的知名度要小很多,维基百科甚至都没有他的词条。本科毕业后,墨菲于
1905
年进入约翰霍普金斯医学院,开始了医学和生理学方向的研究。因为手术操作技能高超,他于
1911
年毕业之后即应佩顿劳斯博士(
Francis Peyton Rous
,
1879-1970
)邀请加入新创立不久的洛克菲勒研究所,参与劳斯博士正在进行的一些前沿研究项目。
在当时,关于癌症发生的诱发因素有各种猜想,其中一种是致癌病毒诱发癌症。劳斯博士正在以鸡肿瘤为研究材料,试图从肿瘤组织滤液中找到这种潜在的致癌病毒。这项研究工作需要执行一些组织移植手术,墨菲的加入为研究提供了重要的技术支持。在研究中,墨菲发现淋巴细胞在组织移植手术之后的生理状况中扮演了重要角色,并由此开始研究移植后排异反应。为了减弱排异反应,墨菲进行了一系列实验试图清除淋巴细胞,包括使用
X-ray
照射实验动物。在尝试清除淋巴细胞的同时,他还顺便研究了放射线对淋巴细胞的影响。在
1922
年发表于实验医学杂志(
J. Exp. Med.
)的论文中,墨菲总结了他的研究小组在此方向的多项实验成果,明确指出高剂量的
X-ray
照射能够摧毁动物的淋巴组织,而有趣的是,低剂量的照射反而能够刺激淋巴细胞的增殖。同时,墨菲的这篇论文中还介绍了一个具体的实验。在这项实验中,墨菲和同事从实验动物身上抽取血清
,
用于培养淋巴细胞。实验结果表明,来自被放射线照射动物的血清,能够刺激淋巴细胞增殖
,
但来自于对照组
(
未被放射线照射
)
动物的血清
,
却会导致淋巴细胞退化。这个现象
,
在使用动物放射线照射后
1~2h
抽取的血清时尤为明显。
墨
菲的实验表明,被放射线照射的动物血清中似乎出现了某种因子,能够让淋巴细胞出现遭受低剂量放射线照射时类似的增殖效应。
詹姆斯·墨菲在这一年所报道的系列研究,揭示了在穆勒的经典模型之外可能有某些因子在细胞间传递着放射线带来的效应,从而让未被放射线照射的细胞也出现一些生物效应。在当时,这种现象完全不能为人们所理解,而且它也与经典的
“
线性无阈值模型
”
直接冲突。这篇论文虽然是作为放射生物学专题的一部分应邀发表,有意思的是,它在发表之后的很长一段时间内被放射生物学界完全无视。因为多种原因,此后很长一段时间,并没有人重复墨菲的实验,或者继续此方向的研究。此外,自始至终,穆勒都没有把这个现象纳入到他关于放射线诱导生物效应的理论体系之中。
墨菲
X-ray
实验中难以解释的结果,成为墨菲无意间释放在放射生物学界的一个幽灵。
身为放射生物学界的边缘人,墨菲自己也并未在此方向继续深入研究,而是凭借其广泛的科学知识,从医学角度关注癌症发生机制。墨菲一生中有不少科学巨匠好友,学术生涯逍遥自在。他在劳氏肉瘤病毒研究中的关键贡献,帮助好友佩顿·劳斯获得了
1966
年诺贝尔生理学与医学奖。墨菲本人在
1950
年平安离世,永远被他的好友们所缅怀。

▲
1966年诺贝尔生理学与医学奖获得者,图片来自诺贝尔奖官网
墨菲的论文发表停止于
1950
年,但幽灵的魅影并未就此消逝。
在墨菲发表
X-ray
实验结果的整整
40
年后,来自田纳西大学农业研究实验室的索托教授(
Jose Souto
),在
Nature
上发表了一篇短小精悍的单作者论文,描述了他所进行的一项有趣的动物实验。索托从被放射线照射的大鼠和羊身上抽取血清
,
过滤后分别注射到未被放射线照射的大鼠中。此外,他还从未被放射线照射的大鼠和羊身上抽取了血清,过滤后分别注射到未接受放射线照射的大鼠中,作为对照组。实验结果发现,实验组(注射来自放射线照射动物的血清)中的大鼠发生乳腺癌的比例显著高于对照组中的大鼠。
相比于墨菲,索托的知名度更低。不过,索托的实验提供了最强有力的直接证据,表明放射线照射后的动物体内出现了某种因子,它能够在未被放射线照射的动物身上诱发癌症。
在墨菲离世
12
年后,他所释放的幽灵再次进入学者的视野。遗憾的是,索托的研究并未在领域内激发持续关注,因为放射生物学领域的研究出现了新的动向。
自广岛长崎核爆以及三哩岛核电站等核事故之后,公众开始高度关注放射线照射后的长期效应。各类核能机构投入资金长期跟踪放射线照射受害者的健康状况。随着研究深入,研究者发现在低剂量照射时,放射线暴露剂量与相应的生物效应之间更多地是非线性关系,这是
“
线性非阈值模型
”
所不能解释的。穆勒所搭建的经典模型首次受到了来自放射生物学领域内的直接挑战。当时,领域内科学家的主流意见是穆勒模型的原理没有缺陷,需要修正的只是具体的量化关系,只需开展实验积累数据对量化关系进行修正即可。
因此,在物理学家协助下,美国多所大学的生物学家搭建了
alpha
粒子放射线设备。因为
alpha
粒子的物理学特性,
“alpha
射线照射剂量
”
可以等价换算为
“
单位时间内每个细胞核被
alpha
粒子击中的几率
”
,让科学家能更好地控制低剂量照射实验中的剂量参数,从而在低剂量范围内实现精确定量研究。哈佛大学的约翰利特(
John. B.Little
)和长泽初美(ながさわはつみ,
Hatsumi Nagasawa)
也采用这种设备进行实验。他们发现多数情况下,低剂量区域的剂量
-
效应关系确实只需要数学校正即可。但是,当剂量进一步降低时,意料之外的情况出现了。在平均
0.07%
细胞核被
alpha
粒子穿透的剂量下,竟然有
30%
的细胞中姐妹染色体交换率
(Frequency ofsister chromosome exchange)
明显上升。这是
“
线性无阈值模型
”
所完全不能解释的现象!在
1992
年的论文中,约翰利特和长泽初美报道了他们的实验,并很快被领域内科学家所重复。
在墨菲的
X-ray
实验发表
70
年后,墨菲的幽灵又一次出现在整个生物医学领域的研究者面前。这一次,人们再也无法忽视他的存在。
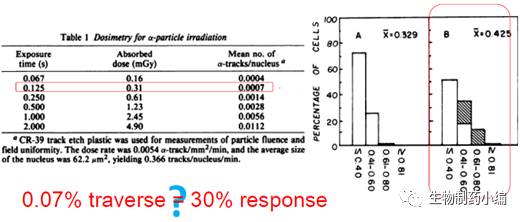
▲
极低剂量照射下,剂量
-
效应关系无法用传统模型解释
图中数据来自约翰利特和长泽初美论文(
Nagasawa andLittle, Cancer Research, 1992
),红色方框指示了当
0.07%
细胞核被放射线粒子穿透时,
30%
的细胞中发生了染色体损伤效应。右侧
A
图为无照射对照,
B
图中灰色区域为相比
A
图增加的染色体损伤比例,即未被照射细胞中发生染色体损伤的比例。
进一步地,再次借助物理学家帮助,放射生物学家搭建了放射线微束
(microbeam)
设备。使用这套设备,科学家可以把放射线照射精确地集中在单个细胞核上。因为此设备的粒子源来自同步加速器,至
2007
年,世界上只建成了两套此类设备。它们分别位于美国哥伦比亚大学放射研究所,以及英国格雷癌症研究所。
借助尖端的放射线微束设备,科学家们在各种细胞系以及多种模式生物中观察到照射区域之外的细胞中发生了诸如染色体损伤、细胞凋亡、细胞周期异常等一系列放射线相关效应。自上世界
90
年代起,科学家们发表了大量研究成果,证实放射线诱导的生物效应并不仅仅只发生在被直接照射的细胞中,而是会扩散到照射区域之外、甚至有一定距离的组织和细胞。至此,人们终于认识到,被放射线照射的细胞确实会释放出某些因子,将放射线照射产生的效应传递给未被照射的细胞,即旁观者细胞(
bystander cell
),并且把这种现象称为
“
放射线诱导旁观者效应
”
(
radiation-induced bystander effects,
简称
RIBE
),而介导
RIBE
的因子则被称为
“RIBE
介导因子
”
。
科学家们相信,只要清楚了
RIBE
介导因子是什么,就能最终揭开墨菲幽灵的真实身份。
今天,人们已经充分认识到
RIBE
的价值。利用
RIBE
现象,临床医师可以在准备放射治疗方案时缩小放射线照射区域,减小健康组织被照射的面积,同时通过诱导凋亡效应间接抑制照射区域周边癌细胞生长,减少放疗诱发二次癌症的风险。另一方面,因为
RIBE
能通过旁分泌方式显著影响被照射区域内生物效应
,
患者可以通过服用药物抑制那些刺激细胞生长的
RIBE
介导因子,削弱被照射癌细胞对抗放射治疗的能力,从而增强放射治疗效果,并保护癌组织附近的正常细胞。
然而,
RIBE
在临床上的应用前景受到了基础研究进展的制约。自
90
年代开始的一系列研究中,研究者提出了多个可能的
RIBE
介导因子,但普遍缺乏足够充分的证据以及深入的机理研究。
这意味着这一方向研究工作的难度大大超过了人们此前的预期。
面对难以突破的瓶颈,
RIBE
领域的研究热度在
21
世纪初到达巅峰后随即快速回落,除了其他领域的研究者偶然进入此方向发表一两篇描述性论文之外,全世界只有少数几位科学家还在默默地坚守
RIBE
研究,同时,可用的放射线研究设备也在日渐减少。
RIBE
研究似乎注定将平淡地迎来它的夕阳,墨菲的幽灵也许将永远保持神秘。
历史的指针悠悠地走到了
2007
年。
这一年,我从清华大学生物系(现生命学院)本科毕业后保送就读本校研究生,并加入了薛定教授
(Prof. Ding Xue
,
Boulder,Colorado University)
在清华大学兼职新建的实验室。当我与
Ding
第一次谈论
RIBE
课题时,我对前文讲述那些科学伟人以及那段波澜壮阔的历史毫无了解。那时,我和
Ding
对
RIBE
的认识仅限于他在
2006
年某次国际会议上与放射生物学专家卡梅尔马瑟希尔(
Carmel Mothersill
)的一次谈话,以及他发给我的两篇马瑟希尔教授的论文。初步了解此方向后,我即刻着手开展实验。
尽管
Ding
此前从未主持过
RIBE
的研究项目,而我在科研上也只是懵懵懂懂的新人,在新实验室与新朋友们开拓新领域的美好前景让我热血沸腾,从此毅然踏上了一条漫长而曲折的道路。
作者注:本文第一章与第二章的部分内容参考了作者博士学位论文,维基百科,相关学术论文,名人生平,以及美国能源部资助项目研究报告等相关资料。

作者介绍:
彭宇,湖北宜昌人,喜爱写作,学生时期有数篇习作发表于各级刊物。高中就读于湖北省宜昌市第一中学,对科学研究萌发浓厚兴趣,曾获生物竞赛全国一等奖、物理竞赛全国二等奖。后放弃保送资格,作为班长与全班同学共同经历2003年高考洗礼,如愿进入清华大学生物系就读。
2007年本科毕业后,保送本系就读硕士研究生,作为实验室第一批学生共同建设实验室,后因决心攻克“放射线诱导的旁观者效应”课题而申请提前攻读博士,有幸获得学院破格批准,自2009年开始正式攻读博士学位。从2007年起,他负责或合作参与不同方向的多项课题研究,覆盖了从基础研究到新药发现等转化研究的多个环节。
2015年毕业后,因在乙肝药物开发的独特经验,进入上海药明康德新药开发有限公司研发服务部进行新药发现阶段研究。2017年,博士期间研究成果《cysteine protease cathepsin B mediates radiation-induced by stander effects》以研究短文的形式发表于国际顶级学术期刊《自然》,受到行业的高度关注。凭借这一杰出成果,被授予清华大学理学博士学位。

















