摘
要:目的
对包载马钱子碱(
brucine
)聚乳酸
-
羟基乙酸共聚物
[
poly(lactic-co-glycolicacid)
,
PLGA
]
(
B-PLGA
)纳米粒进行处方与工艺优化。
方法
采用沉淀法制备
B-PLGA
纳米粒,以平均粒径、多分散系数(
PDI
)、
Zeta
电位、包封率和载药量为评价指标,采用单因素考察法结合星点设计
-
效应面法(
CCD-RSM
)筛选
B-PLGA
纳米粒的最优处方,并将最优处方进行表征及体外释放实验。
结果
最优处方选择丙酮作为有机溶剂,泊洛沙姆
188
(
F68
)作为稳定剂,超声时间为
1 min
,磁力搅拌速度为
900 r/min
,磁力搅拌时间为
30 min
,
F68
用量为
0.35%
,载体用量为
25 mg
,药物用量为
1.0 mg
,有机相与水相的比为
0.54
。所制得的
B-PLGA
纳米粒为淡蓝色乳光透明液体,粒径为(
97.12
±
4.23
)
nm
,
PDI
为
0.098
±
0.035
,
Zeta
电位为(
−
27.30
±
0.31
)
mV
,包封率为(
69.24
±
1.42
)
%
,载药量为(
2.65
±
0.03
)
%
。通过表征,纳米粒形态完整,通过体外释放实验得知,纳米粒体外释放拟合符合
Higuchi
方程。
结论
星点设计
-
效应面法可用于包载马钱子碱
PLGA
纳米粒处方与工艺优化,且优化后的纳米粒具有缓释作用。
马钱子碱(
brucine
)是马钱科马钱属植物马钱子
Strychnos nux-vomica
L.
种子的主要活性物质
[1]
,具有显著性镇痛、抗炎作用
[2]
,还具有抗肿瘤、中枢神经系统兴奋等作用
[3-4]
,是一种高效的抗肿瘤单体,可用于胃癌、肠癌、肺癌、肝癌、白血病等疾病的治疗,但是由于马钱子碱毒性大、水溶性差、体内代谢迅速,且马钱子碱的治疗剂量与中毒剂量较接近
[5]
,故传统制剂不利于马钱子碱发挥药效,从而使其在临床上的应用受到了极大限制。
纳米技术在医学方面的应用研究一直备受瞩目,是近年正在发展的一种新型毫微粒类给药系统,可以降低药物的不良反应、延缓体内释放及具有良好的靶向性,纳米药物在改善药物活性及降低药物毒性方面具有独特优势,具有推动药学发展的巨大潜力
[6-8]
。
目前,聚乳酸
-
羟基乙酸共聚物
[
poly(lactic- co-glycolic acid)
,
PLGA
]
载体作为制剂辅料已被美国食品药品监督管理局和欧盟药品局批准用于临床,是制备纳米粒应用最广泛的生物可降解高分子材料,其对脂溶性药物具有较强的包裹能力,同时降解速率规律,可以实现药物的可控释放,在药物制剂领域中具有巨大的开发价值和市场
[9-11]
。
星点设计
-
效应面法是近年来常用的一种设计方法,可以很好地完成二次项拟合工作,具有实验次数相对较少、精确度高、操作简单、优选条件预测性好等优点
[12-13]
。因此,本实验采用该方法结合单因素考察法进行包载马钱子碱
PLGA
(
B-PLGA
)纳米粒的处方与工艺优化,为马钱子碱进一步临床研究奠定了基础。
1
仪器与材料
1.1
仪器
Waters e2695-2698
高效液相色谱仪系统,美国
Waters
公司;
FA1204B
分析电子天平,济南鑫贝西生物技术有限公司;
HJ-3
恒温磁力搅拌器,常州仪器制造有限公司;
ZetasizerNano-ZS90
激光粒度分析仪,英国马尔文仪器有限公司;
KQ-250DE
型数控超声波清洗机,昆山市超声仪器有限公司;
LVEM5
低电压台式透射电子显微镜(
TEM
),
QUANTUM
量子科学仪器贸易有限公司。
1.2
试剂
马钱子碱对照品,批号
110706-200505
,质量分数
98%
,中国食品药品检定研究院;泊洛沙姆
188
(
F68
),德国
BASF
公司;司盘
40
,江苏四新界面剂科技有限公司;甲醇,色谱纯,北京
Dikma
公司;无水乙醇,分析纯,天津市富宇精细化工有限公司。
2
方法与结果
2.1 B-PLGA
纳米粒中马钱子碱含量测定
2.1.1
检测波长的确定
称取适量的马钱子碱对照品,将其溶解到色谱甲醇溶液中,定容到合适的浓度,二级阵列管检测器上设置检测波长
190
~
400 nm
,进行检测。马钱子碱在
223.3
、
265.7
、
301.2 nm
处有最大吸收峰,结合相关文献报道
[4,14]
的波长范围,确定
265 nm
为马钱子碱的检测波长。
2.1.2
色谱条件
色谱柱为
Dikma C
18
(
250 mm
×
4.6 mm
,
5 μm
);流动相为甲醇
-
[
水
-
乙酸
-
三乙胺(
230
∶
2.4
∶
0.3
)
]
(
30
∶
70
);检测波长为
265 nm
;体积流量
1 mL/min
;进样量
10 μL
;柱温
30
℃。
2.1.3
供试品溶液的制备
从已经准备好的
B- PLGA
混悬液中精确量取
10 mL
溶液,将其加入
15 mL
色谱甲醇中,在
40 kHz
、
200 W
的环境下超声,时间为
20 min
,使纳米粒破乳,将处理后的溶液用孔径为
0.22 μm
的过滤膜滤过后得到
B-PLGA
纳米粒供试品溶液。用同样的方法制取
PLGA
空白纳米粒溶液。
2.1.4
对照品溶液的制备
先精确称量
3.1 mg
的马钱子碱,加入甲醇溶液使其定容至
25 mL
,作为对照品储备液,质量浓度为
124.00 μg/mL
。
2.1.5
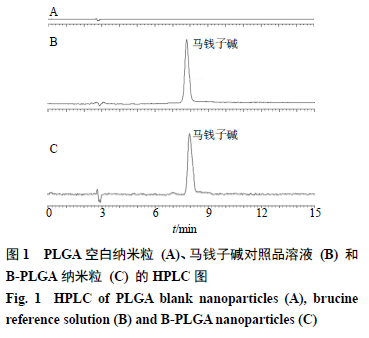
专属性考察
分别取
PLGA
空白纳米粒溶液、马钱子碱对照品溶液和
B-PLGA
供试品溶液在“
2.1.2
”项色谱条件下进行检测,对其专属性进行考察,结果见图
1
。
可以看到,在该色谱检测条件下辅料对主药马钱子碱的含量测定没有干扰,方法专属性良好,因此符合测定要求。
2.1.6
线性关系考察
精密量取马钱子碱对照品溶液
10.00
、
5.00
、
2.50
、
1.25
、
0.63
、
0.31 mL
,置于
10 mL
量瓶中,配制出
6
种质量浓度的对照品溶液,分别为
124.00
、
62.00
、
31.00
、
15.50
、
7.75
、
3.88 μg/mL
。按“
2.1.2
”项色谱条件下进行检测,并记
录峰面积,以马钱子碱质量浓度为横坐标(
X
),色谱峰面积为纵坐标(
Y
),对其进行线性回归,得到线性回归方程为
Y
=
15 539
X
+
39 436
,
r
=
0.999 7
,结果表明马钱子碱在
3.88
~
124.00 μg/mL
线性关系良好。
2.1.7
精密度
试验
取
124.00 μg/mL
的马钱子碱对照品溶液,在“
2.1.2
”项色谱条件下
1 d
内测定
6
次,连续测定
6 d
(每天
1
次),日内精密度和日间精密度
RSD
分别为
0.87%
和
0.90%
,说明日内、日间精密度良好。
2.1.8
稳定性试验
精密吸取同一份
B-PLGA
纳米粒供试品溶液,分别
在制备后
0
、
2
、
4
、
8
、
10
、
12 h
时,按“
2.1.2
”项色谱条件进样测定。结果发现
12 h
内马钱子碱峰面积
RSD
为
1.12%
,表明供试品溶液在
12 h
内稳定性良好。
2.1.9
重复性试验
分别取同一
B-PLGA
纳米粒样品
6
份,按照“
2.1.3
”项下方法制备供试品溶液
,在
“
2.1.2
”项色谱条件下测定峰面积,计算得到马钱子碱质量浓度的
RSD
值为
1.04%
,表明该方法重复性良好。
2.1.10
加样回收率
试验
精密吸取
0.3 mL
的空白纳米粒,共
9
份,分为
3
组,各组分别精密加入
0.3 mL
的低、中、高质量浓度(
10
、
40
、
70 μg/mL
)的马钱子碱对照品溶液,各
3
份,混匀。将处理后的溶液用孔径为
0.22 μm
滤膜滤过,并在“
2.1.2
”项色谱条件下进样检测并记录,计算加样回收率,结果
3
种质量浓度溶液的平均加样回收率在
98%
~
101%
,且其
RSD
值均小于
2%
,结果表明该方法符合检测要求。
2.2
包封率与载药量的测定方法
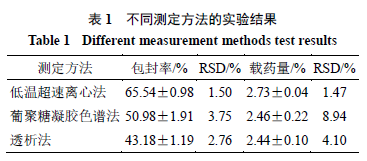
选取几种常见包封率和载药量的测定方法,并对其优缺点等进行分析,选择出适宜的测定方法,不同测定方法实验结果见表
1
。
2.2.1
低温超速离心法
取出
2 mL
的
B-PLGA
纳米粒混悬液,并将其放置在离心机中,在离心半径
40 cm
,
15 000 r/min
转速下离心
30 min
,将沉淀的纳米粒收集,再用蒸馏水超声使其分散,继续离心,重复
3
次,然后用孔径为
0.22 μm
的过滤膜滤过,计算其包封率和载药量。
2.2.2
葡聚糖凝胶色谱法
取出
2 mL B-PLGA
纳米粒混悬液,将其添加到已经经过处理的
Sephadex G-50
凝胶柱上,用蒸馏水洗脱
2 min
,收集纳米粒,然后用孔径为
0.22 μm
的过滤膜滤过,计算其包封率和载药量。
2.2.3
透析法
将装有
2 mL B-PLGA
纳米粒透析袋置于透析外液为含
20%
乙醇
pH 7.4
的磷酸盐缓冲溶液(
PBS
)中,用转速为
1000 r/min
的磁力搅拌器搅拌
4 h
,取透析内液,用孔径为
0.22 μm
的过滤膜滤过,计算其包封率和载药量。
包封率及载药量计算公式为包封率=
(
W
2
-
W
1
)/
W
2
,载药量=
(
W
2
-
W
1
)/
W
3
,其中
W
1
为测得的游离马钱子碱含量,
W
2
为马钱子碱总投料量,
W
3
为
B-PLGA
纳米粒总量。
由表
1
可知,通过低温超速离心法得到的药物包封率与载药量最高,最低的是透析法;而且,透析法耗费的时间较长,所以不排除存在纳米粒中药物释放的可能;葡聚糖凝胶色谱法的
RSD
值较大,可能因为某批次样品稀释过程中导致药物泄露,使得包封率和载药量的数值不稳定;低温超速离心法测得包封率和载药量较高且偏差值较小;因此,本课题最终确定使用低温超速离心法对纳米粒的包封率进行检测。
2.3
B-PLGA
纳米粒处方工艺优化
2.3.1
制备方法的选择
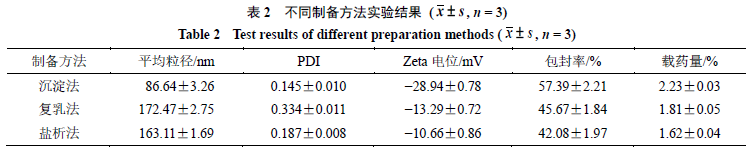
选取几种常见的制备方法,并对其制备过程及优缺点进行分析,选择出
B-PLGA
纳米粒适宜的制备方法,不同制备方法实验结果见表
2
。
复乳法:用质量为
1.2 mg
药物和
1 mL
蒸馏水
混合成溶液并将其作为内水相,用
W
1
表示;然后
用
25 mg
共聚物和
10 mL
丙酮混合并经过超声处理后作为油相,用
O
表示;用蒸馏水将聚山梨酯
80
制备成浓度为
0.2%
的水溶液作为外水相,用
W
2
表示。操作方法:首先取出
O
溶液并向其中加入
W
1
,然后将
O
与
W
1
的混匀溶液放入细胞破碎仪中,超声
30 s
;然后将其加入到
17.6 mL W
2
溶液中并放入磁力搅拌器中,再次超声
30 min
后得到并
W
1
/O/W
2
复乳;然后将溶液放入蒸发仪中除去有机溶剂,获得纳米粒溶液。
沉淀法:称取出
25 mg
共聚物,将其放入到
10 mL
丙酮中,超声使其溶解,该溶液作为有机相。向里面添加
1.2 mg
药物,再次超声使其充分溶解。配制
20 mL
含
0.05% F68
的水溶液,将其作为水相,将有机相加入到水相中并将其放在转速为
1000r/min
的磁力搅拌
30 min
,将溶液放入旋转蒸发仪中除去有机溶剂,获得纳米粒溶液。
盐析法:取
0.5 mL PLGA
共聚物材料的丙酮溶液,加入到
1.5 mL
含
28% MgCl
2
的
F68
溶液中,混合后的溶液超声
3
次,每次时间为
10 s
。再加到
1.5 mL
的溶有
10 mg
药物的水中,使丙酮扩散,于室温条件下磁力搅拌,直到丙酮全部挥干,即得。
由表
2
可知,不同的制备方法对制备
B-PLGA
纳米粒有着不同的影响。
3
种方法比较后可知,沉淀法制备纳米粒时药品包封率和载药量均高于其他
2
种方法,粒径最小,分散较好,且沉淀法实验操作过程较其他
2
种方法简便。因此,本课题选择使用沉淀法作为
B-PLGA
纳米粒的制备方法。
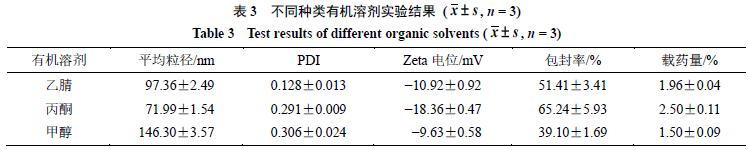
2.3.2
有机溶剂种类的考察
在保持其他条件不变的情况下,以乙腈、丙酮、甲醇有机溶剂作为有机相制备纳米粒,判断有机溶剂种类对
B-PLGA
纳米粒制备的影响,结果见表
3
。
由实验数据可知,丙酮作有机溶剂时的纳米粒的平均粒径最小,但是其包封率和载药量都最大,粒径分布均匀,体系稳定,所以本实验最后确定有机溶剂为丙酮。
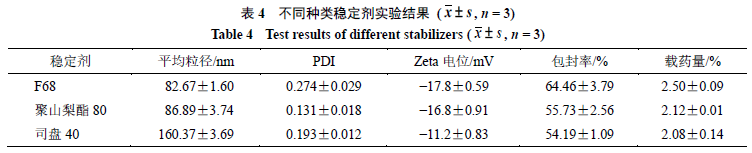
2.3.3
稳定剂种类的考察
在保持其他条件不变的情况下,分别以
F68
、聚山梨酯
80
、司盘
40 3
种表面活性剂为稳定剂制备纳米粒,考察不同种类稳定性对
B-PLGA
纳米粒制备的影响,结果见表
4
。
随着稳定剂的改变,平均粒径和
Zeta
电位逐渐变大,而
PDI
均较好,包封率和载药量都在逐渐变小,由此可见,
F68
较聚山梨酯
80
和司盘
40
更加稳定,所以应用
F68
作为本实验的稳定剂。
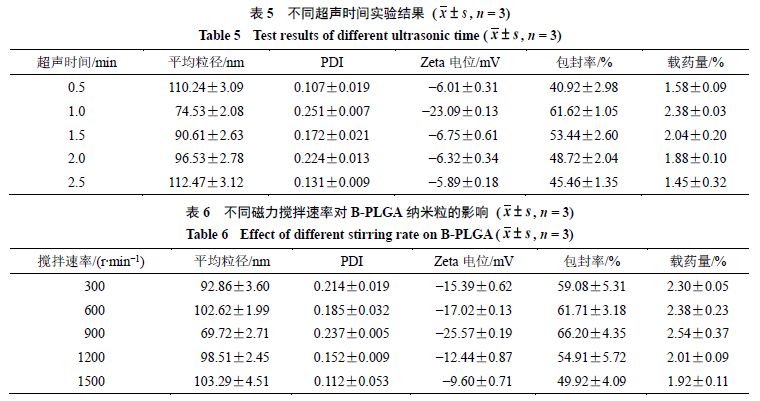
2.3.4
超声时间的考察
保持其他条件不变,考察超声时间分别为
0.5
、
1.0
、
1.5
、
2.0
、
2.5 min
时,
对
B-PLGA
纳米粒制备的影响,结果见表
5
。随着超声时间的增加,平均粒径和
Zeta
电位均是先减小后增大,而其包封率和载药量都是先增大之后减
小。根据推测可能是因为超声时间的增加会使得纳米粒重新聚结,导致药物泄漏,粒径增大,包封率和载药量变小,所以本实验最后确定超声时间为
1.0 min
。
2.3.5
磁力搅拌速率的考察
保持其他条件不变,考察
300
、
600
、
900
、
1200
、
1500 r/min 5
个搅拌速率对
B-PLGA
纳米粒制备的影响,结果见表
6
。
当磁力搅拌速率在
900 r/min
时平均粒径最小,纳米
粒的分布相对均匀,
体系稳定,包封率和载药量均处于最大值。所以,本实验磁力搅拌的速度确定为
900r/min
。
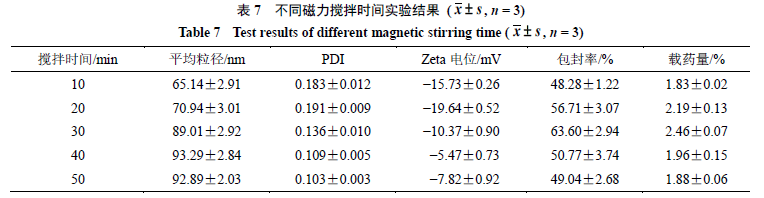
2.3.6
磁力搅拌时间的考察
保持其他条件不变,考察
10
、
20
、
30
、
40
、
50 min 5
个磁力搅拌时间对
B-PLGA
纳米粒制备的影响,结果见表
7
。
当磁力搅拌时间为
30 min
时,纳米粒的分布相对均匀,粒径的大小变化不大,包封率和载药量都最大,所以本实验最后确定的磁力搅拌时间为
30 min
。
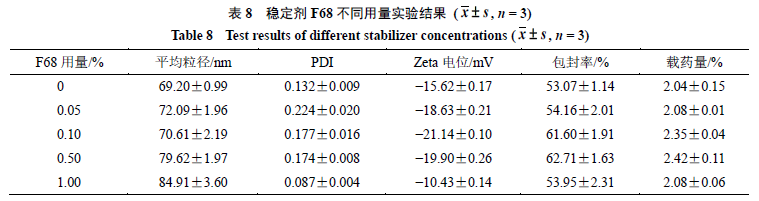
2.3.7
稳定剂
F68
用量的考察
保持其他条件不变的前提下,将
F68
用量设置成
0
、
0.05%
、
0.10%
、
0.50%
、
1.00%
系列不同的用量制备纳米粒。考察
F68
用量对
B-PLGA
纳米粒制备的影响,结果见表
8
。
随
F68
用量的逐渐增加,平均粒径逐渐变
大,但包封率和载药量均呈先变大后又变小的趋势,由此可知,
F68
用量对
B-PLGA
纳米粒制备的影响较大,而在
F68
用量为
0.5%
左右包封率载药量较大,所以本实验最后确定
F68
用量为
0.50%
左右,需进一步优化。
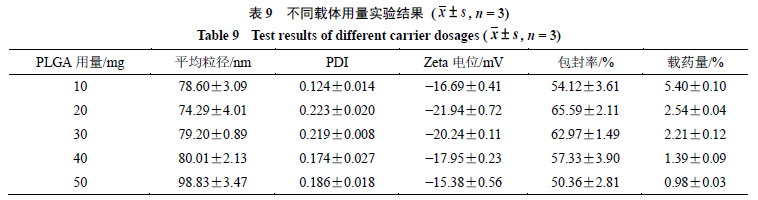
2.3.8
载体
PLGA
用量的考察
保持其他条件不变,选择
10
、
20
、
30
、
40
、
50 mg 5
个
PLGA
用量
对制备
B-PLGA
纳米粒的影响,结果见表
9
。平均粒径和
Zeta
电位先变小后变大,包封率先变大后变小,载药量逐渐变小,可见载体
PLGA
用量对
B-PLGA
纳米粒的制备影响较大,载体用量在
20 mg
时,包封率最大,所以需对载体用量进一步优化。
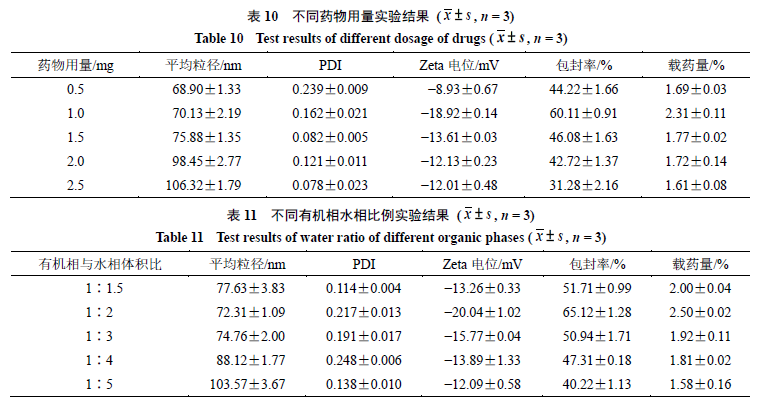
2.3.9
药物用量的考察
保持其他条件不变,通过改变药物用量,判断药物用量对
B-PLGA
纳米粒制备的影响。分别制备
0.5
、
1.0
、
1.5
、
2.0
、
2.5 mg 5
个药物用量的纳米粒,结果见表
10
。
随着药物用量的增加,平均粒径逐渐变大,
Zeta
电位先变小后变大,包封率和载药量先变大后变小,药物用量在
1.0 mg
时,包封率和载药量均最大,所以本实验最后确定的药物用量为
1.0 mg
。
2.3.10
有机相与水相体积比的考察
保持其他条件不变,将有机溶剂与水的体积比作为变量,分别设置
5
个比例
1
∶
1.5
、
1
∶
2
、
1
∶
3
、
1
∶
4
、
1
∶
5
考察对制备的
B-PLGA
纳米粒的影响,结果见表
11
。
有机相与水相比例的逐渐减小,使得平均粒径和
Zeta
电位值先变小后又逐渐变大,分布均匀,体系稳定,包封率和载药量均逐渐增大后减小。因此,当有机溶剂和水的比例在
1
∶
2
时,纳米粒的状态最好,可进一步优化。
2.4
星点设计
-
效应面法
(
CCD-RSM
)
优化处方
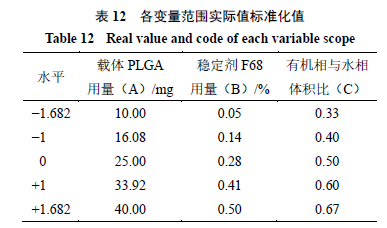
2.4.1
实验设计
在前期对于影响
B-PLGA
纳米粒
各种指标的单因素考察基础之上,发现载体
PLGA
用量、有机相与水相体积比、稳定剂
F68
用量对处方考察指标影响较大,所以本实验需要针对这
3
个因素进行更加深入的
CCD
实验设计。本实验共从
5
个角度对其进行衡量,其中包括中心点、析因设计点、极值点。当
r
=
1.682
,各个变量范围的实际大小和标准大小见表
12
。本实验将包封率和载药量作为响应参数,分别用
Y
1
和
Y
2
表示,然后进行
CCD
实验,实验结果见表
13
。
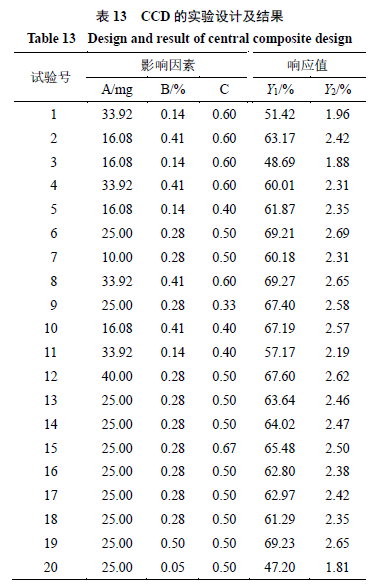
2.4.2
模型拟合及方差分析
分析软件为
Design- Expert V8.0.6
,以包封率(
Y
1
)、载药量(
Y
2
)分别对
A
、
B
、
C
实验数据进行二次多项式回归方程拟合。
二次多项式拟合方
程:
Y
1
=
71.42
-
0.042A
+
6.41 B
+
0.72 C
-
1.14 AB
+
1.34 AC
+
4.27BC
-
3.60 A
2
-
5.61 B
2
-
0.93 C
2
(
r
2
=
0.915 8
,
P
=
0.000 1
);
Y
2
=
1.86
-
9.153
×
10
−3
A
+
0.061B
+
0.011 C
-
0.016AB
+
0.026 AC
+
0.091 BC
-
0.071 A
2
-
0.120B
2
-
0.018 C
2
(
r
2
=
0.885 1
,
P
=
0.000 1
)。
从
r
2
和
P
的计算结果可以看出,二次多项式的拟合相对较好,因此可用此模型对
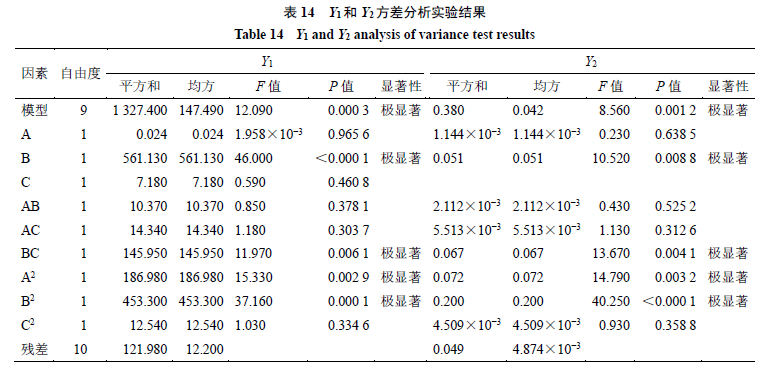
B-PLGA
纳米粒的处方进行分析和预测,其分析实验结果分别见表
14
。由表
14
可
知,
Y
1
、
Y
2
模型项
P
<
0.001
,说明回归方程的关系是极显著的。对于
Y
1
模型方程
B
、
BC
、
A
2
、
B
2
都是显著项,是
Y
1
的显著影响因素,交互影响因素
3D
效果图与等高线图见图
2
。对于
Y
2
模型方程
B
、
BC
、
A
2
、
B
2
都是显著项,是
Y
2
的显著影响因素,交互影响因素
3D
效果图与等高线图见图
3
。