
方法验证的目的是通过测试会造成粒径结果差异的所有可能参数,以确定方法的稳健性和完整性。FDA将验证定义为“建立文件证据,提供高度的保证,确保特定的过程能持续生产符合其预定规格和质量属性的产品”
1、软件的验证
定期进行测试以确认其性能(IQ / OQ(至少每年一次)。
软件是经过验证的软件,应符合CFR211 Part 11的规定。
本文将依次考虑每个主要变量。
2、方法的验证
(1)取样
对于粒度测定,
第一步就是如何取出具有代表性的样品
。从表1中可以看出,不同取样方法是有很大差异的。
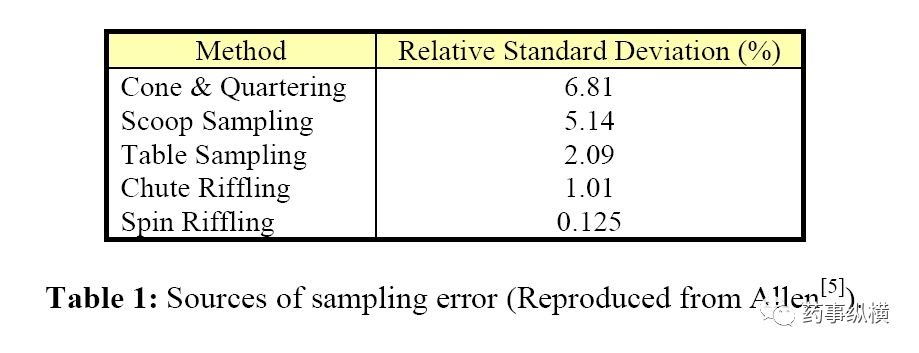
Riffling法最适合自由流动的粒子,但如果要处理大量的粉末,可能需要很长时间。如果样品是悬浮液,那么这会带来一系列的问题。而粉末,在运输过程中导致堆顶部的大颗粒和在底部的细粉,悬浮液将会相反。
大颗粒必须充分混匀。
使用某种搅拌器(特别是磁力搅拌)可能会导致大颗粒被抛到容器的外部而不能被取到。
(2)样品制备
样品制备为“以有意义的方式将样品预处理和进行测量的技术”。
样品分散时,任何情况下,分散介质,空气(用于干法分散)或液体都不应对颗粒造成不可逆的改变(如溶解或聚集)。
整个样品制备过程时方法开发的一部分,而不是验证。
(3)
范围
理论上仪器的检测范围应覆盖样品的粒子范围,对于范围在20nm-2000μm之间的粒度仪来说,对于大多数药物样品的检测没有问题。
(4)专属性
在粒度分析中没有严格的要求来进行这个测试。适当的技术应该在方法开发中建立。当然,不同的粒度分析方法可能会导致同一样品的不同结果。另外,
对于激光粒度检测,很难开发一种能区分制剂内中不同组分的粒度分析方法。在悬浮液的情况下,可能需要配制空白混合物并分开分析。
(5)耐用性
分析方法的耐用性表明其能够保持不受测试参数的微小变化的影响,从而在日常使用中保证其可靠性。
在进行重复性,重现性和中间精密度测试之前,应考虑方法的耐用性。
通常考虑的变化是测量持续时间和测量稳定性的变化。干法测量的气压和湿法测量的泵/搅拌速率的变化是方法开发的重要部分,通常在这里可以简要提及。
a)测量时间
这个测试的目的是确定一个合适的测量持续时间,然后用于重复性,重现性和中间精密度测试。
样品应按照所研究的方法进行制备。
10次测量的周期应该持续2,5,7,10和15秒的时间。应记录每个时间的单个数据和平均数据。结果可以绘制成图。可以通过中值粒度的相对标准偏差来选择适当的持续时间。对于中值粒径[D(v,0.5)]大于10μm的粒子,相对标准偏差(RSD)应小于3%;中间值粒径小于10μm的粒子的RSD必须小于6%。
这反映了一个事实:即较小的颗粒越难分散。
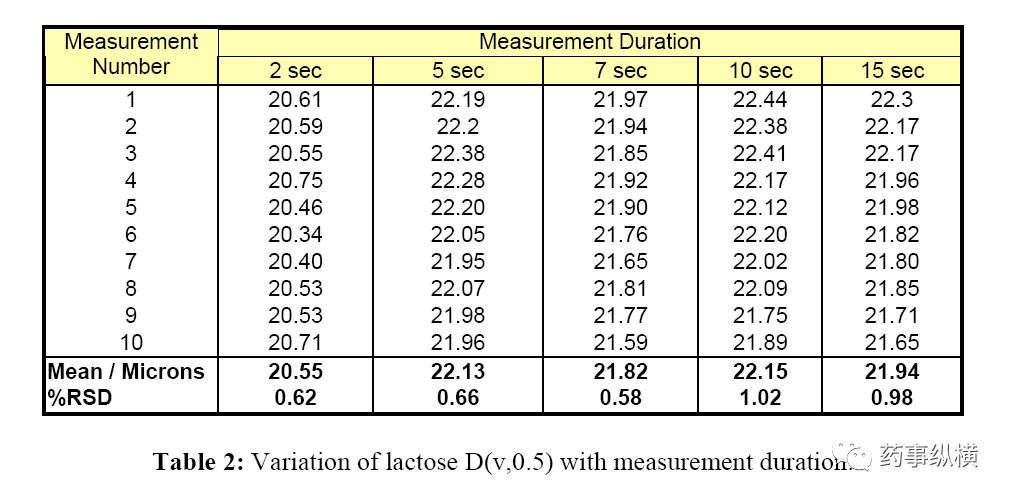
可以看出RSD随时间增加,因此选择RSD低(5秒)的中间点进行测量。从总体数据看,可以推断2秒是不够的,因为它似乎没有给予较大的粒子足够的时间进行采样,所以D(v, 0.5)明显较低。
b)重复性/样品测量稳定性
为了确定样品在分析过程中是否稳定且不发生团聚,解聚或溶解,有必要在已知时间点监测粒度分布。
样品应按照所研究的方法进行制备。
建议在初期建立的时间内至少进行五次测量。测量可以在1、3、5、7和10分钟后进行。应在每个时间点至少进行五次重复测量。然后应确定D(v,0.1),D(v,0.5)和D(v,0.9)值的平均值和相对标准偏差。
对于D(v,0.5)大于10μm的物质,当满足下列条件时,可接受的时间点标准:D(v,0.5)RSD 小于3%,D(v,0.1)和D(v,0.9)RSD小于5%。
对于D(v,0.5)小于10μm的物质,当满足下列条件时,可接受的时间点标准为:D(v,0.5)RSD小于6%,D(v,0.1)和D(v,0.9)RSD 小于10%。
这反映了较小的颗粒更难分散的事实。这些是ISO13320中规定的可接受性的标准,许多样品应该很容易达到更低的RSD。
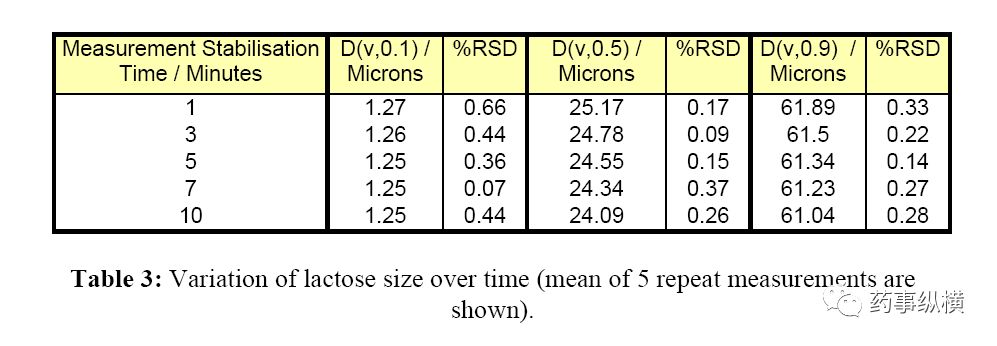
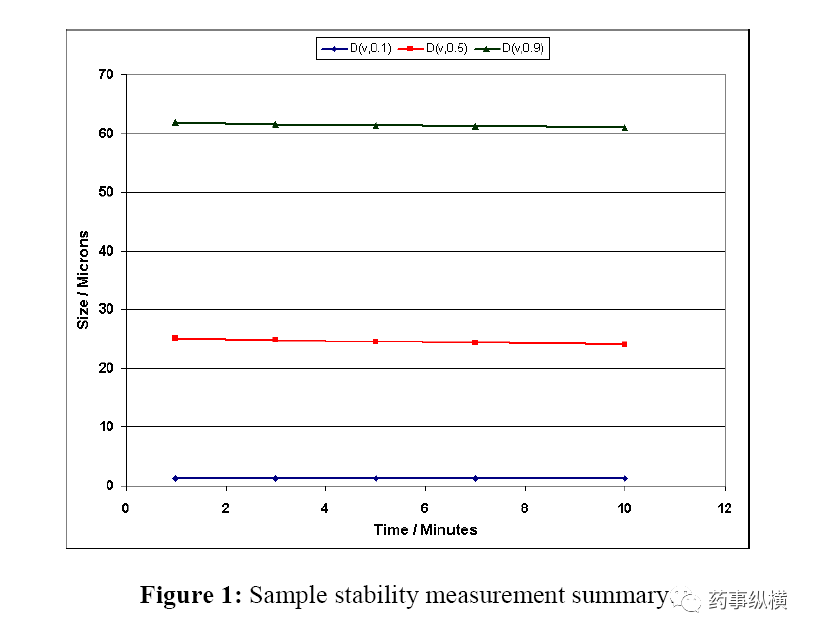
从上述结果可以清楚地看出,乳糖样品在悬浮状态下是稳定的。从这些结果可以确定,1分钟后应进行测量,以使样品时间达到平衡。
c)气压(干式测量)/超声波(湿式测量)
作为方法开发的一部分,应先进行压力确定(见ISO 13320第6.2.3.2节)。
合适的压力使颗粒分散,但不发生颗粒减小。
大多数药物是易碎的,如果压力太高,将在进料器被研磨成粉。分散和研磨通常同时发生(导致分布变宽)。通过在不同的压力下测量相同数量的样品(理想地通过旋转切割器采样到单一粒径),可以确定在没有研磨的情况下达到最大分散时的压力。证明没有发生研磨的最好方法是湿和干分散,获得几乎相同的结果。
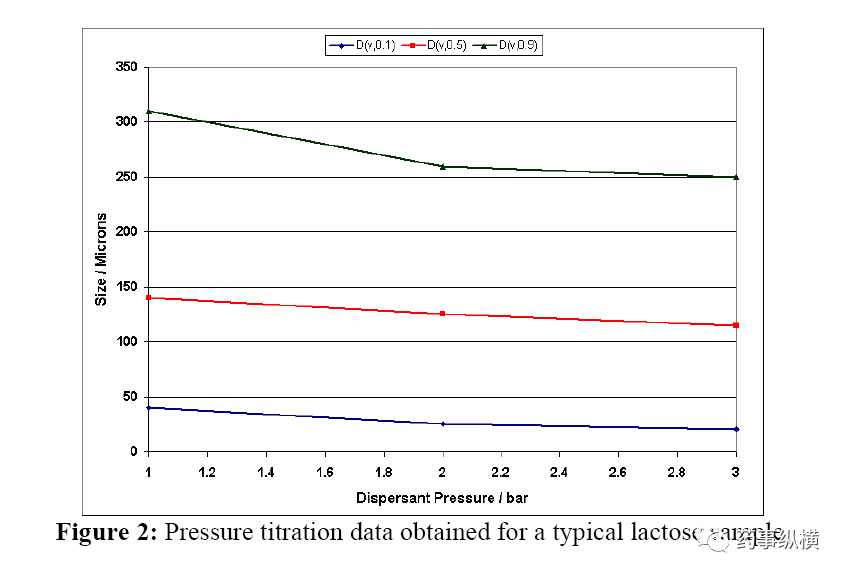
由上图可见,1 bar的压力不足以材料分散。只要压力大于2 bar,就可以获得好的结果。
ISO 13320建议使用超声波辅助分散,过多的超声波会击碎的药物颗粒,尽管这是极不常见的。
作为方法开发的一部分,应该测试改变超声波的持续时间和功率对粒度分布的影响。
理论上,应在超声波检查之前,期间和之后分别进行测量,以检查声波处理对测量的耐用性有何影响。除了分离颗粒之外,超声波还可以增加颗粒-颗粒碰撞的速率,实际上还可能导致聚集。
d)泵和搅拌速率
测量过程中使用的泵和搅拌速度应作为方法开发的一部分进行测试。
所选择的条件应该能够在不引起夹带空气的情况下悬浮所有物质(如果使用表面活性剂则是特别的问题)。
图3显示了根据搅拌器设置,乳糖样品结果的变化。可以看出,2000rpm以上时结果达到稳定。正是在这一点上,所有的物质正确地悬浮和分散。搅拌速率在2000rpm以下时,样品沉降导致结果比预期小。
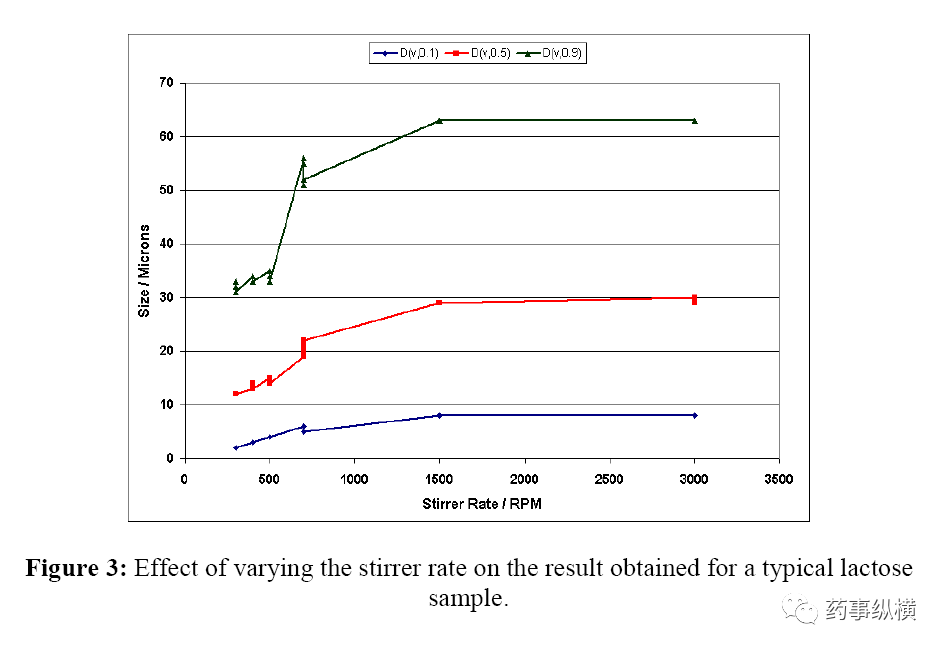
e)折射率选择的确认
折射率的选择应该作为方法开发工作的一部分。
可以使用折射率匹配流体来提供真实折射率的实验证据。
(6)线性















