欢迎点击
【药用植物研究前沿】
↑关注我们!
来源:
iDRUGS
药物研发具有投入大,风险高,周期长。近年来,以深度学习为代表的人工智能技术在药物研发领域已经崭露头角,尤其是在药物发现阶段中全新分子库生成,活性及
ADMET
性质预测以及药物合成路线预测等方面,深度学习技术相比传统机器学习方法体现出明显优势。因此,人工智能技术被业界寄予厚望,利用该技术降低药物研发成本,缩短研发时间,进而加速药物研发进程。
今日,广东省微生物研究所谢黎炜研究员团队与中大药学院徐峻教授团队联合,在药物化学权威杂志
EuropeanJournal of Medicinal Chemistry
发表了标题为“
Deep learning enables discovery of highlypotent anti-osteoporosis natural products
”的文章
,报道了基于深度学习技术从天然产物库中虚拟筛选发现全新的高活性抗骨质疏松活性化合物,虚拟筛选发现的
5
个天然产物结构新颖,其中体外活性最好的
2
个化合物分别为
32nM
和
68nM
;已提交中国发明专利申请,具有重要的潜在开发价值。
骨质疏松
骨质疏松症是一种以骨量低下,骨组织微结构损坏,导致骨脆性增加,易发生骨折为特征的全身性骨病。骨质疏松性骨折作为骨质疏松症的严重并发症,危害巨大,是老年人致残和致死的主要原因之一。我国已成为世界上老年人口绝对数最大的国家,人口老龄化日趋严重。骨质疏松症作为老龄化社会常见疾病,发病率高,是影响老年人生活质量的重要因素,同时长期的治疗与护理带来巨大的家庭和社会负担。目前临床上抗骨质疏松药物主要包括:抗骨吸收药物,如双膦酸盐类、雌激素受体调节剂、
RANKL
抑制剂等;促骨形成的药物,如甲状旁腺激素类似物。这些药物虽然能在一定程度上提高骨质疏松患者的骨密度,但存在各种副作用,如双膦酸盐类药物会引起下颌骨坏死,雷洛昔芬会引起静脉栓塞。因此,我们亟需研究更加有效、副作用更小的抗骨质疏松症治疗药物。
基于深度学习的虚拟筛选及实验验证
深度学习的优势在于非监督式学习特征,并在图像、语音、自然语言处理等方面取得巨大成功,然而,在化学领域,化学任务的机器学习方法依然依赖于复杂的特征工程。
2017
年谷歌提出了消息传递网络(
Message PassingNeural Network
,
MPNN
),首次证明
MPNN
可以直接从分子图中学习到分子的特征并应用于各种分子性质的预测中。本文从文献和数据库中收集基于细胞水平测试的抗破骨细胞活性的表型数据集,使用注意力机制的消息传递神经网络(
SA-MPNN
)模型在
logP
数据集(
21364
个分子)上进行预训练,然后利用抗破骨细胞活性的表型数据集进行迁移学习得到最终模型(
P-SAMPNN
),同时作为对比,构建了基于
ECFP
分子指纹的随机森林(
RF
)和全连接神经网络
(DNN)
模型,基于
SMILES
的注意力机制的双向长短期记忆网络
(SA-BiLSTM)
模型。结果显示,
P-SAMPNN
模型具有明显优势,模型
AUC
值为
0.92
。随后利用该模型对
specs
天然产物数据库进行预测,选择打分较高的化合物,通过结构分析以及肉眼筛选,从中选择
10
个天然产物购买并通过体外破骨细胞分化实验测试,发现
5
个活性天然产物,其中
2
个纳摩级,
3
个微摩尔级,其中活性好的
2
个化合物为异喹啉类生物碱,体外活性均优于目前经典的抗骨质疏松药物阿仑膦酸钠。通过结构相似性分析发现,
5
个活性天然产物与已报道的化合物相似度低,均为全新骨架化合物,具有良好的后续开发价值。
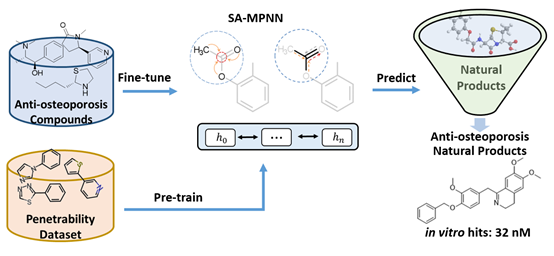
图
1.
基于深度学习的抗破骨细胞活性抑制剂的虚拟筛选流程
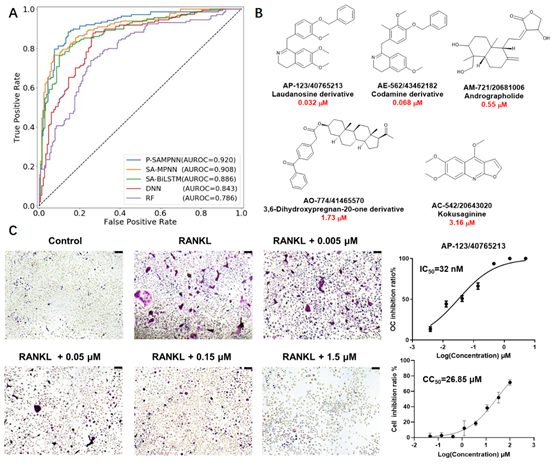
图
2.
不同模型表现以及基于
P-SAMPNN
筛选到的
5
个活性天然产物。
活性天然产物显著抑制破骨细胞相关基因表达及其成药性预测
基于深度学习虚拟筛选发现的
2
个
nM
级活性化合物为异喹啉类生物碱,初步机制研究发现,这两个化合物均可以计量性显著降低破骨细胞成熟分化中关键基因
Ctsk
,
Nfatc1
,
Tracp
以及
Rank
的表达,进一步确证了细胞水平的筛选数据,同时将上述基因比对到
KEGG
中破骨细胞成熟分化通路图中,可以推测这类活性化合物应该是作用于通路上游基因。为进一步研究这
2
个化合物抗破骨细胞分化的特异性以及成药性,我们对化合物进行了
PAINS(pan-assayinterference compounds)
检测和
ADMET















