
通常人们认为人体所有细胞的DNA突变都是一样的,然而,在个体发育过程中,在不同的细胞亚群中每时都发生着频率较低的自发突变。因此这些突变可能在人的一些细胞中出现,但不是全部细胞。这些体细胞“嵌合”突变类似于新发突变,因为它们没有经过纯化选择,因此比遗传自父母的变异更有可能有害。新发突变是许多孟德尔单基因遗传病和复杂疾病遗传变异的主要组成部分。从父母向小孩遗传的嵌合突变可能富集致病性,类似于在疾病群体中鉴定的新发突变。因此,在家族基因数据中分析出嵌合遗传的方法是至关重要的。
全外显子组测序对最可能携带致病变异的编码区进行检测,是研究遗传疾病的有力工具。全外显子组测序数据也可用于分析嵌合突变,因为在有些区域其测序深度还是比较高的。
我们对两个队列筛查了嵌合突变,分别是儿童期不明原因猝死和癫痫性脑病,猝死队列包括9个家庭,每个家庭都有一个先证者猝死,通过尸检未发现死因,我们怀疑猝死患者或多或少都与癫痫和心脏疾病相关。据统计24-32%的猝死病例有热性惊厥史,而对照组仅为2-4%。癫痫脑病队列为338例trio家系,有很大比例的患者为致病性新发突变导致。
介绍嵌合遗传导致儿童期不明原因猝死的家庭
九个猝死家庭其中一个家庭由两个健康的父母和三个后代组成:一个无症状的儿子,一个在20.8个月时意外死亡的女儿(猝死先证者)和一个Dravet综合症的儿子。
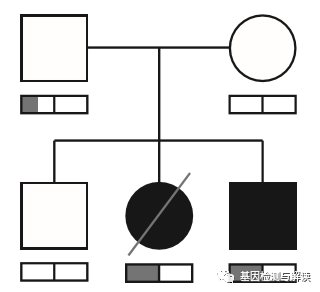
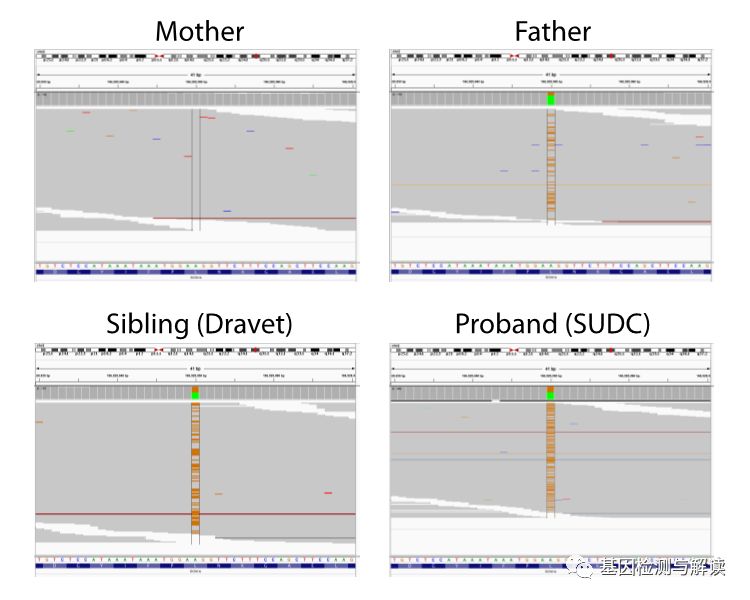
图1 先证者与Dravet综合症携带SCN1A致病位点50%突变丰度(杂合子),父亲没有表型但携带25%的嵌合突变
先证者和Dravet综合征弟弟都伴有热性惊厥。先证者是足月出生的; 她有正常的发育节点,没有医疗问题。在7个月大到死亡时,她有七次热性惊厥发作。一个假设是,先证者和患有Dravet综合征的兄弟共有一个致病变异。 我们对两个孩子按照隐性基因分析没有得到阳性结果。然后,我们开发了一种筛查技术,使我们能够分析这个家庭和其他猝死家庭从父母遗传的嵌合的致病性变异。
嵌合突变遗传筛查
我们构建了一个系统的筛查策略,在家系trio基因数据中以确定亲代的嵌合突变遗传事件。对于给定的trio,筛选标识出对照组中不存在的高质量非同义变异,在先证者中是杂合的,并且在父母的reads中也观察到一定比例,对于这些变异,我们然后对携带者亲代和先证者孩子的突变等位基因reads ratio进行二项式精确检验,以确定获得父代和孩子中观察到的reads比率的可能性。

图2 筛选嵌合突变流程
结果
猝死队列嵌合突变筛查
在该队列中挑选出606个非同义突变,作为亲代其突变reads与野生型reads比例需要偏离0.5,而子代趋向0.5,我们发现有2个高可信度的位点符合,
后续通过一代测序验证发现只有一个符合。
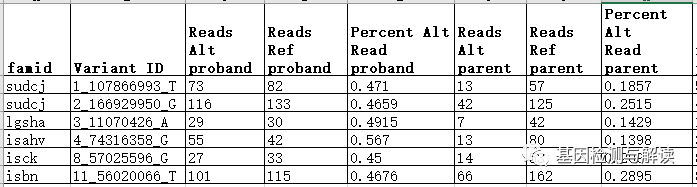
表1 猝死与癫痫脑病队列疑似嵌合突变遗传案例
癫痫脑病队列嵌合突变筛查
对338个trio家系亲代与子代两两比较发现有13142个罕见的非同义突变,有四个位点符合标准。其中只有SLC6A1预测为有害,一代测序验证符合。
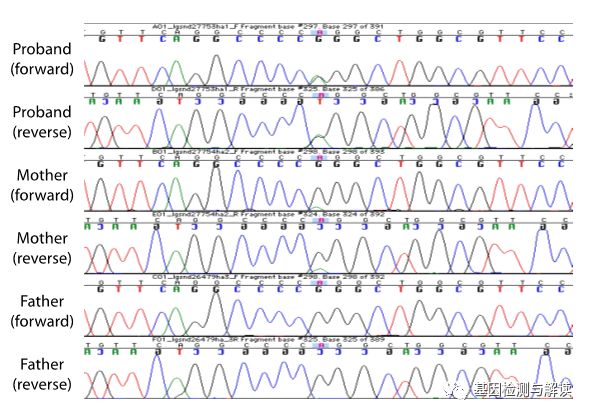
讨论
受猝死先证者父母SCN1A嵌合突变的启发,我们开发了一个通用筛选方法来鉴定家系中的父母嵌合突变遗传。当我们将这种筛选方法应用于9个猝死家庭队列以及338个trio癫痫脑病队列时,我们在693个父-子对中确定了6个嵌合突变遗传。我们的研究结果表明,这个基本的框架已经可以用来系统地筛选父母嵌合突变遗传的数据。由于这些遗传的嵌合突变像新发突变一样,不必经过纯化选择,所以当确定用于严重早发性疾病的患者时,它们是特别有意义的。目前还不清楚有多少未确诊的遗传性疾病可以通过亲本嵌合遗传来解释,特别是考虑到使用标准全外显子组测序数据检测到这种事件的频率较低。然而,我们的结果表明,在临床确定致病变异的时候,除了注重分析新发突变,也要考虑父母嵌合突变。





