HR+乳腺癌患者长期面临疾病复发的风险,因此,延长内分泌辅助治疗可能可以进一步降低疾病复发风险。既往的研究已经显示,对于辅助他莫昔芬5年后继续延长内分泌治疗可以降低疾病进展风险。但对于HR阳性的绝经后早期乳腺癌患者中,序贯5年辅助内分泌治疗后,继续延长AI治疗,是否可以进一步降低疾病复发风险,尚无研究证据。近期,DATA研究结果正式发布在《Lancet Oncology》,将为这一问题带来答案。
近10年来,乳腺癌的治疗取得重大进展,患者的总生存得到显著提高。回顾欧洲乳腺癌患者的生存数据,1999-2001年,乳腺癌年龄调整的5年相对生存率为78%,2005年-2007年,5年相对生存率为78%升高到82%。既往的数据显示,在绝经后HR阳性的乳腺癌患者中,辅助5年AI,或2-3年他莫昔芬序贯AI满5年,相比于辅助他莫昔芬5年,可以降低30%复发风险。在辅助他莫昔芬5年后继续延长他莫昔芬的治疗或AI,同样可以改善生存。因此,ASCO和ESMO指南推荐,HR阳性的早期乳腺癌,推荐使用辅助AI治疗或他莫昔芬序贯AI治疗满5年,或接受他莫昔芬5年的患者继续延长辅助内分泌治疗至10年。
此外,一些临床医生会推荐接受序贯内分泌治疗5年后的患者继续延长内分泌治疗,对于HR阳性的患者,持续面临疾病复发的风险,术后5-10年复发风险为5%;术后10-20年,淋巴结阴性和阳性患者的复发风险分别为2%和3%。然而,目前关于接受序贯内分泌治疗满5年的患者,继续延长AI的使用时间能否给患者带来获益,缺乏研究证据。基于这一问题,进行了DATA研究,这是一项前瞻性的随机开放多中心III期研究,在HR阳性的绝经后早期乳腺癌患者中,评估2-3年辅助他莫昔芬治疗后,序贯不同时长的AI治疗。
DATA研究是一项开放的多中心研究,在荷兰79个国家进行。研究入组绝经后的HR阳性的早期乳腺癌,患者已经完成了2-3年辅助他莫昔芬治疗,且未发现疾病复发。允许患者在围术期接受过化疗和/或放疗,研究入组时,曲妥珠单抗尚未纳入标准治疗。其他排除标准包括:在本次乳腺癌诊断前10年内有乳腺癌病史,5年内有其他浸润性恶性肿瘤病史(皮肤基底部鳞癌或宫颈原位癌除外)。
患者在2-3年辅助他莫昔芬治疗后,1:1随机分配至接受6年(延长内分泌治疗组)或3年(对照组)辅助阿那曲唑治疗。分层因素包括:淋巴结状态(阳性 vs 阴性),HR状态(ER和PR均为阳性 vs ER阳性PR阴性 vs ER阴性PR阳性),HER2状态(阳性 vs 阴性 vs 状态未知),他莫昔芬治疗时长(<=2.5年 vs >2.5年)。
主要研究终点为适应性的DFS,即随机3年后的DFS(因为两组患者均接受了3年的阿那曲唑治疗)。定义为疾病进展的终点事件包括:非浸润性和浸润性乳腺癌复发(局部,区域或远处),第二原发非浸润性和浸润性乳腺癌和其他恶性肿瘤(皮肤基底癌或鳞癌,宫颈原位癌除外),或任意原因的死亡。次要研究终点为适应性的OS,即随机3年后的OS,第二原发乳腺癌发生率和不良事件。
2006年6月至2009年8月,研究共筛查了1912例患者,其中955例分配至3年阿那曲唑组,957例分配至6年阿那曲唑组。其中1860例(6年组931例,3年组929例)患者为合格的入组人群,见下图1.
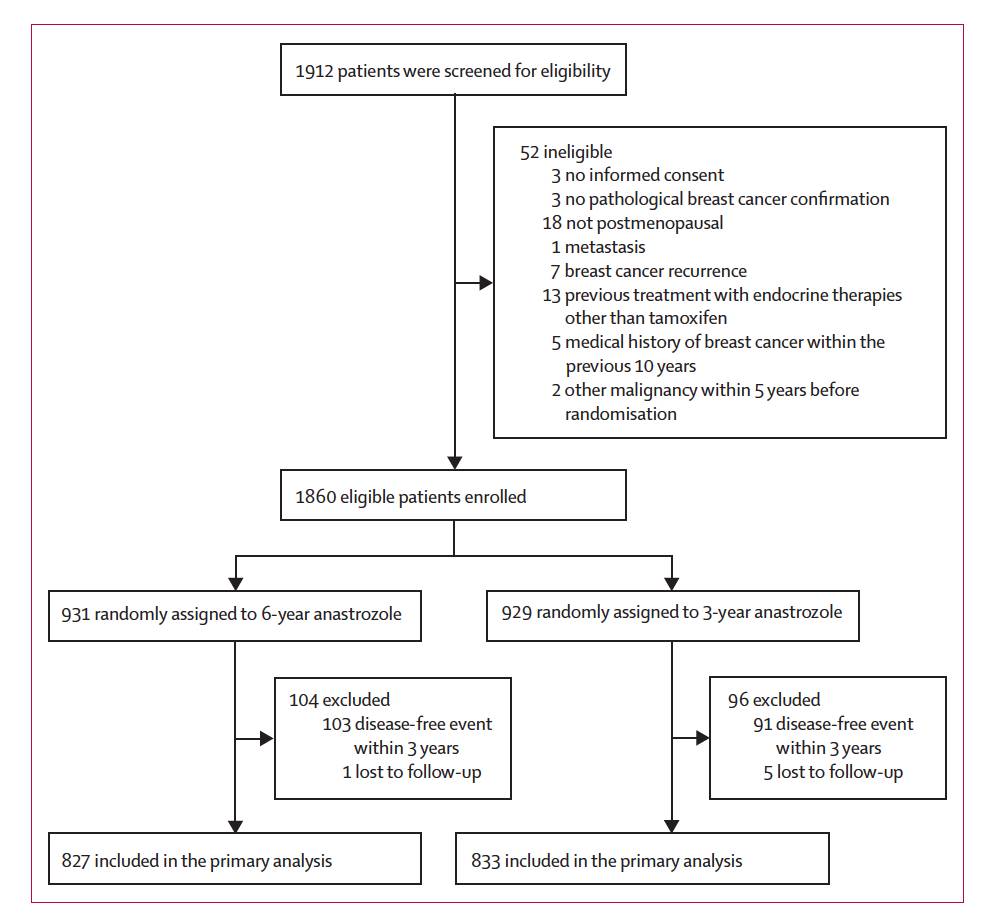
图1. 研究入组流程图
本次汇报该研究中随机3年后疾病没有进展的1660例患者的研究数据。两组患者的基线特征均衡。6年组和3年组随机时的年龄分别为57.7岁和57.6岁,接受他莫昔芬治疗的中位时长都分别为2.3年。
最后随访日期为2016年7月14日,适应性的中位随机时间为4.2年。6年组和3年组,3年适应性的DFS率分别为90.7%和88.9%;5年适应性的DFS率分别为83.1%和79.4%,HR=0.79(95%CI:0.62-1.02;P=0.066),见下图2A。图2B和图2C分别分析了不同分层因素(淋巴结状态和ER/PR状态)患者的DFS比较。进一步对比两组患者的5年适应性OS率,6年组和3年组分别为90.8%和90.4%,HR=0.91;95%CI:0.65-1.29;P=0.60,见图2D。
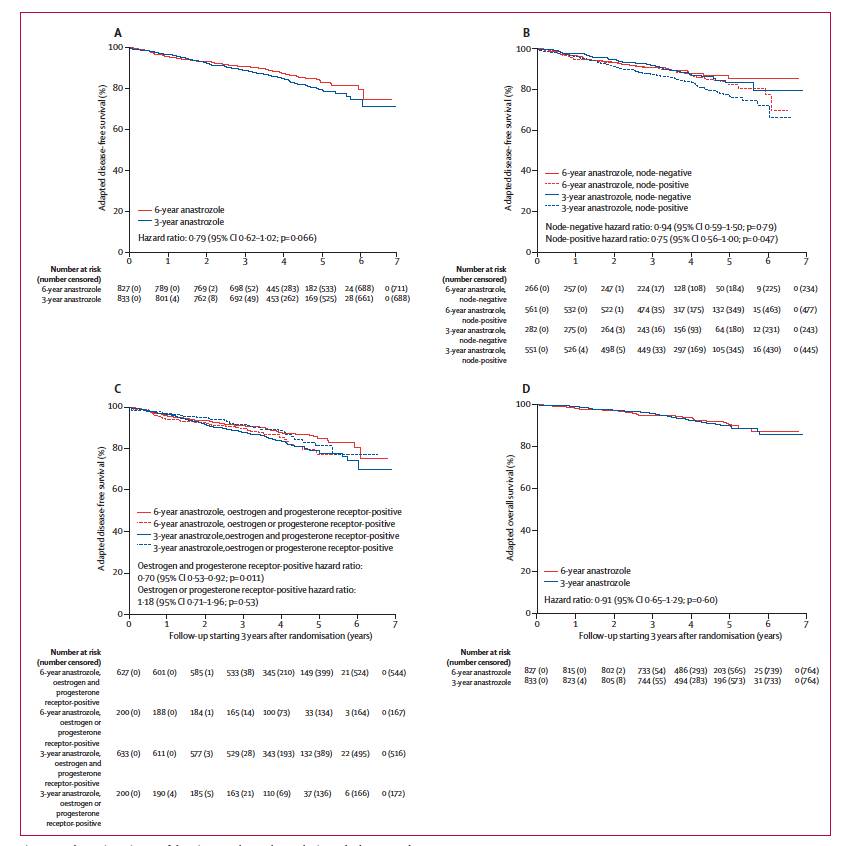
图2. 主要和次要研究终点和亚组分析。
探索性的分析提示,无论患者既往是否接受过化疗,在ER和PR均阳性且淋巴结阳性的患者中(n=849),6年组对比3年组,观察到5年适应性OS率的改善,分别为84.4%和76.2%,HR=0.64;P=0.0075。此外,在大肿瘤(>=T2,N=429),也观察到OS的改善,5年适应性OS率分别为82.7%和69.2%;HR=0.53;P=0.0031.
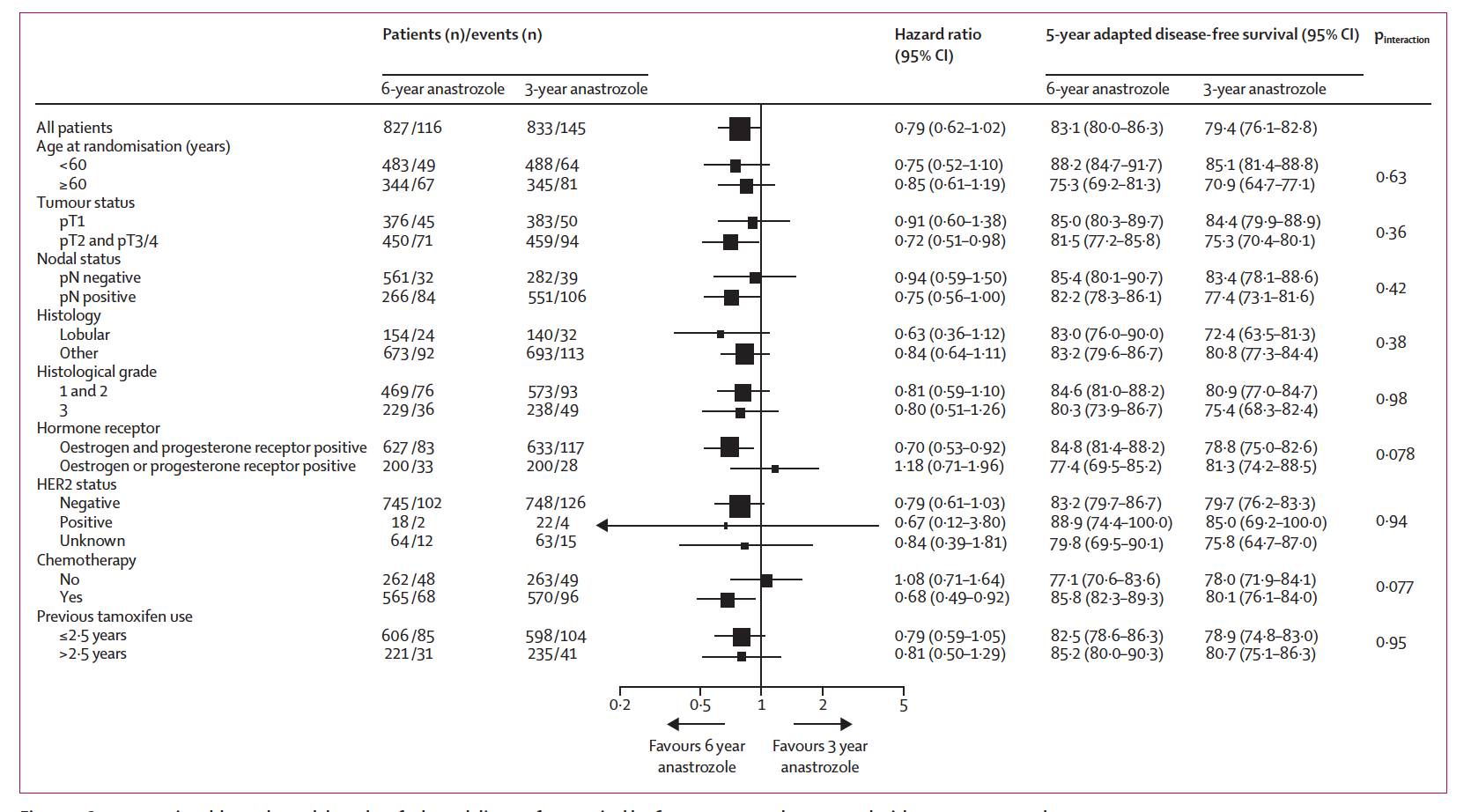
图3. DFS的亚组分析
第二原发乳腺癌发病风险对比:适应性的5年累积第二原发乳腺癌发病率,6年组和3年组分别为1.5%(95%CI:0.5-2.4)和3.3%(95%CI:1.7-4.9),HR=0.50;95%CI:0.23-1.07,P=0.068,如下图4,两组没有统计学差异。
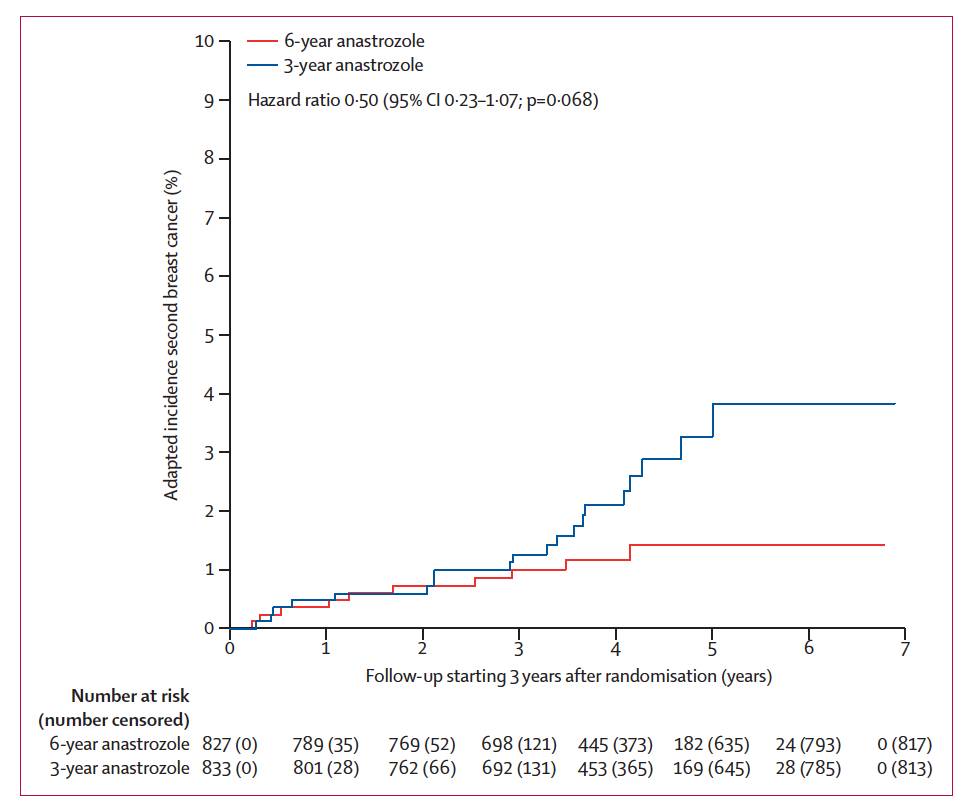
图4. 第二原发乳腺癌的累积发病风险对比
安全性对比:与预期一致,在随机后的头3年,两组患者的不良事件发生率相当,但从整个观察期来看(随机后0-6年),6年组的关节痛或肌肉痛发生率更高,分别为58% vs 53%;骨质疏松的发生率也更高,分别为21% vs 16%。但3-4度的关节痛或肌肉痛发生率,两组相当,分别为9%和9%;3-4度的骨质疏松的发生率,两组也相当,分别为2%和1%。在心血管不良事件发生率上,两组也相当。多数的不良事件为1-2度,未观察到致死性的毒性。
DATA研究在绝经后HR阳性的早期乳腺癌患者中,探索了在完成5年序贯辅助内分泌治疗后,继续延长内分泌治疗能否改善患者的生存结局。结果显示,在总体人群中,完成5年序贯内分泌治疗后,继续使用阿那曲唑3年不会显著改善患者的DFS和OS。然而,亚组分析提示,对于部分特定人群,延长内分泌治疗确实能带来生存获益,如本研究所示,ER和PR均为阳性的患者。基于这一研究结果,目前不推荐所有绝经后HR阳性的患者,在完成5年序贯内分泌治疗后,继续延长AI治疗,但部分患者可能从延长治疗中获益。此外,研究者认为,随着治疗时间的延长,患者用药的依从性下降,因此,在推荐延长AI治疗时,临床医生应该充分考量潜在的获益和风险。
Extended adjuvant aromatase inhibition after sequential endocrine therapy (DATA): a randomised, phase 3 trial. Lancet Oncol 2017; 18: 1502–11.
28个肿瘤相关临床试验招募患者
点击下方图片即可查看详情


















