单克隆
抗体
药物
被誉为“
生物
导弹”,是国际上公认的科技含量最高的生物药品之一。同时,这也是全球最受欢迎的药物之一。这一领域诞生了多种重磅药物,比如第一个治疗肿瘤的嵌合抗体Rituxan,大名鼎鼎的类风湿关节炎药物。
Adalimumab单抗,2014年全球销量NO.1 Avastin,以及百时美施贵宝和默沙东家的宝贝Opdivo和Keytruda。
除了热门的PD-1、PD-L1,单克隆抗体家族还有一位冉冉升起的新星——双特异抗体。
双
特异性
抗体是指含有两种特异性抗原结合位点的人工抗体,可以同时与靶细胞和功能细胞进行相互作用,进而增强对肿瘤细胞的杀伤功能。与普通抗体相比,其效果可能达到普通单抗的100-1000倍,剂量可降到原来1/2000。
全球首个获批的双特异性抗体药物是Fresenius的Removab,被用于治疗恶性腹水。但个产品到目前为止并没有取得FDA的批准,仅仅是在欧盟委员会批准下在欧洲范围内销售。唯一一个FDA批准的双特异性抗体药物则是安进的Blinatumomab,该药物被批准用于治疗费城染色体阴性(Ph-)复发性/难治性前体B细胞急性淋巴细胞白血病。
罗氏在2014年以4.89亿收购了奥地利生物技术
公司
Dutalys,获得其此外,强生、赛诺菲等制药巨头正在不断加码。中泰证券2016年的一份报告中便指出,自2014年起,罗氏、强生、赛诺菲、辉瑞等制药巨头在该领域的总投资额已接近40亿美元。
早在30多年前,双特异性抗体的该你那就被设计出来了,但知道几年前才解决其中的一些技术挑战,使得双特异性抗体能够进入到临床。
技术难点
技术平台则是关键。罗氏曾花4.89亿美元收购了奥地利的一家生物技术公司Dutalys,目的就是获得这家公司的双特异性抗体平台DutaMab,不从其自身CrossMab系统的缺陷。
目前全球正在使用的技术平台超过30个,其中,MacroGenics公司的DART平台被强生、辉瑞、施维雅、武田等多家制药巨头采用。目前拥有在研项目做多的公司——安进所使用的则收购了Micromet,获得其技术平台BiTE的所有权。
国内的技术平台有4个,包括键能隆的iTAB、天演药业的动态谨遵抗体技术DPL、友芝友的Ybody、以及岸迈生物的FIT-lg。其中,FIT-lg平台也通过技术授权的方式被信达生物使用。值得一提的是,岸迈生物创始人吴辰冰也是雅培DVD-IgG技术平台的发明人。
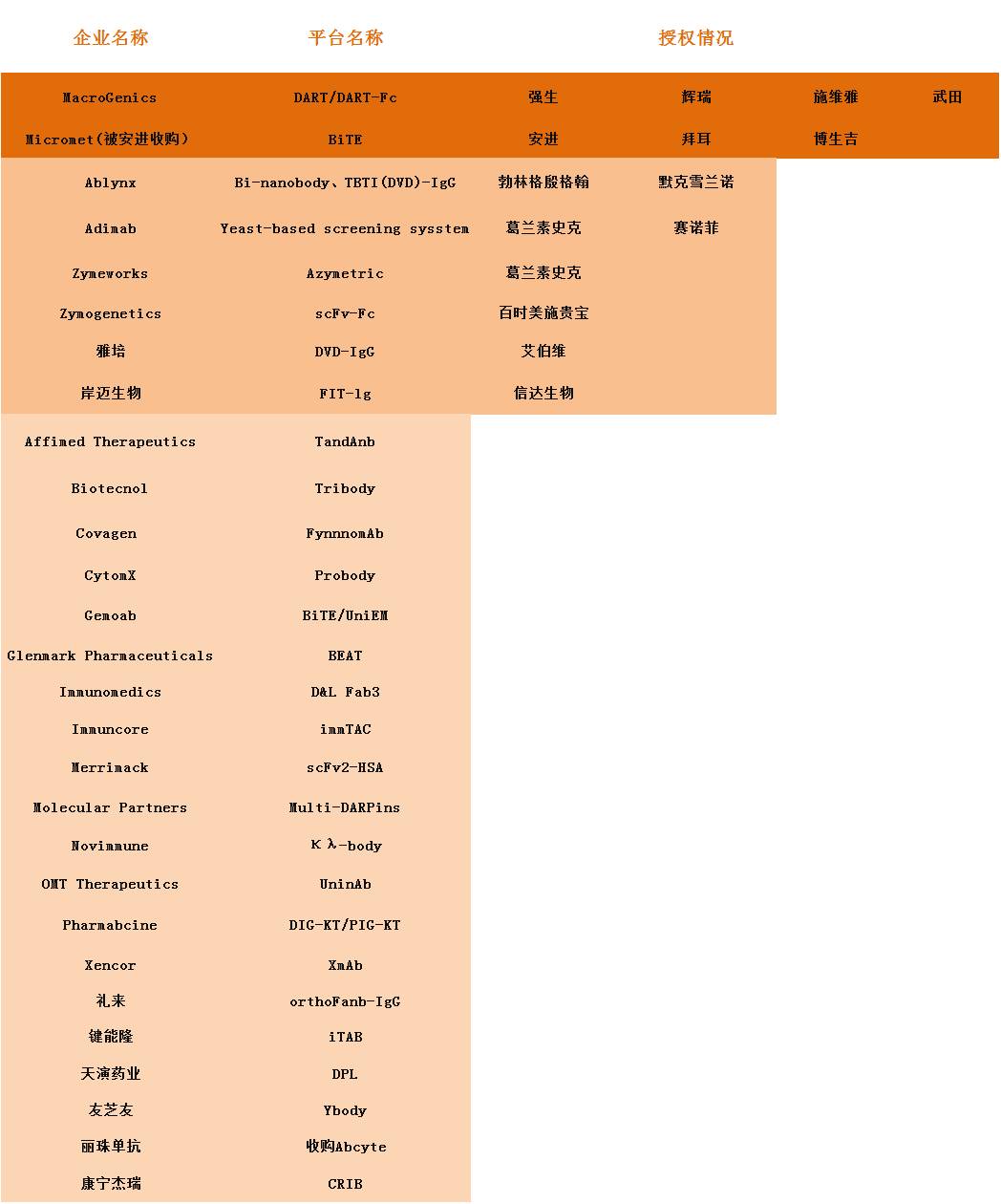
技术平台及授权情况
临床看点
截止到2017年9月,全球范围内共有68项正在进行的双特异性抗体临床试验,其中美国就有31个项目。

这些项目中,几乎所有的研究都处于临床1期和2期,并且大部分都处于招募或者已经完成的状态。目前已经完成的项目共有25个,但公布结果的只有10个。
其中,安进、芭芭拉.安卡马纳司癌症中心的在研项目最多,各7个;另外罗氏、MacroGenics各三个;强生、默克各有两个在研项目;辉瑞和礼来也各有1个项目在临床试验中。
无疑,安进是双特异抗体市场最大的玩家,罗氏的研发的在研项目不是最多,但其旗下的ACE-910一度是最被外界认为最有希望的药物分子。
安进生物的一项临床试验正处于3期临床试验,旨在研究Blinatumomab在白血病和急性淋巴细胞疾病中的疗效,将通过与传统的化疗药物对比,验证Blinatumomab的安全性和有效性。目前,该项目正处于招募中,预计将在2022年完成。
Neovii的一项研究项目是2期和3期临床合并进行。该项目旨在研究Catumaxomab (Removab)对EpCam阳性肿瘤(如胃癌、结肠癌、乳腺癌等)的治疗效果。项目与2004年启动,2009年完成,但目前尚未公布实验结果。
这些全球巨头之外,MacroGenics同样是双抗领域的实力派。
2014年12月,强生为了获得MacroGenics的双特异抗体药物全球授权,与MacroGenics达成了7亿美元的授权协议(其中预付款1.25亿美元,阶段性付款5.75亿美元)。
就在于强生达成协议的前几周,武田也与该生物技术公司签署了价值5亿美元的交易,获得MacroGenics 临床前试验性抗体 MGD011。支付了5000万美元授权费,另将支付7500万美元以每股39美元的价格收购MacroGenics的股份。根据当时的报道,MacroGenics价股因这个消息飙升16%。
这家公司凭借技术平台和早期分子的授权,与几乎所有布局双特异性抗体的制药巨头都达成了授权合作。强生、武田、辉瑞、施维雅使用技术平台均来自MacroGenics,默沙东在2015年与MacroGenics达成了与Keytruda(默沙东的PD-L1抑制剂)联合用药协议。
国内企业
中国目前在进行的临床试验只有一个,是本康生物制药与解放军302医院合作的基于靶向活化CIK细胞治疗和双特异性抗体治疗对进展期肝癌的随机、对照临床研究。目前该研究正处于2期临床试验招募中。
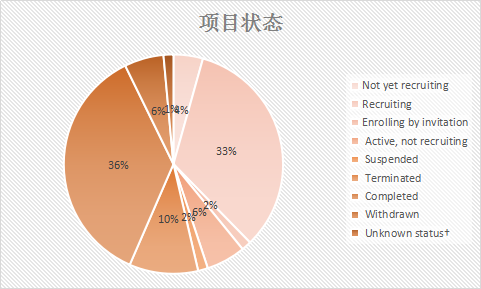
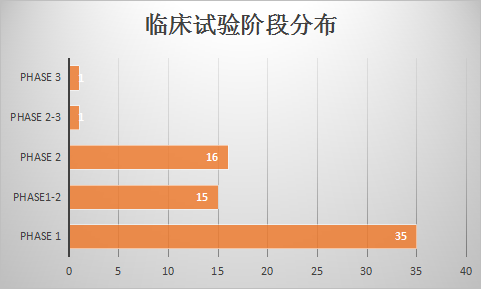
以上是从clinicaltrials.gov获得的数据,即在美国登记注册的实验情况。动脉网又在中国药物临床试验登记与信息公示平台上查找了双特异性抗体相关信息,目前尚未找到在国内注册的临床试验项目。
据动脉网不完全统计,国内目前从事双特异性抗体研发的企业共有15家,其中包含两家上市公司。除了丽珠、恒瑞等上市公司,以及康宁杰瑞、信达、君实等深耕抗体领域的企业外,一些年轻的创业公司也值得关注。
友芝友
这些企业中,友芝友拥有的药物品种最多,一共有8个,其中针对乳腺癌的HER2/CD3抗体已经完成成药性研究和中试工艺研发。
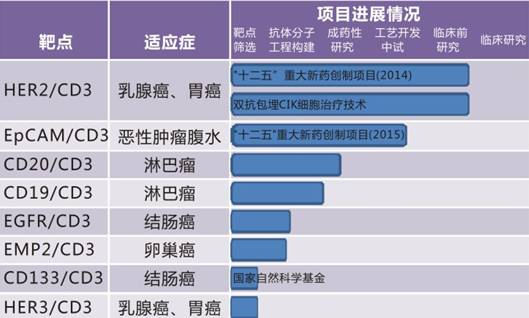
图片来自友芝友官网
友芝友是一家专门从事生物医药自主创新研发的高科技企业。其母公司友芝友医疗与华中科技大学联合组建了友芝友个体化医学研究中心,由我国遗传药理学和药物基因组学领军人、个体化医学倡导者、中国工程院院士周宏灏教授担任负责人。
公司副董事长周鹏飞是加拿大麦克马斯特大学分子免疫学博士,并在斯坦福医学院肿瘤中心从事过博士后研究工作。周鹏飞是国内双特异性抗体药物研发的领军人物,拥有和曹国15年的免疫治疗、抗体药物研发、以及团队管理经验,曾担任中美冠科生物技术(Crown Bioscience Inc.)免疫学高级总监,辉瑞-冠科亚洲肿瘤研发中心执行总监,深圳第二人民医院外科主治医师。
另外,公司副总裁易继祖、抗体研发总监张建东也都拥有10年以上的生物医药经验,在国内外顶级科研院校、医药企业进行抗体研究和开发工作。
光从团队上讲,友芝友是一个由院士领衔,制药巨头研发高管参与的国际化背景团队。无论是产品数量还是研发进度上,友芝友都走在国内双特异性抗体研发的前列。
公司于2016年5月完成了由磐霖资本(磐霖资本股权投资基金)领投的A轮融资,并与跟投方珅奥基医药达成全面合作意向。
根据最新消息,友芝友自主开发的“注射用重组抗HER2和CD3人源化双特异性抗体” (项目编号“M802”),已经于2017年9月29日获得国家食品药品监督管理总局(CFDA)颁发的临床试验批件(批件号:2017L04744)。这是首例在我国进入临床开发阶段的自主创新双特异性抗体,对我国整个医药创新行业而言都具有里程碑意义。
本康生物
本康生物成立于2015年,主要从事生物制药和细胞治疗创新工具和技术解决方案的开发。
公司技术团队中不乏出自安进、拜耳这些巨头公司的研发人才,依托公司在蛋白质工程领域多年的研究经验,公司储备了大量有望改造和提升细胞治疗技术的工具,涵盖双特异性抗体药物开发、细胞培养方案及基于磁珠的细胞分离技术以及细胞检测等诸多方面。
目前一共有5个双特异性抗体药物,其中有三个正在展开临床试验,除了一项是在美国申报以外,其他两项试验尚未公布申报地点。
天演药业
天演药业成立于2012年,致力于新一代抗体技术的开发。公司联合创始人罗培志是在抗体开发和抗体工程方面有着丰富专业知识的连续创业者。他曾合作创办了Abmaxis,这家公司于2006年被默沙东制药公司(Merck)收购,并购之后罗博士担任默沙东制药公司(Merck)的生物药总监兼抗体工程负责人。在这之前,他曾在Xencor担任首席科学家。
此外,药明康德董事长李革也是公司董事之一。
天演药业分别于2014年12月和2016年一月完成了两轮融资,其中A轮融资800万美元、B轮融资2亿人民币,投资方包括富达亚洲、药明康德。
复宏汉霖
在生物制药领域,复宏汉霖应该算是“后起之秀”。这家公司由复星医药与美国科学家团队于2009年12月合资组建,公司主要致力于应用前沿技术进行单克隆抗体生物类似药、生物改良药以及创新单抗的研发及产业化。依托中美两地的资源,复宏汉霖在短短几年间就跻身国内抗体研发企业前列。














