火灾引发的
烟雾吸入性急性肺损伤(SI-ALI)
是火灾事故中致死率极高的并发症,其病理机制复杂且缺乏针对性疗法。传统动物模型因物种差异难以模拟人体反应,而单细胞模型无法还原肺部多细胞互作的动态过程。此外,火灾中现代合成材料燃烧产生的混合毒气(如氰化氢、苯类)成分复杂,现有烟雾生成技术稳定性不足,导致研究重复性差。
因此,如何
构建精准、可重复的人类肺损伤模型
,并筛选有效药物,成为亟待解决的科学难题。

鉴于此,来自
海军军医大学的万小健
等团队开发了
一种基于肺芯片(Lung-on-a-Chip)和类器官的整合模型
。该模型通过精准控制现代非金属材料燃烧烟雾的生成,首次在体外模拟了火灾烟雾吸入导致的肺泡-毛细血管屏障损伤、氧化应激及炎症级联反应,并筛选出维生素C联合布地奈德的潜在治疗方案。
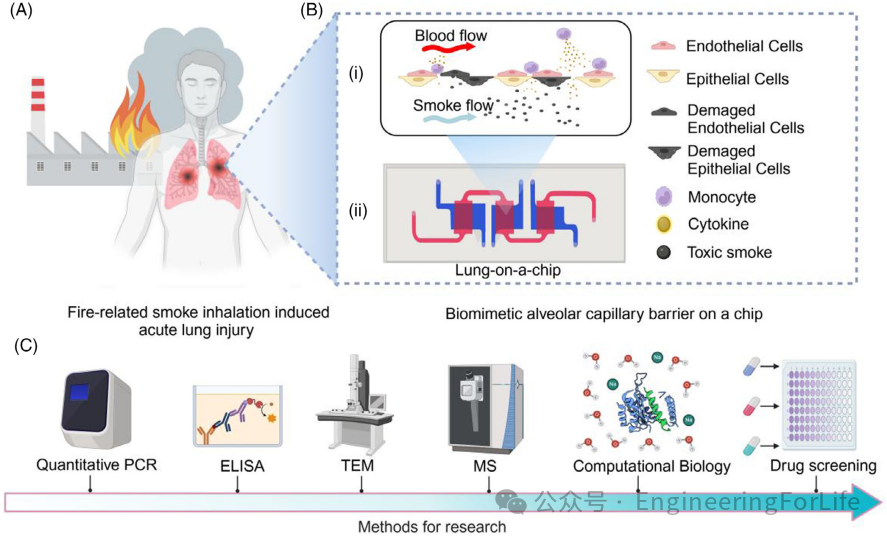
本文要点:
(1)多技术融合构建高仿真肺损伤模型:
团队首次将肺芯片与类器官技术结合,优化芯片重力驱动设计,模拟肺泡动态屏障。通过傅里叶红外光谱实时监测烟雾成分,精确复现现代建材燃烧毒气(如聚酰亚胺泡沫、橡胶),解决了传统烟雾模型稳定性差的问题。该模型成功再现了线粒体损伤、免疫细胞黏附等关键病理特征,为机制研究提供可靠平台。
(2)发现COMT等新型分子靶点:
通过蛋白质组学分析,团队鉴定出COMT(儿茶酚-O-甲基转移酶)和NIT1(腈水解酶1)等关键分子,并揭示其在氧化应激和代谢紊乱中的核心作用。分子对接筛选出雷托巴胺等FDA已批准药物的潜在疗效,为老药新用提供新方向。
(3)临床级药物组合验证:
利用芯片模型,团队首次验证了静脉注射维生素C联合雾化布地奈德的协同疗效。该方案显著降低炎症因子(IL-6、TNF-α)和细胞凋亡,且通过人源肺类器官模型进一步确认其安全性,为临床转化奠定实验基础。
本研究
通过肺芯片与类器官技术的创新整合
,突破了传统模型的局限性,为火灾烟雾肺损伤的机制解析和药物开发提供了高效平台。
未来,该技术可扩展至其他吸入性损伤(如化工毒气、PM2.5)的研究,并推动个性化治疗方案的筛选。此外,COMT等新靶点的发现为开发特异性抑制剂或调节剂开辟了可能。
参考资料:
https://doi.org/10.1002/VIW.20240114
来源:
EngineeringForLife
声明:仅代表作者个人观点,用于研究用途,作者水平有限,如有不科学之处,请在下方留言指正!






