正文


2016年,欧洲药品管理局(EMA)继续推行了其在2013年发起的基本组织机构改革,以更好地支持EMA保护公共健康的使命,强化欧洲药品监管体系的协调性。
新架构使EMA对药品生命周期的监管更为紧密:有专职负责支持医药研发企业的部门,专职负责药品科学审评和程序管理的部门,还有负责监管药品的部门(包括药物警戒和检查)。
业务方面,EMA优化了人用药品审评流程的模式,其基础是努力精简内部流程,将重点放在增加价值的活动上。在新的审评模式下,审评流程负责人和流程助理负责特定药品申请,实行类似美国的项目管理模式。该模式有望改善对特定药品监管活动的协调,特别是同一产品并行处理审评、检查等多个监管程序时更有效率。
EMA还通过组织定期的平台会议和网络研讨会,增加与行业利益相关方的互动。同时进行了一项调查,以获得有关其各种上市后批准程序的反馈意见,并综合反馈意见进行了审评流程方面的改进,主要目的是简化流程并推出新的监管指南,以支持申请人对药品全生命周期的管理。EMA 2016年的工作核心主要包括:药品审评;为创新药物研发提供支持;监测药品在真实世界中的风险获益等。

去年, EMA共批准81个人用药品上市,其中27个为新活性物质,数量上低于2015年的39个和2014年的40个。批准的产品中,包括小分子药物、抗体、血液制品、细胞产品及疫苗等。EMA批准的产品大部分都是FDA 2016年或2015年批准的品种,并且欧盟批准了2个前沿性的细胞治疗产品,FDA尚未批准上市。
GS公司的strimvelis是欧盟批准的第2个基因治疗产品,用于治疗腺苷脱氨酶(ADA)缺陷所造成的严重免疫缺陷疾病。EMA批准的另1个细胞治疗产品是MolMed公司进行基因改造后的外源T细胞zalmoxis,用于造血干细胞移植后免疫系统的重建。
EMA率先批准了礼来的JAK抑制剂baricitinib,用于治疗中重度类风湿性关节炎。2017年4月,美国FDA认为该药需提供补充临床证据,尚未批准该药上市。2个在2016年被FDA拒绝批准的新药,在EMA获批(分别是Amicus公司的治疗法布里病的药物migalastat,以及安进公司的用于治疗慢性肾炎所致的继发性高甲状旁腺机能亢进etelcalcetide)。
所有获得EMA批准的药品中,有近50%均在研发阶段通过沟通获得EMA的科学建议(Scientific advice)。科学建议是EMA药品审评的关键工具,帮助申请人收集高质量的风险-效益数据和提高药品研发成功率,以支持药品的上市许可申请。
与美国FDA类似,EMA正加快批准那些尚未满足临床治疗需求的新药上市。2016年,超过1/3的药品使用多于至少一种优先审评工具批准,例如平行EMA/HTA建议、有条件批准等。
统计发现,2016年,7个新药通过加速审评通道上市(该加速审评时限为150天,而标准审评时限是210天)。8个新药通过“有条件批准(conditional marketing authorisation)”通道上市,即批准时依据的临床资料尚不完整,上市后的药品应继续获取完整临床数据。
欧盟的孤儿药认定申请数量也在不断增加。
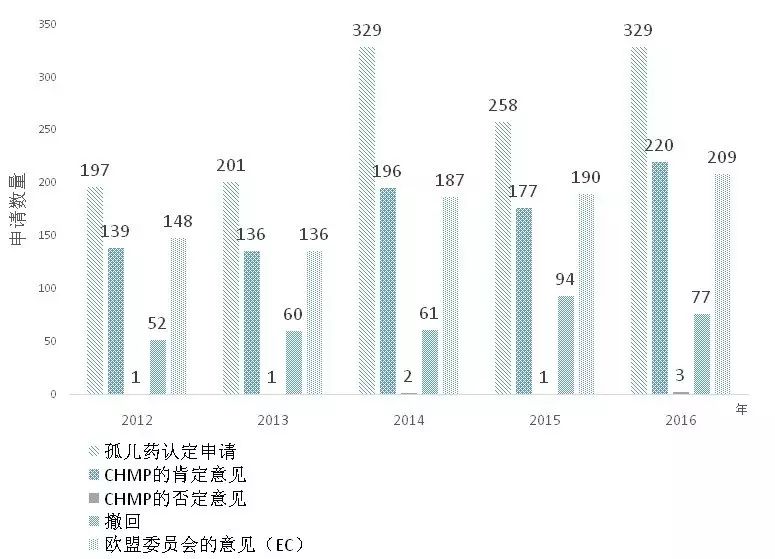
其中,EMA的孤儿药认定申请在2016年达到峰值329件,2015年仅有258件(如图1所示)。EMA还与美、日监管合作伙伴就孤儿药监管开展合作,去年提交到EMA的孤儿药认定申请中,有将近1/3平行提交到另一监管机构。
EMA对集中审批药品的标准审评时限为210天。相比之下,美国的标准审评为10个月,优先审评为6个月。EMA评估期间,可能会发现申请的问题,需要企业进一步的信息或澄清,此时需要停止审评时钟,以便企业有时间回复。然后将EMA的CHMP的意见转交欧盟委员会(EC),由欧盟委员会收到CHMP意见后的67天内决定是否授予上市许可。
梳理发现,2016年初始上市许可的实际审评时限与最近几年相比仍保持稳定。通过EMA集中程序药品审评的平均天数为:CHMP评审为199天,EMA观察期11天,企业时钟停止156天,最终EC决策过程52天。
出于安全原因撤销上市的通知数量也略有下降,从2014年的132项到2015年的160项,下降到2016年的118项。
图1 欧盟2012-2016年孤儿药认定过程
笔者留意到,EMA在2016年推出了一系列促进药物研发的举措,与下属科学委员会和各工作小组在药物早期研发和试验阶段给予申请人建议,以提高患者急需药品的可及性。
2016年3月,EMA发布《申请人寻求进入PRIME计划指南》设置“优先药物(PRIority Medicines,PRIME)”通道,主要是促进医疗需求尚未满足的疾病,治疗细菌耐药、重大疫情(如埃博拉)等药物的研发。PRIME并没有引进新的法规条款,而是建立在EU已有的法规框架上。其目的是协调EU中现有的法规工具和注册程序,以促进未被满足临床需求的药物开发。其主要依托的是两项法规Reg. (EC)726/2004和Reg.(EC)507/2006。
在药物开发初期,审批人员就与进入通道的申请人及时频繁的沟通。EMA称,通过在研发各阶段提供反馈,帮助申请人拟定恰当的临床试验方案,招募合适的受试者,最终提高临床试验成功率。
进入PRIME通道,申请人提交一份申请说明药物符合尚未满足的医疗需求的条件,包括能够为患者带来重大治疗优势的证据说明,该药品申请被授予PRIME资格后,EMA将会委派一位来自EMA人用药品委员会(CHMP)的专员,与申请人沟通提交上市申请前的一切技术问题。如果药物同时被认定为先进疗法(Advanced Therapies)治疗药物,EMA则会委派来自先进治疗药物委员会(CAT)的成员参与沟通。EMA还会组织CHMP/CAT专员、EMA多学科专家小组及相关方召开启动会议,为药物的总体研发方案和注册策略提供指导,并在提交上市申请时与申请人确认获得加速审评的可能性。
2016年,EMA共计收到84件PRIME申请,一半来自中小型企业。15个药品申请最终获得PRIME认定,包括6个肿瘤治疗药(共17个药品申请)。10个药品被同时授予先进疗法治疗药品资格。PRIME申请大多数为癌症治疗药物,包括基于遗传修饰的T细胞(CAR T细胞)的创新型免疫治疗药物。从申请数据量看,PRIME政策备受业界关注。由于PRIME计划旨在用于最急需的药物,迄今为止,只有相对较少的药品被该计划接受。
此外,先进疗法药品是EMA的另一亮点。2016年,有两个先进疗法药品获批,分别为GSK的基因治疗药Strimvelis,用于治疗重度联合免疫缺陷症;意大利Molmed公司的Zalmoxis,用于接受单倍体造血干细胞移植患者的转基因T细胞的细胞治疗。
从项目设计初衷看,PRIME目标定位于最早期阶段的研发工作。目前进入PRIME的第一批候选药品中只有32%处于Ⅲ期临床。
EMA对科研机构及中小规模企业提供额外的帮助,相比大型制药公司,前者往往缺乏药物研发经验。对于已获得部分积极的临床前数据的科研机构及中小企业,EMA会设定更早进入PRIME的时间节点。截至2016年12月,EMA只批准了一家中小企业Albireo公司的回肠胆汁酸转运体抑制剂A4250进入PRIME,用于治疗进行性家族性肝内胆汁淤积症。截至2017年5月25日,EMA已批准23个药品进入PRIME。
EMA之所以将关注重点集中于先进疗法药品,是因为这些药物通常为罕见病用药,在临床试验中会面临独特的挑战。繁冗的CMC要求往往会拖延甚至摧毁某些有潜力的候选药物的申请进程。更复杂的是,先进疗法药品不得不面临不同监管机构的审查,各自有独特的监管要求。通过早期介入和提供支持,监管机构将会深入了解这类公司所面临的问题,从而有可能帮助其克服困难,推进研发进程。这也是PRIME项目的吸引力之一。
适应性路径(adaptive pathways),是指一种有前景的药物以渐进的方式批准用于患者的结构化方法。该药物可能最初被批准用于可能受益最大的小部分患者群体,随着时间的推移收集其他使用证据。适应性路径是与医学和数据生成相关的监管科学概念,是EMA努力促进患者及时获得新药的重要举措,可以让有需求的患者较早获得治疗药物。
适应性路径依据的是公认不确定性条件下的渐进式学习路径,其中涉及数据采集和监管评估的迭代阶段。其基本原则具体有3点:
第一,迭代开发,即意味着:从有限的患者人群开始,逐步审评,然后扩大到更广泛的患者人群;根据评估可用于预测重要临床结果的早期数据(替代终点)进行有条件批准后,确认产品的利益-风险平衡;第二,通过真实世界的药品使用来收集补充临床试验数据和证据;第三,患者和卫生技术评估机构早期参与讨论药品的开发。
适应性路径主要适用于医疗需求较高的区域,这些区域难以通过传统路线收集数据,大型临床试验又会无必要地使不太可能受益的患者暴露于该药物。
适应性路径建立在现有欧盟法律框架内已经实施的监管流程基础之上。包括科学咨询、同情使用、有条件的批准、患者登记和其他药物警戒工具,允许收集真实世界数据和制定每种药物的风险管理计划。适应性路径不会改变风险-效益的评估标准,也不改变获得上市许可的效益-风险平衡的要求。
EMA于2014年3月-2016年8月间开展了试点项目,以探索适应性路径概念与正在开发的药物的实际影响。试点项目为利益相关方(包括患者和卫生技术评估机构)之间的非正式对话提供了框架。
试点期间,EMA收到62份申请,并选择性召开了18项面对面会议申请。试点结束时,6名申请人已收到EMA和HTA机构的平行建议。2016年12月,EMA还与欧盟委员会共同举办了试点项目的经验研讨会。
适应性路径涉及从研发早期开始,与利益相关方合作,积极主动规划获取证据的最佳方式。同时,它能够确定生成证据最合适的工具,这意味着将更多地利用观察(真实世界)数据支持随机对照试验,尤其是在随机对照试验不够充足的情况下。上述研讨会解决了适应性路径试点发现的重要问题,包括如何更好地满足患者的需求,如何生成合适的数据辅助药物审评,以及如何确保欧盟药品审评的高标准。EMA充分考虑了利益相关方的不同观点,并将试点的经验与利益相关方的反馈整合到现有的科学建议机制中,以汇集卫生技术评估机构(HTA)、患者以及医务人员三方意见。有兴趣遵循适应性路径的医药开发商,可向EMA提交建议书,EMA将定期更新获取的经验,并继续通过各种论坛与利益相关方交流。
2016年5月,EMA组织了一次多方利益相关方专家会议,探讨促进欧洲先进疗法药物(advanced therapy medicinal products,ATMPs)的开发和扩大患者对新疗法可及性的可能方式。
ATMPs包括基因治疗、组织工程药物(tissue engineered products)和体细胞治疗,这些药品可能会改变大多数病症的治疗,尤其是在有证据显示传统治疗方法无法有效治疗的疾病领域。然而,自2008年欧盟关于ATMPs的法规指令Regulation (EC) No 1394/2007、Directive 2001/83/EC生效以来,只有8个ATMPs通过审批。同时,ATMPs的临床试验代表迅速增长的新兴领域,须通过一致且合适的监管环境以支持更好的创新。
本次研讨重点关注:促进研究与开发;优化ATMPs的监管流程;从医院临床豁免转移到上市许可;改善资金、投资以及患者可及性。研讨后,EMA、科学委员会以及欧盟委员会和多个成员国监管部门一起制定了行动计划,该计划将于2017年内发布。
(本文作者来自沈阳药科大学国际食品药品政策与法律研究中心)
■编辑 刘莉
★更多深度报道见《医药经济报》~ 















