BioArt按
:
日前,
The FASEB journal
在线发表了来自中国华南农业大学动物营养调控实验室
束刚
教授和
江青艳
教授课题组题为“Alpha-ketoglutarate prevents skeletal muscle protein degradation and muscle atrophy through PHD3/ADRB2 pathway”的研究论文。该论文发现α-酮戊二酸作为运动后产生的重要代谢中间产物,能有效缓解因皮质酮及抗萎缩蛋白质缺失诱导的肌肉萎缩及蛋白质降解,并恢复肌肉萎缩模型动物的运动能力和肌肉力量。研究发现,α-酮戊二酸可以通过抑制脯氨羟化酶3,减少β2-肾上腺素能受体羟基化和泛素化降解水平,从而缓解肌肉萎缩。该项工作不仅首次揭示了α-酮戊二酸在缓解肌肉萎缩方面的新机制,也为治疗肌肉萎缩及肌无力的药物研发提供了新的靶点。

论文解读:
肌肉萎缩
是一种因肌肉营养代谢不良而导致的肌肉功能障碍,肌肉无力,蛋白质降解增加的代谢疾病,给患者带来生命威胁。长期卧床、固定肢体,以及癌症和艾滋病等长期消耗性疾病均可导致不同程度的肌肉萎缩。肌肉萎缩病因复杂多样,目前临床上除运动辅助治疗外,还缺乏有效的治疗药物。
α-酮戊二酸
(α-ketoglutaric acid,
AKG
)是三羧酸循环的一种关键代谢中间产物。此前有研究报道,运动可显著增加血液AKG水平【1】。而且,AKG也被认为是一种重要的活性代谢中间产物,在干细胞发育【2,3】、抗衰老【4】、抗癌【5,6】和调节能量代谢[7]等方面均具有重要作用,但AKG在改善和治疗动物肌肉萎缩的功能及相关作用机制尚不清楚。
此前,华南农业大学动物营养调控实验室
束刚
教授和
江青艳
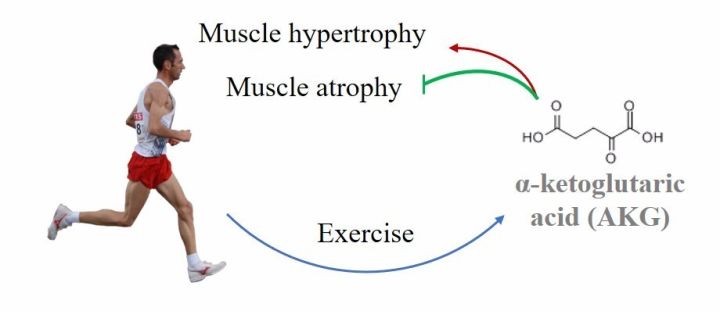
教授的课题组已经发现,外源添加AKG可显著提高正常小鼠的运动能力,激活蛋白质合成相关信号通路,增加肌肉蛋白质合成增加【8】。在此基础上,本文进一步研究发现,AKG可显著逆转糖皮质激素诱导的小鼠肌肉蛋白质降解,并能改善杜氏肌肉萎缩模型小鼠的肌肉萎缩症状,提高小鼠的肌肉力量和运动能力。该结果说明
AKG可能是介导运动治疗肌肉萎缩的重要中间分子,而且也有望研制成一种新型运动替代物用于改善人类的运动能力
(
下
图
)。
脯氨酸羟化酶
(Proline hydroxylase, PHD)是一种依赖氧气和氧化代谢中间产物的双加氧酶,包括PHD1/2/3三种亚型。目前研究较多的是PHD1感受细胞内缺氧信号,调控低氧诱导蛋白1(hypoxia inducible factor 1,HIF-1)在细胞内的稳定性【9】。该过程被认为与血管异常增生和癌症的形成密切相关,因而获得了2016年美国拉斯克医学奖(
下图
)。

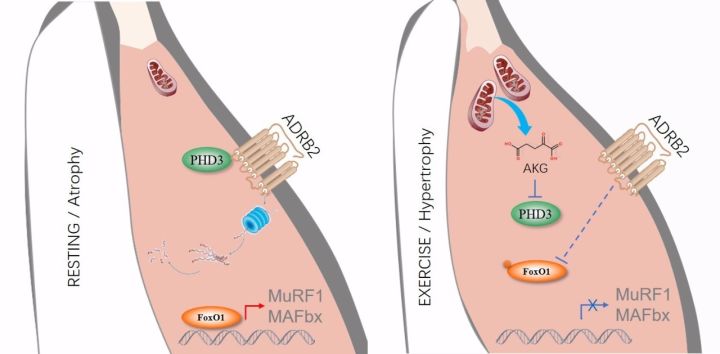
束刚教授课题组深入研究还发现,骨骼肌组织中表达丰度最高的是PHD3,其次是PHD1,而PHD2表达量最低。而且,AKG能特异性下调PHD3的表达,同时降低肾上腺素β2受体(β2-adrenergic receptor, ADRB2)的泛素化水平。ADRB2是一种G蛋白偶联受体,主要分布在骨骼肌,以及骨骼肌和支气管平滑肌。肾上腺素主要通过ADRB2,增加骨骼肌血液供应,抑制肌肉萎缩。上述结果表明,
AKG缓解肌肉萎缩和蛋白质降解的作用主要是通过下调PHD3的表达,抑制ADRB2的羟基化和泛素化降解来实现的。这些机制也有望为研制治疗肌肉萎缩及相关代谢疾病的药物提供新治疗靶点
(
下图
)。
据悉,
蔡兴才
博士和
袁业现
硕士生是该论文的共同第一作者,华南农业大学动物科学学院
束刚
教授、
江青艳
教授和美国贝勒医学院儿童营养中心
徐平稳
博士后为共同通讯作者。
参考文献:
[1] A. Leibowitz, Y. Klin, B.F. Gruenbaum, S.E. Gruenbaum, R. Kuts, M. Dubilet, S. Ohayon, M. Boyko, E. Sheiner, Y. Shapira, A. Zlotnik, Effects of strong physical exercise on blood glutamate and its metabolite 2-ketoglutarate levels in healthy volunteers,
Acta Neurobiol Exp
(Wars) 72 (2012) 385-396.
[2] B.W. Carey, L.W. Finley, J.R. Cross, C.D. Allis, C.B. Thompson, Intracellular alpha-ketoglutarate maintains the pluripotency of embryonic stem cells,
Nature
518 (2015) 413-416.
[3] T. TeSlaa, A.C. Chaikovsky, I. Lipchina, S.L. Escobar, K. Hochedlinger, J. Huang, T.G. Graeber, D. Braas, M.A. Teitell, alpha-Ketoglutarate Accelerates the Initial Differentiation of Primed Human Pluripotent Stem Cells,
Cell Metab
24 (2016) 485-493.
[4] R.M. Chin, X. Fu, M.Y. Pai, L. Vergnes, H. Hwang, G. Deng, S. Diep, B. Lomenick, V.S. Meli, G.C. Monsalve, E. Hu, S.A. Whelan, J.X. Wang, G. Jung, G.M. Solis, F. Fazlollahi, C. Kaweeteerawat, A. Quach, M. Nili, A.S. Krall, H.A. Godwin, H.R. Chang, K.F. Faull, F. Guo, M. Jiang, S.A. Trauger, A. Saghatelian, D. Braas, H.R. Christofk, C.F. Clarke, M.A. Teitell, M. Petrascheck, K. Reue, M.E. Jung, A.R. Frand, J. Huang, The metabolite alpha-ketoglutarate extends lifespan by inhibiting ATP synthase and TOR,
Nature
510 (2014) 397-401.
[5] R.V. Duran, E.D. MacKenzie, H. Boulahbel, C. Frezza, L. Heiserich, S. Tardito, O. Bussolati, S. Rocha, M.N. Hall, E. Gottlieb, HIF-independent role of prolyl hydroxylases in the cellular response to amino acids,
Oncogene
32 (2013) 4549-4556.
[6] W. Xu, H. Yang, Y. Liu, Y. Yang, P. Wang, S.H. Kim, S. Ito, C. Yang, P. Wang, M.T. Xiao, L.X. Liu, W.Q. Jiang, J. Liu, J.Y. Zhang, B. Wang, S. Frye, Y. Zhang, Y.H. Xu, Q.Y. Lei, K.L. Guan, S.M. Zhao, Y. Xiong, Oncometabolite 2-hydroxyglutarate is a competitive inhibitor of alpha-ketoglutarate-dependent dioxygenases,
Cancer Cell
19 (2011) 17-30.
[7] Q. Yang, X. Liang, X. Sun, L. Zhang, X. Fu, C.J. Rogers, A. Berim, S. Zhang, S. Wang, B. Wang, M. Foretz, B. Viollet, D.R. Gang, B.D. Rodgers, M.J. Zhu, M. Du, AMPK/alpha-Ketoglutarate Axis Dynamically Mediates DNA Demethylation in the Prdm16 Promoter and Brown Adipogenesis,
Cell Metab
24 (2016) 542-554.
[8] X. Cai, C. Zhu, Y. Xu, Y. Jing, Y. Yuan, L. Wang, S. Wang, X. Zhu, P. Gao, Y. Zhang, Q. Jiang, G. Shu, Alpha-ketoglutarate promotes skeletal muscle hypertrophy and protein synthesis through Akt/mTOR signaling pathways,
Sci Rep
6 (2016) 26802.
[9] C.B. Thompson, Into Thin Air: How We Sense and Respond to Hypoxia,
Cell
167 (2016) 9-11.

束刚
现任华南农业大学动物科学学院教授,博导。2000年毕业于安徽科技学院畜牧专业,2003年在南京农业大学获基础兽医学硕士学位,随后一直在华南农业大学动物科学学院动物营养调控实验室工作,并获得动物营养与饲料科学博士学位。2014年获国家留学基金委资助在美国德克萨斯州贝勒医学院儿童营养研究中心访学一年。目前主要研究方向是代谢中间产物营养生理与能量代谢。现任畜牧兽医学会动物生理生化分会和广东省生理学会理事。2014年入选广东省“优秀青年教师培养计划”;2017年入选华南农业大学 “丁颖人才支持工程”。近年来,以(共同)第一/通讯作者在
Cell Reports,FASEB Journal,Journal of Nutritional Biochemistry,Journal of Agricultural and Food Chemistry
和
Journal of Animal Science
等杂志发表多篇论文。


BioArt,一心
关注生命科学,只为
分享更多有种、有趣、有料的信息。
关注请长按上方二维码。投稿、合作、转载授权事宜请联系微信ID:
fullbellies
或邮箱:
[email protected]
。





