针对
程序性细胞死亡受体1
(
PD-1
)及其配体
程序性死亡配体1
(
PD-L1
)的
免疫检查点阻断疗法
已经显示出重大的临床益处,多款免疫检查点抑制剂药物成功上市,并挽救了无数癌症患者的生命,
基于免疫检查点的肿瘤免疫疗法也荣获了
2018年的诺贝尔生理学或医学奖
。这些都
使肿瘤免疫疗法成为关注的焦点。
然而,大多数患者在使用免疫检查点抑制剂后,初期很有效,但没有表现出持久的缓解,并且有一些肿瘤甚至对检查点抑制剂完全无效。
现有的基于抗体的药物通过构象阻断细胞表面上的PD-L1来起作用,但是最近的研究表明
PD-L1并非全部存在于细胞表面
,也存在于细胞内,并且可以通过循环重新填充到细胞膜上。
因此,
降低PD-L1的细胞丰度是PD-L1作为关键免疫抑制分子可靠且持久靶向的关键
。
2019年3月25日,
仁济医院
消化科
许杰
团队
设计并开发了
一种多肽,通过竞争抑制PD-L1的棕榈酰化,可以消除癌细胞中PD-L1的表达。
该研究提供了关于PD-L1稳态调节的新见解,并开发了针对PD-L1依赖性癌症免疫逃逸的新策略。也为免疫检查点抑制剂研发提供了新的研究思路。
该研究以
Inhibiting PD-L1 palmitoylationenhances T-cell immune responses against tumours
为题发表在最新一期的
Nature
子刊
Nature Biomedical Engineerin
g 杂志上。
通讯作者:
许杰
(仁济医院)
;
第一作者:
姚晗
(仁济医院)
、
兰江
(华西医院)
、
李楚舒
(仁济医院
)、
石虎兵
(华西医院)
。

PD-1
(programmed cell death 1)
,程序性死亡受体1,是免疫细胞
T细胞
上表达的一种蛋白,用于识别并“杀死”肿瘤细胞。
PD-L1
(programmed cell death-Ligand 1)
,程序性死亡配体1,是
肿瘤细胞
上所表达的蛋白,PD-L1会特异性结合PD-1,结合后便抑制了T细胞的活化和增殖,从而造成
肿瘤细胞的逃逸
。

棕榈酰化修饰
(Palmitoylation)
是一种蛋白质翻译后修饰,在调控蛋白的转运、稳定性、细胞定位等方面有重要作用,棕榈酰化修饰由棕榈酰转移酶催化。
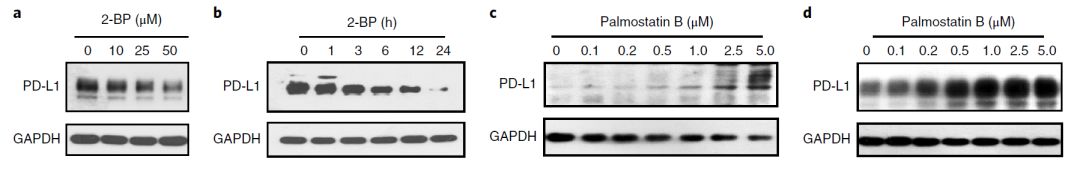
首先,研究团队发现棕榈酰化的
抑制
剂2-BP
可显著抑制肿瘤细胞中PD-L1的表达。而
棕榈酰化的
增强
剂palmostatin B
可
显著增强肿瘤细胞中PD-L1的表达。
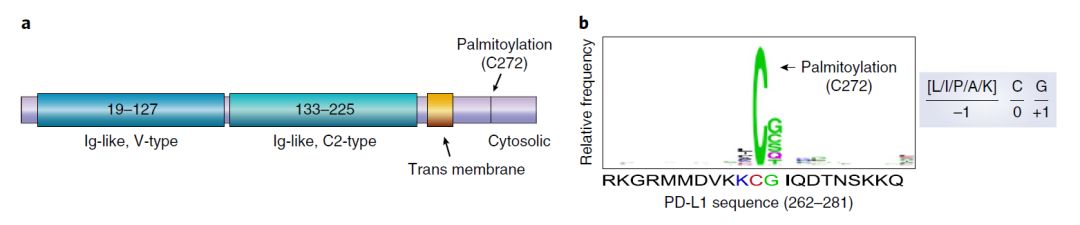
然后,研究团队通过CSS-palm 4.0和MDD-Palm两种模型一致预测到PD-L1上的棕榈酰化位点位于C272氨基酸处,位于PD-L1蛋白的细胞内结构域。
泛素-蛋白酶体途径,是一种比较普遍的内源蛋白降解方式。
需要被降解的蛋白先被泛素化修饰
,然后被蛋白酶体降解。
棕榈酰化可以显著抑制PD-L1的泛素化修饰
,从而抑制PD-L1的降解。
肿瘤细胞中PD-L1的棕榈酰化主要由棕榈酰转移酶家族中的
DHHC3调控,通过shRNA敲低
小鼠MC38肿瘤细胞中DHHC3的表达,导致PD-L1的表达显著降低。小鼠体内实验进一步表明,敲低
DHHC3会显著抑制
MC38肿瘤细胞的生长。

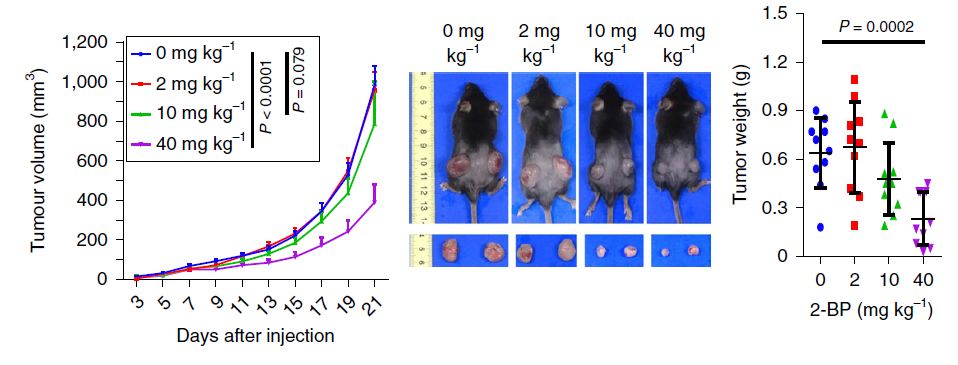
前期的实验已经证实棕榈酰化的抑制剂
2-BP
能够
显著抑制肿瘤细胞中PD-L1的表达,研究团队将
棕榈酰化的抑制剂
2-BP
按不同剂量注射给携带MC38肿瘤的小鼠,发现
40mg/kg剂量的
2-BP
可以显著抑制肿瘤生长,
表明
通过棕榈酰化抑制剂2-BP靶向PD-L1棕榈酰化可以有效抑制肿瘤细胞的PD-L1依赖性免疫逃逸。
虽然棕榈酰化抑制剂
2-BP
可以有效抑制肿瘤细胞中的棕榈酰化,从而抑制肿瘤生长,但是哺乳动物细胞中有20多种棕榈酰转移酶,
2-BP
这种小分子抑制剂没有特异性,并不能只靶向调控肿瘤细胞中PD-L1棕榈酰化的
DHHC3。
竞争性抑制
是靶向特定酶的有效方法,因此研究团队考虑利用竞争性抑制的策略开发特异性更好的棕榈酰化抑制剂。该研究已经
鉴定了PD-L1的棕榈酰化位点,
位点附近的多肽序列可能通过竞争性结合
DHHC3,从而抑制
内源性PD-L1的棕榈酰化。
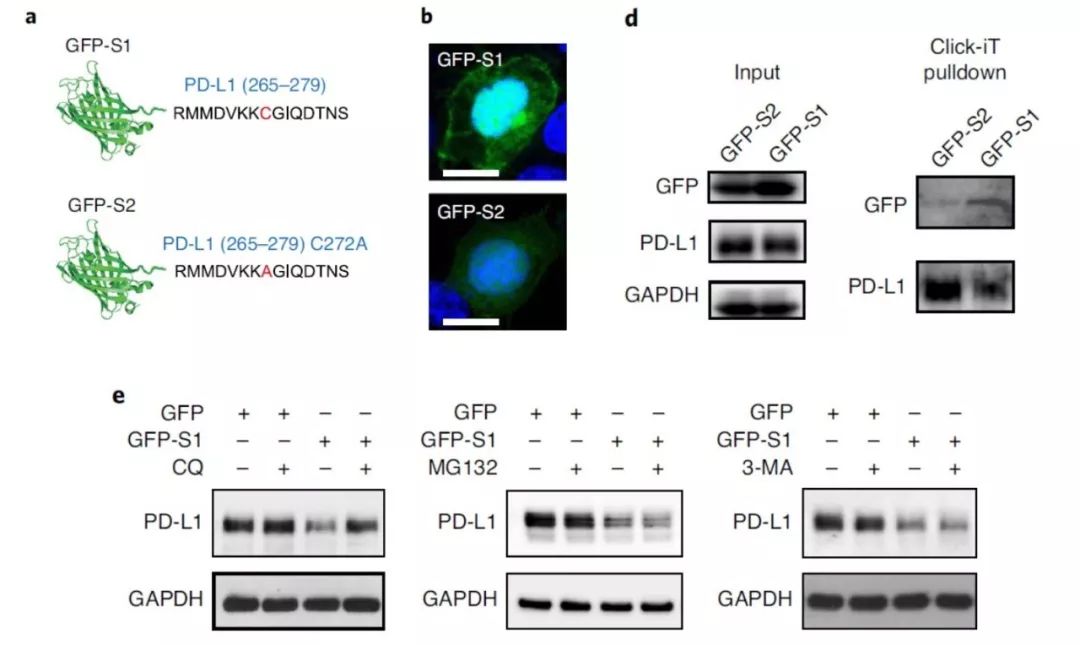
将
绿色荧光蛋白
(GFP)
与含有棕榈酰化位点的PD-L1
(265aa-279aa)
序列
(命名为S1)
的多肽融合,对照组为不包含有C272A突变的多肽序列
(命名为S2)
,结果表明S1可以有效降低PD-L1的棕榈酰化,从而显著降低肿瘤细胞中PD-L1的表达。
这表明,
竞争性抑制的策略可以抑制PD-L1的棕榈酰化
。
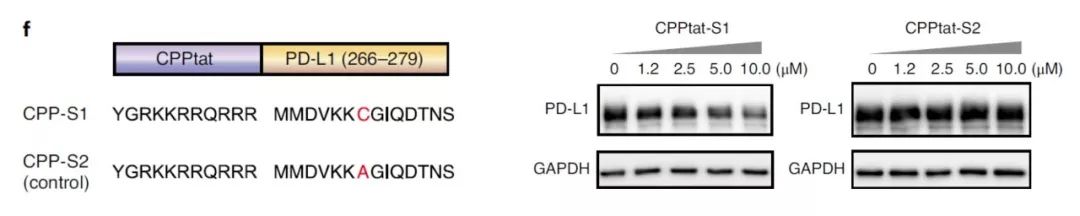
最后,研究团队将设计并开发的
PD-L1棕榈酰化的
竞争性抑制剂引入肿瘤细胞。
细胞穿透肽
(CPP)
是细胞内递送生物分子的有效方法,将CPP与S1序列融合成多肽。实现结果表明,
CPP-S1多肽可以有效降低PD-L1的表达。
研究团队进一步检测了CPP-S1多肽在小鼠体内的耐受性。小鼠腹腔注射