UDI
系统在医疗器械经营领域中的推进与实践
刘亚芝, 李杨, 赵宇, 张锋, 周强, 胡咏梅,
刘郭欢,王晓贞, 王小蕊, 周蕾
医疗器械唯一标识
(unique device identifier
,
UDI)
是医疗器械的身份证。
2019
年
8
月,国家药品监督管理局发布《医疗器械唯一标识系统规则》,旨在进一步加强医疗器械全生命周期的监督管理,创新监管模式,自
2019
年
10
月
1
日起正式施行。通过建立
UDI
系统,有利于运用信息化手段实现对医疗器械在生产、经营和使用各环节的快速、准确识别,有利于实现产品监管数据的共享和整合,实现政府监管与社会治理相结合,形成社会共治的局面,从而进一步提升公众用械安全有效的保障水平。
UDI
系统的推进和实践是一项相对复杂且十分具有挑战性的工作,需要打通医疗器械在生产、经营、使用和监管各个环节中的连接。对于医疗器械经营企业,利用
UDI
可建立符合现代化的物流体系,实现医疗器械供应链的透明化、可视化、智能化。本文基于首批参与
UDI
系统试点的应用实践,从医疗器械经营企业角度出发,详细阐述
UDI
系统在我司推进与实践过程中遇到的问题、应用的具体工作方法及措施,分享实践案例,为我国全面落地实施
UDI
系统、实现医疗器械全生命周期闭环管理提供借鉴。
1 UDI
系统在医疗器械经营企业推进中的问题分析
1.1
对接的上游生产企业众多,多数企业不具备赋码能力
作为医疗器械领域全国最大的流通企业,我司对接的上游生产企业数千家。虽然截至
2020
年
4
月
19
日,我国有超过
3 200
家医疗器械生产企业使用了国际物品编码协会
(GS1)
标准,企业可不必改变原有产品标识标准而高效实施
UDI
和追溯系统,但目前全国参与
UDI
试点的医疗器械生产企业仅
116
家,对接的多数上游企业仍不具备赋码的能力和条件。
1.2
经营产品类别繁杂、数量庞大,信息化、精细化管理技术要求高
我司经营范围涵盖各品类医疗器械,商品数据库
MDM
系统中已有商品规格超过
200
万。让分类繁杂、数量庞大的产品在经营过程中的每一个环节都实现
UDI
全程追溯,无论是信息系统建设,还是实现精细化的全生命周期闭环管理,均具有难度,对信息化、精细化管理的技术要求高。
1.3
下游医院客户专业性强,行业内管理要求复杂,信息对接客观受限
医院内的医疗器械管理往往与专科疾病的诊疗相关,且医院内本身已有进行医疗处置的
HIS
、
LIS
、财务系统、医保结算系统等各种专业信息系统。医院内涉及患者相关的信息不可共享,而要实现
UDI
系统在医院内部全流程追溯,必然要和院内各系统进行对接,而信息共享部分受限、有些系统年代较久远无法做接口等情况,也给
UDI
系统的推进带来不少信息对接方面的问题。
2
基于
UDI
系统的医疗器械全生命周期闭环管理实践
基于美国、欧盟已实施的药品追溯标准
EPCIS
,同时充分考虑国内医疗器械业务特点,以“数字货单”为追溯接口,支持多种追溯模式。生产企业连接“数字货单”追溯接口后,无需自建追溯体系,解决其需要高成本投入
(
重新建立经营、药店、医院业务系统
)
的问题,避免了资源浪费,提高行业效率。医院通过“数字货单”追溯到的信息可实时反馈到内部信息系统的预警预测平台,实现医用耗材精细化管理。“数字货单”可以数字化网络传输“订单”“订单确认”“发货单”“入库单”“发票号”等单据,将企业资源计划
(enterprise resource planning
,
ERP)
系统、仓储管理系统
(warehouse management system
,
WMS)
、院内供应链服务
(supply processing distribution
,
SPD)
系统等串联起来,让供应链上下游如厂家、海关、商检、物流、经营企业、第三方物流、医院、患者等互联互通,实现真正的电子商务,实现业务与全程追溯融合。
生产企业是推进实施
UDI
系统的源头,我司协助生产企业建设溯源平台
(
见图
1)
、防窜货及销售信息统计平台,借助
UDI
为契机进行信息化升级;积极为生产企业提供咨询、发码、生产线改造、追溯等完整解决方案,重点支持试点前未赋码的企业,包含普通卫生材料、体外诊断产品、骨科、口腔、全链条、新冠肺炎疫情相关的共计
13
家生产企业。
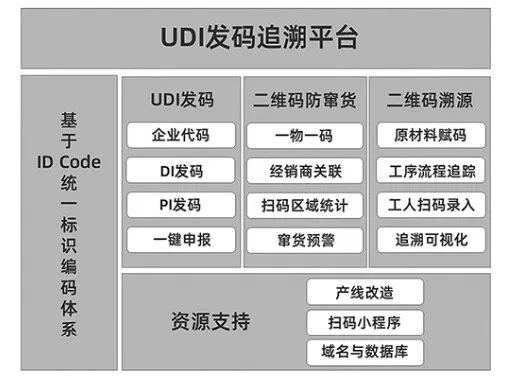
图
1 UDI
发码追溯平台
UDI
系统由
UDI
、
UDI
载体和
UDI
数据库组成,
UDI
则由产品标识
(DI)
和生产标识
(PI)
两部分组成。国家
UDI
数据库由国家药品监督管理局
(
以下简称“国家药监局”
)
统筹规划建立,内容主要包含医疗器械产品标识及相关信息,即
UDI
-
DI
。在经营企业自身信息化升级改造的过程中,与国家
UDI
数据库的对接尤为重要,我司采取的具体实践措施有:①对接
UDI
数据库,实现数据下载。②制定主数据
(MDM)
与国家
UDI
数据库下载数据的对接实施方案,分三阶段进行。阶段
1
:建立
UDI
本地库,每天定时获取国家
UDI
库中的数据,存储于本地数据库镜像,通过生产厂家、注册证号、商品名称、规格型号等与
UDI
数据库中产品信息进行对码,辅以人工判断,实现简单产品的关联映射;阶段
2
:通过首营时收集标签和
DI
、盘库时收集
DI
与商品信息对应关系、厂家提交等多种方式,尽快完成有
UDI
码产品的
DI
收集及与商品信息的对应;阶段
3
:改为通过
DI
与国家药监局
UDI
-
DI
或本地镜像自动同步更新,最终通过
DI
实现自动更新。③连通
ERP
支持
UDI
系统实施,对接
MDM
,自动同步更新,实现一扫首营、一扫查找、一扫自动录入和后台核验
UDI
信息
(
见图
2)
。④连通
WMS
支持
UDI
系统实施,对接
MDM
,支持所有发码机构、载体和字段。⑤
ERP(JDE)
数据与
UDI
数据对码,见图
3
。
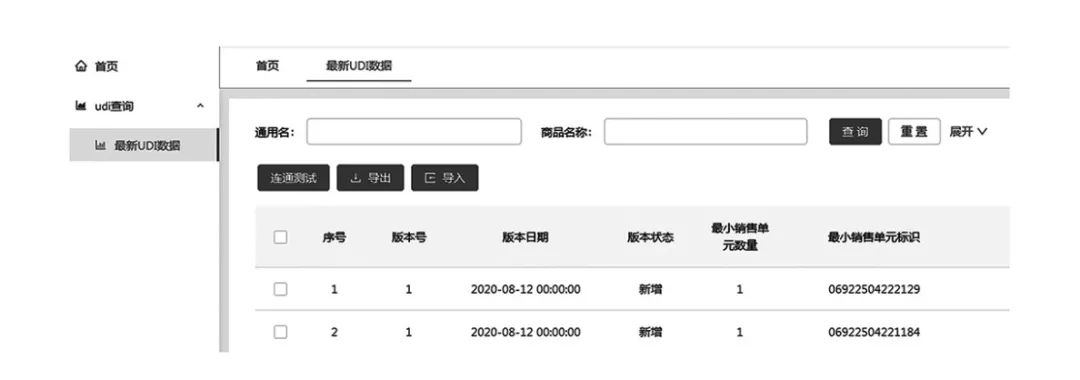
图
2
最新
UDI
数据查询-
MDM
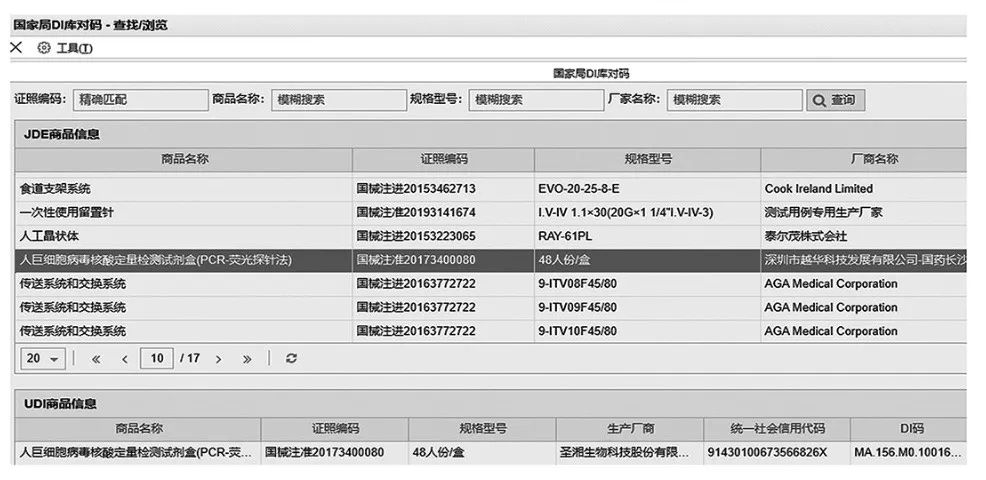
图
3 JDE
数据与
UDI
数据匹配
为下游医院客户导入医疗器械全程追溯系统
(
见图
4)
,实现对医疗器械生产、流通、使用全过程中不良事件监测预警、产品召回的追溯管理,有效控制风险,提高管理效率。承接北京、上海、湖南等大型三级医院的“医院耗材物联网供应保障管理系统”建设,基于
UDI
数据库搭建医院主数据同步平台与资质证照平台,通过标准化产品信息及分类,不断优化中心库数据,帮助终端医疗机构有效向上追踪产品生产、流通数据,保证产品的安全性,让产品有源可溯,有据可查,减少医疗差错,规范医疗行为。
将
UDI
与医院物资信息化管理系统
(SPD
系统
)
、
HIS
系统相结合,
SPD
赋码与
UDI
编码规则保持一致,深入医院各级库房,进行全流程、全方位、全产品的精细化管理:①全流程:权威多渠道
UDI
数据来源;消毒供应应用
UDI
本体赋码;定数包应用
UDI
赋码;智能耗材柜采用
UDI &
无线射频技术
(radio frequency identification
,
RFID)
方案。②全方位:高低值耗材、设备、
IVD
;基础数据及资质证照;
GUP
;不良事件、召回、临床研究。③全产品:对未赋码产品按
UDI
规则赋物流或院内码。
实现扫
UDI
码即可进行院内医疗器械供应链全程监管,可在不增加工作压力的前提下,解决医院各系统之间“信息孤岛”的问题,打破院内医疗器械物流和信息流分离的局面
(
见图
5)
,助力实现医疗器械全生命周期闭环管理。
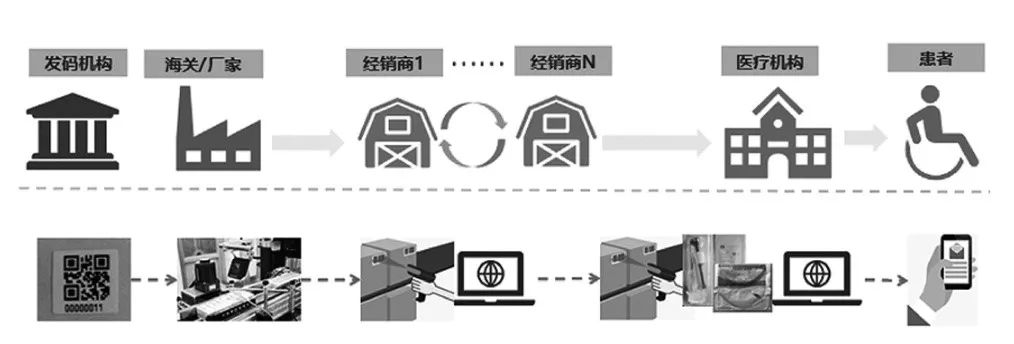
图
4
基于
UDI
的
FLI
+溯源系统
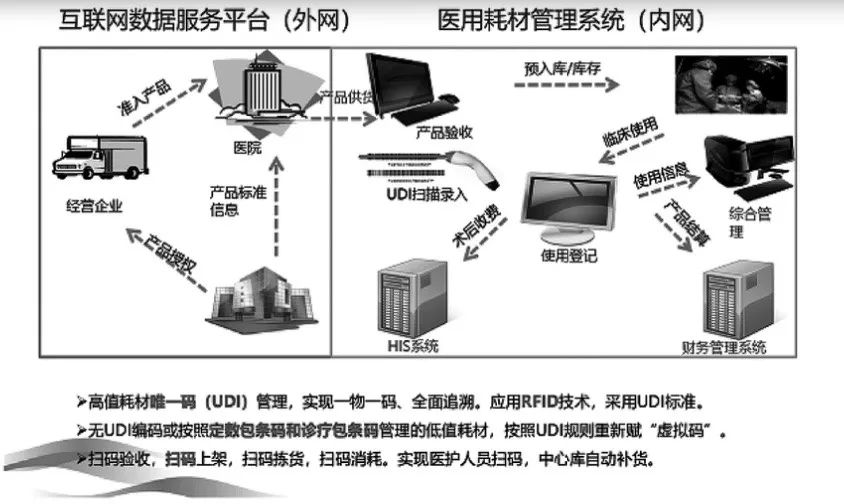
图
5
基于
UDI
及
SPD
系统的医院耗材信息化管理架构
3 UDI
系统在医疗器械经营企业中的实践经验与成效
3.1
制定经营企业推进应用
UDI
系统的基本原则
①在医疗器械采购、验收、贮存、销售、运输、售后服务、不良事件报告、纠正、召回、投诉、追溯等供应链全过程,通过记录
UDI
,实现医疗器械的快速、准确识别以及数据的共享和整合。
②检查纸质、电子表单中与
UDI
数据库字段一致或类似的字段,并制定规则,保证数据的一致性,逐步实现在记录中采用从
UDI
-
DI
中提取标准数据以取代其他来源数据。
③采用
UDI
来实现跨不同系统和跨地域的医疗器械信息的链接。
④对于希望扫描
UDI
并从本地或国家药监局
UDI
数据库中提取相关数据自动填充到录入界面、表单的软件系统:可扫描
UDI
,解析
DI
、
PI
;可扫描所有被认可的发码机构的
UDI
编码格式、载体格式;电子、纸质均可收集、存储和交换
UDI
中各字段信息;系统应该能够使用
UDI
-
DI
在本地
UDI
数据库进行实时查找和验证;如果有自动识别和数据采集技术
(automatic identification and data collection
,
AIDC)
部分,则应通过扫码来记录
UDI
;如果从企业外部接收到
UDI(
如追溯系统、电子贸易等
)
,则完整的
UDI
和
UDI
组成字段都应该分别自动填充到指定的
UDI
字段、
UDI
-
DI
字段和分解后各个
UDI
-
PI
字段中。
①验证多码并行的操作性,参考欧盟标准,牵头制定“扫码通”标准,实现
1 h
快速改造。
②首营时要求企业提供
UDI
-
DI
编码和标签。
③利用
UDI
-
DI
的唯一性、数据库字段信息和关联的其他信息,自动填写相关表单,实现资质证照的校验和
GSP
要求的其他校验,并在日常经营中充分利用
UDI
,汇总大数据,实现商业智能。
④要求已赋码的上游企业,在国家药监局填报;未赋码的,可以先按
UDI
规则赋物流码。
⑤要求制造商对产品各级销售包装单元赋
UDI,
优先考虑二维码;建议医院采用
UDI
,取消自编码,直接对接
UDI
-
DI
和院内主数据
(
如院内码、医保耗材码
)
。
⑥建议上下游采用
ISO EPCIS
电子产品编码信息系统标准,通过订单、发货单、包装层级
UDI
关联、随货同行单、验收单、发票等单据的数字化和标准化,传递交易信息,实现数字化供应链、两票制自动核验,并与监管平台、省集采平台、海关
EDI
报关系统对接。
3.3
基于
UDI
系统开展医疗器械全生命周期闭环管理的实践案例
①联合发码机构和扫码枪企业等,在国家药监局标管中心的统一协调下,共同制定
UDI
扫码输出、药品器械追溯实施标准。采用扫码通标准,解决
GS1
等变长字段扫码和智能耗材柜
UDI
联合
RFID
问题。
②通过
DI
自动批量编码技术,协助某生产企业快速完成
625
个
IVD
产品编码及数据上传,包括新冠肺炎疫情急需的新冠检测试剂盒。联合国药研究院、中关村工信二维码中心和服务商,共同为某家试剂产量庞大的企业设计了全自动赋码的产线改造方案:
UDI
数据管理平台与自动化赋码设备直接对接,编码、序列化赋码、关联,一步到位。对河南某生产企业进行现场支持,实现以中关村
MA
二维码为载体的
UDI
全线跑通,初步验证不修改软件系统即可初步兼容
UDI
及二维码。
③参与北京某医院基于
UDI
-
ID
的主数据同步系统建设,关联院内码和医保分类码,实现三医联动。统一院内的药品、器械、疫苗全程追溯系统建设,解决数据归属、多追溯系统互联、批次追溯等难题,支持多方式数据传递
(
接口、文件上传、
WEB
录入、
EMAIL
、
AS2
加密通道等
)
。
UDI
是实现医疗器械科学化、标准化、精细化管理的基石。经营环节是医疗器械全生命周期的中间环节,中国医疗器械有限公司、国药集团医疗器械研究院、国药联众、国药上海、国药上海先进等
UDI
试点单位,充分发挥了经营企业作为供应链枢纽的作用,联动上下游业务主体一起推进实施
UDI
系统。积极组织和参与
UDI
系统培训,为企业和医院提供咨询和整体解决方案;整合多方资源协助生产企业赋码;探索应用经营企业
UDI
系统应用的标准和规范;联合医院、医保,探索实践了
UDI
系统全链条衔接应用。顺应国家监管要求,基于
UDI
系统实施医疗器械全生命周期的精细化闭环管理,保证医疗器械管理的质量,通过全流程信息化追溯系统提高生产、经营、使用各环节的业务效率,推动各环节主体同步推进并协同应用
UDI
系统,有利于全国
UDI
系统的稳步推广。
本文刊登于《中国医药导刊》2020年第9期,更多精彩内容可登陆《中国医药导刊》官方网址http://www.zgyydk.cn,热忱欢迎智慧监管领域相关研究人员积极投稿。





