
实质上,这是一篇关于科技与癌症的长篇文章,需耐心阅读。在抗争癌症的长期斗争中,科技是人类所不断追逐的利器,但我们最后往往会发现,能够决定胜负关键因素却是生命本身的意志,因为科技从来就不是一蹴而就的。

▲ Carmen Teixidor已经与癌症斗争了30年
Carmen Teixidor 女士与乳腺癌战斗了 30 年。她觉得,她已经看过了所有可能治好她癌症的医生。她已经接受了多轮放疗和激素治疗,治疗过程的确是一种煎熬。25 年前,她还尝试过一次化疗,但她的生活质量因此大打折扣,从此她将化疗列入了黑名单。她也做过很多次手术,但当从麻醉中恢复意识后,她却不得不面对让人失望的消息,她开始对手术产生恐惧。
1985年夏天,她第一次得知自己得了癌症,当时医生在她左胸发现了一个大的肿瘤,随后她被迫做了乳房切除术。
在位于纽约的公寓里,她盯着地板回忆道:“实在太可怕了”。对于癌症诊断而言,从来就没有所谓的好时候。但对于Teixidor来说,癌症诊断技术使她开始了自己的艺术生涯——她的两座真人大小的雕塑被放在了洛克菲勒大学的广场上,最近她还完成了Harlem医院的壁画。
这位身材苗条的女士已经年逾70,银灰色的头发扎成了富有活力的马尾辫,她经历了一次又一次的癌症复发,接受过各种癌症治疗方法,从外科手术到最近让人难以置信的分子疗法。
Teixidor 几乎都没有注意到对她病情产生了决定性影响的时刻。2013年秋天,位于纽约的斯隆-凯特琳癌症研究中心(以下简称斯隆癌症中心)的医生分析了一小片她的癌细胞组织,并测定了癌细胞的DNA序列。就像很多学术癌症中心一样,他们这样做是为了寻找可能导致恶性增长的具有指示意义的基因突变。这些具有指示性的基因突变就是新一代特殊设计药物的目标。
结果,Teixidor的癌细胞的确产生了一些受到医学界关注的基因突变。但有一个问题是:当时没有特别针对她的药物问世。
对于 Teixidor 来说,2013年秋天是个无忧无虑的时期,因为她的癌症(尽管复发了很多次)看上去已经受到了控制。但后来事情发生了变化。她说:“两年前,那次复发非常严重。”她可以感觉到一些癌细胞从她的头骨扩散出来,还有一些在她的下颌扎根。她的脖颈有肿瘤,之后扫描显示她的骨头和骨盆里也有肿瘤。这次的病症以前从未有过而且前景不容乐观,这让她很长时间都很阴郁。
斯隆癌症中心的肿瘤学家向她推荐了一个化疗方案,但她拒绝了。“除了化疗我别无选择,为此我觉得非常压抑”,她承认。
塞翁失马,焉知非福。正当Teixidor的癌症病情恶化时,医疗技术也有了进展。
斯隆癌症中心和其他机构经过测试发现,她癌细胞中的一个基因突变与一种试验药物的目标能够匹配起来。虽然,当时癌症靶向药物的价值还存在争议(一个近期的科技评论文章将其描述为“靶向肿瘤学的幻想”),Teixidor依旧加入了临床试验,从2015年夏末开始服用药物。
几周后,她开始感觉癌细胞在减少——后来的扫描也证明它们确实变少了。
虽然有了Teixidor这样让人振奋的试验结果,但靶向癌症治疗的问题依然困扰着医生、科学家、健康保险公司以及今年在美国确诊的超过160万癌症患者。有多少病人能从他们的癌细胞DNA测序中受益?谁会接受这个异常昂贵的治疗方案?现在仅仅一小部分病人能从中受益,社会又愿意承担多少费用?
自从人类基因组项目开始,科学家们就一直梦想着,用精准的个人分子信息来指导疾病的诊断和治疗。
思路其实很简单:获得患有某种疾病的患者的DNA序列,找到产生疾病的基因突变,然后就像打靶一样,用设计好的药物有目标地攻击突变。
然而,不幸的是,生物的复杂性远远超出了我们现有的医学知识范畴。虽然研究者们希望能够用有限的几种常见基因突变解释很多疾病的成因——心脏病、高血压、糖尿病和精神分裂,这些疾病有大量的失败案例,但我们尚未掌握其机理。
然而,癌症治疗却是这些让人失望的案例中的一个亮点。癌细胞很明显地表现出基因异常,这就为药物提供了明确目标。在靶向肿瘤疗法受到广泛议论之前,靶向治疗方案已经成为了癌症治疗中的主要方案。
1998年,美国食品药品监督局批准了一种药物,用于一小部分乳腺癌患者的治疗,他们的癌细胞因为一种HER-2受体的表面分子存在而表现得异常活跃。Herceptin是第一个靶向癌症治疗药物,其后又有两种畅销药研发问世,它们是2001年问世的Gleevec(目标是白血病中的基因突变)以及2011年问世的Zelboraf(目标是黑色素瘤的基因突变)。
随着 DNA 测序变得相对便宜更能被大家接受,这些药物的成功给了人们希望,任何一种肿瘤的基因都可能成为线索,帮助人们找到直接攻击其突变的办法。
简单地说,靶向肿瘤治疗背后蕴含的思路就是:医生对肿瘤进行活检,分析其DNA序列,发现基因突变,其中一些突变可以用已批准的分子药物进行治疗。曾经,医生们会纠结于是治疗乳腺癌还是皮肤癌,将来对癌症定性的依据会变成基因突变类型,而不再是身体的某个部位。
这听起来非常诱人。研究者希望找到每一种癌症基因的弱点,但他们发现癌症突变的生物性要复杂的多得多。实际上,一位负责治疗Teixidor的医生已经开始证明,这到底有多复杂。
2012年4月,美国和欧洲15家领先癌症中心的医生们开始招募病人加入一项大型临床试验,展开一种癌症靶向药物的基础前期测试。他们研究了过去10年的数据,发现患有黑色素瘤这种致命性癌症的病人中,有半数都有名为BRAF基因的基因变异。这种突变使得黑色素瘤细胞很容易受到一种名为Zelboraf药物的攻击。
虽然这种药不能治愈癌症,甚至对一些病人没有任何效果,但在某些病人身上,它能暂时控制住这种高度恶性肿瘤的扩散。

▲ David Hyman是斯隆-凯特琳癌症研究中心的一位肿瘤学家
David Hyman是Teixidor在斯隆癌症中心的一位医生,他领导了一个国际研究小组,他们的研究目标是寻找黑色素瘤中的突变是否存在于其他癌症类型中。
他们希望找到一组病人(不管他们癌症种类如何,都有相同的基因突变),然后用这种药物对他们进行治疗。
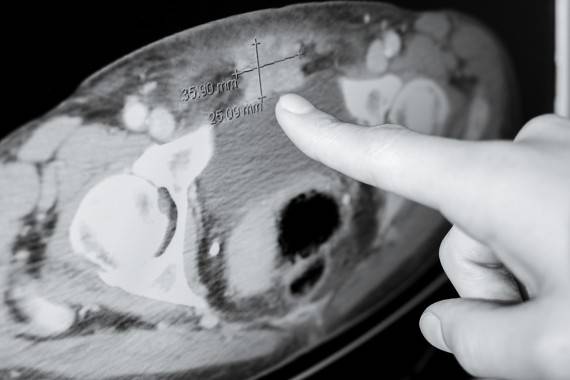
▲ 斯隆癌症中心的Hyman指出MRI扫描上的一个肿瘤
他们的研究结果发表在了2015年8月的《新英格兰医学》杂志(New England Journal of Medicine )上,该结果对肿瘤学界是鼓励也是警示。Hyman和同事们找到的携带BRAF突变的病人,分别患有肺癌、结肠癌、甲状腺癌以及其他类型的癌症。
这种药物对有的人有用,但让人略感意外的是对有的人不起作用。比如对于非小细胞肺癌(non-small-cell lung cancer)患者,他们发现药物能对超过40%的患者起效,减缓他们的疾病发展。
然而,对结肠癌患者而言,虽然他们也有相同的基因突变,这种药物根本不起作用。

▲ 玻片上是经过染色的肿瘤活检组织
这种结果困扰着一批肿瘤学家,比如Michael Kolodziej,他是Flatiron Health 公司一位负责人。Flatiron Health 是一家数据分析公司,主要负责从电子健康记录中筛选信息。
“实际上对于很多病人来说,这对他们没有任何帮助”,他说,“但对于其他人来说,这可能是你可以做的唯一重要的事。但我现在还说不清具体对谁。”
像这样的困窘还有很多。在大多数癌细胞中找到突变都非常稀有,而且其中很多给出的医学信息也模糊不清。现在有一些基因突变是可以治疗的,其他的还不能——至少现在不能。此外,这些治疗方案还不算真正的成功。它们只对一小部分病人有疗效,但这些疗效还没有经过时间的考验;对很多人则根本没有疗效。
研究者们正试图找出原因。就在Hyman和同事们于2015年夏天发表了研究结果的同时,美国国家癌症研究中心(以下简称国家癌症中心)启动了一项大型的野心勃勃的研究项目,他们希望,将所有癌症种类中的某一特定突变与合适的靶向治疗方案匹配起来,为此要进行严格的测试试验。
这项正在进行的研究包括了24个不同的子项目,每一个项目都通过特定路径观察分子的变化,路径方向则由药物来决定。项目涉及了3000多名患者,研究中心将他们的癌细胞进行了测序。
当研究者找到了匹配药物以后,从10月份的结果看大概有22%的概率,他们就将相应的药物直接送到癌症中心对患者进行治疗。
国家癌症中心的Barbara Conley认为,一些关于靶向治疗的怀疑是有证据的。“我认为我们最终会成功。但这毕竟不是轻而易举的事情。”她说。Hyman对此没有表示反对。但随着更多的癌细胞得到测序,更多的靶向药物被研发,靶向治疗会快速发展。
一个幸运的患者可能会发现,今天没法治疗的癌症到了明天就有了治疗办法。现在Hyman可以在自己电脑里,轻松找出在斯隆癌症中心的系统中任何一个病人癌细胞产生的基因突变信息。
2013年春天,Carmen Teixidor做了肿瘤活检,但当斯隆癌症中心的研究者们寻找肿瘤细胞突变的位置时,基因测序没有给出结果。他们随后在10月份又重复了一次测试,这一次测试结果显示Teixidor的癌细胞DNA有几处突变,包括一个名为AKT1的基因。
不幸的是,当时并没有相应的治疗方法——用靶向治疗的行话来说,它还不是有指导意义的基因突变。
然而,就像斯隆癌症中心的其他病人一样,她的癌细胞DNA数据被加入了数据库,这样医院的任何一个临床测试首席研究员都能用她的癌细胞数据进行药物测试。
AKT突变最早发现于2006年,被认为是癌症的诱因之一, 有几家制药公司研发出了AKT抑制剂。最初在癌症患者中的试验是“非常不成功的”,Hyman说,但是将药物用在携带易受攻击突变的患者身上,可能会加大药物起效的机率。
AstraZeneca 公司是几家研发 AKT 抑制剂中的一家,该公司生产了一种名为AZD5363的试验用药,提供给斯隆癌症中心等机构进行临床试验。
当Hyman于2014年开始从事AKT的靶向治疗试验时,Carmen Teixidor的名字出现在他的电脑屏幕上。Hyman说:“随着这个领域的发展,我们好像找到了治疗她的办法。”

▲ 斯隆癌症中心的一位实验技术员将DNA样本放回低温冷冻柜中
2015 年 9 月,Teixidor 开始服用针对 AKT 突变的药物,这种基因突变当时正在她身体里快速扩散。刚开始,药物的副作用让她日渐虚弱,所以她的医生调整了剂量。后来,她的身体很快有了反应,效果非常明显。
“我们几乎马上看到了疗效”。在治疗几周后,她反映已经感觉不到肿瘤的存在。Hyman补充道:“ 肿瘤消失了,这是当靶向治疗起效时一个非常典型的效果,其疗效非常迅速。”
仅仅两个月后,研究者就在美国癌症年会(American Association for Cancer Research)上展示了AKT试验的初期结果。从初期分析的结果看,Hyman说:“大部分患者接受治疗后,癌细胞都有不同程度的退化。”
他补充道,Teixidor 的反应“维持的时间特别长”。她的主治医生现在正很细致地研究她的癌细胞DNA序列,希望能找到为什么她的癌细胞对这种疗法异常敏感的原因。
在最近一次Teixidor与斯隆癌症中心的Hyman团队见面时,她提了一个问题,一个很少有患者对试验用药提出的问题。“我问了关于药物的长期副作用。”她说。答案是:没人知道确切的答案。
毫无疑问,Teixidor 也是足够幸运的,能够在一家大型研究中心得到治疗。不是每家癌症中心都有条件使用最前沿的癌症基因组技术——最近,美国总统奥巴马发起的“癌症登月计划”也发表了官方声明,承认了这种不平等。
他们在一份9月公布的报告中指出,“绝大部分美国人都没有机会得到靶向癌症测试治疗。因为肿瘤学临床试验一般在大型的癌症研究中心进行,而不在大部分癌症病人进行治疗的社区癌症中心进行。”

▲ 斯隆癌症中心的实验室里一台自动备样仪
的确,癌细胞测序仍然是一个相对不普及的项目。前NIH负责人Harold Varmus认为,癌症基因组的一个巨大“缺憾”就是参与试验的患者太少了。
美国医疗补助(Medicare)及大部分医疗保险(health insurers)都不涵盖DNA测序的费用,而其费用不是小数目:每次活检的癌细胞测序费用,根据测试机构不同从600到1000美元不等。
但是,Varmus指出这已经比一些标准化癌症检查手段要便宜,比如很多成像扫描。他说:“癌症患者一般都要进行几十种成像扫描——CT扫描、PET扫描、MRIs等。”这些检查每一项的花费基本在 500 到 5000 美元不等。

▲ 斯隆癌症中心的数据库意味着肿瘤信息已经可以使用
然而,测序费用只是造成靶向癌症药物昂贵的一部分原因。靶向疗法经常一个月就能轻易烧掉10000美元。保险公司通常不会报销这些费用,因为他们没法确定到底有多少患者能从中受益。
Vinay Prasad是位于波特兰的俄勒冈州卫生科学大学(Oregon Health and Science University)的肿瘤学家,近期他的研究表明,在患有复发性无法治愈的肿瘤患者中,仅有1.5%的患者能从靶向疗法中受益——但对于很多人来说,也只是延长几个月的生命。
他在一篇发表于《自然》杂志的文章里说,尽管在极个别案例中对患者产生的疗效让人振奋不已,但“大部分癌症患者还不能从靶向治疗中受益”。另一位肿瘤学家Howard West ,质疑了研究者们的行为——他们“为了极少数的成功欢呼雀跃。他们为了达到这种所谓的成功,却对无数的失败案例闭口不谈。”
他说:“对,的确有一小部分赢家。但是这就像买彩票一样。难道值得我们投入上百万美元去找那几个患者,要是找不到呢?”
这些批评让像Razelle Kurzrock这样的研究者感到困惑,Razelle Kurzrock任职于加州大学癌症中心(UCSD )。Kurzrock和她的同事近期分析了上百个临床试验的结果并提出了他们的看法,当靶向药物与特定癌细胞突变相匹配时,药物起效的概率和无恶化生存期都有明显增长(无恶化生存期,progression-free survival,这个指标是指药物生效到患者的肿瘤重新恶化之间的时间)。
她说:“显然,靶向药物对多种癌症都有效果”。她的研究开始于休士顿德州大学安德森癌症中心,现在她在UCSD继续该项研究。她认为,患者已经开始从新一代的测序和相应药物中开始受益。
“你可以看到显著的效果”,她说,当医生使用多种靶向联合治疗方式时,药物起效概率还能增加。
我们希望,一旦获得更多数据后,能有更多的患者得到帮助。Hyman举了个例子,去年3月FDA批准了一种药物,针对大概1%的肺癌患者中出现的基因突变。
根据Hyman描述“能显著延长患者寿命”。他表示,如果我们不用每年去寻找22.5万名美国肺癌患者中的基因突变,那这些钱就可以省下来用在给病人的医疗保险上了。
“我们没法坐视不理”,他说,“即使它对100%的患者都不起作用,即使它只对1%、5%或者10%的患者有效,那也足够了”。
不管有多少人能受益,Carmen Teixidor仍然心存感激。就在前不久,她坐在电脑旁,翻看着装满她作品的文件夹。她解释说,这是近期的一系列作品,原始图片是一张聚焦于她自身皮肤的一英寸见方的照片。
然后,她对原始图像做了修改——包括对皱纹和所有东西(通过镜像和数字处理),创造出非凡的织物图案和让人惊叹的三维形状,比如花瓶和花朵。
在谈话中,她提到与癌症相处了那么多年已经让她释然。她发问:“如果你不能感觉到生命的终点在哪,那什么是生命?”

▲ Teixidor将继续她与癌症的战斗
然而,在去年11月,医生告诉她,她的癌细胞又开始长大,这让她的未来多了一丝不确定。她苦笑道:“现在,我选择不去想它。”
编辑:李青青
欢迎关注DT君的科幻电影公众号:


招聘
编辑、视觉设计、视频策划及后期
地点:北京
联系:[email protected]
MIT Technology Review 中国唯一版权合作方,任何机构及个人未经许可,不得擅自转载及翻译。
分享至朋友圈才是义举














