2015 年 7 月 22 日,国家食品药品监督管理总局发布了《关于开展药物临床试验数据自查核查工作的公告》(2015 年第 117 号),正式拉开了临床试验数据自查这场临床试验行业轰轰烈烈的整风运动的序幕。
自「 722 文」发布至今,已有快两年,这期间,CFDA 共发布了 7 大批自查名单,12 个药物临床试验数据现场核查计划公告。
此次, Insight 通过临床自查核查的数据
(数据统计到 2017.06.27)
整理,
还原这 2 年整个临床数据自查核查的过程,
演算下一批自查名单进入核查计划的时长,
推测未来纳入到现场自查计划的企业品种
.....
7 大批次自查名单
在 7 大批自查名单中,被要求自查的共有 2032 个药品注册申请受理号,部分企业在名单发布后将产品主动撤回,撤回的受理号中也不乏有一些跨国大企业或是曾经获得 CDE 优先审评公示的受理号。
药品注册申请人撤回注册申请,并不意味着不予批准注册退出市场,注册申请人重新开展或者补充完善临床试验后,可以重新申报。
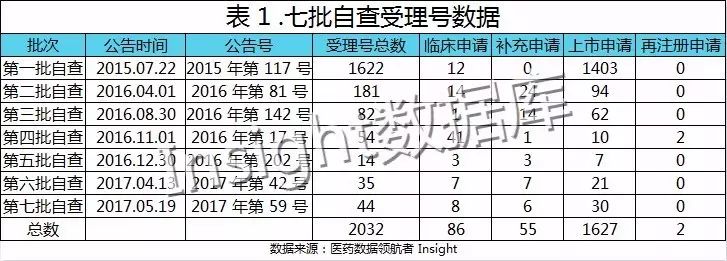
表 1 中七批自查受理号的临床申请、补充申请、上市申请和再注册申请的具体数据情况来自 Insight 数据库。从表中可以看出,7 大批次名单的公布时间,从早先的 8 个月到现在短至 1 个月,公布时间在不断的加快,照这速度,在不久之后,不是按照最新的注册审评标准报的上市申请以及有过临床试验的其他申请类型,都会一一出现在后续的要求自查核查的名单中。
数据结果显示,上市申请的受理号均占超大份额,可见企业自查的重头戏在于要求药企在药品上市前把好最后一道关,保证药品未来使用时的安全性和有效性,不留后患。
12 个现场核查计划
现场核查计划指的是,核查中心对于需核查的品种按审评顺序、自查报告筛选以及举报信息等情况拟定的并公示出来的现场核查计划。若在核查中发现擅自修改数据、瞒报数据、虚假数据以及数据不可溯源等弄虚作假的问题,其注册申请将不予批准。
截至今日,共公布 12 个现场核查计划,涉及 351 个药品注册申请受理号,最近一批公布时间就在本月的 23 号。
现场核查审评结论
到目前为止,现场核查后批准进口的受理号共有 38 个,均为前 3 个批次的受理号,后 4 批次的自查受理号还在审评中或是处于排队待审评状态。批准进口的受理号中,以勃林格和诺华两个企业的受理号最多,具体信息如下表:
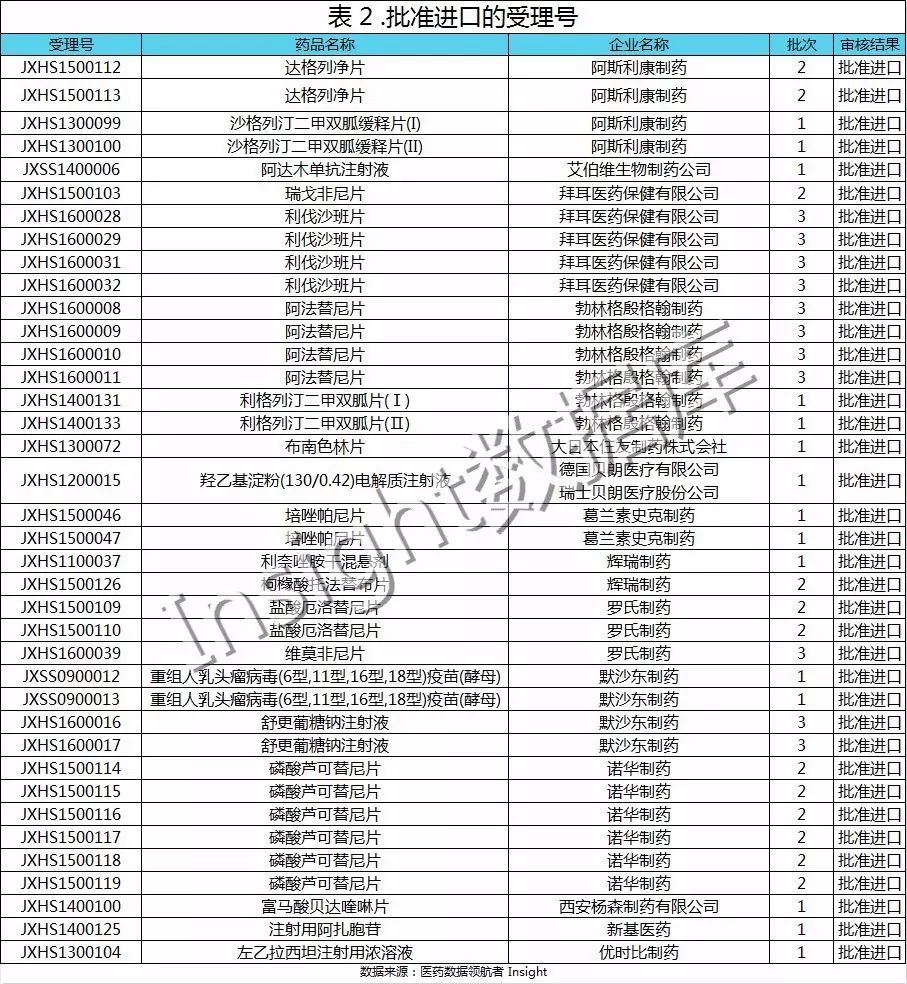
目前,现场核查后批准临床的受理号共有 7 个,多为第 4 批的受理号,原因可能是因为第四批基数大,其申请临床数占 7 批自查名单总和的一半。具体信息如下:
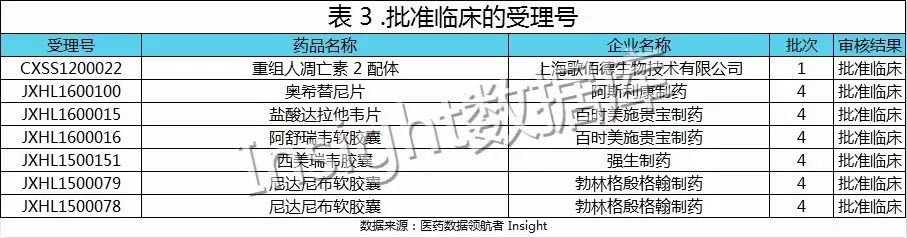
现场核查后批准生产的受理号共有 17 个,均为前 3 个批次的受理号,且多为第一批次。独有的一个在第三批次自查名单中的,已被批生产的是安徽贝克生物制药有限公司的富马酸替诺福韦二吡呋酯片,该品种是优先审评审批的品种,具体信息如下:
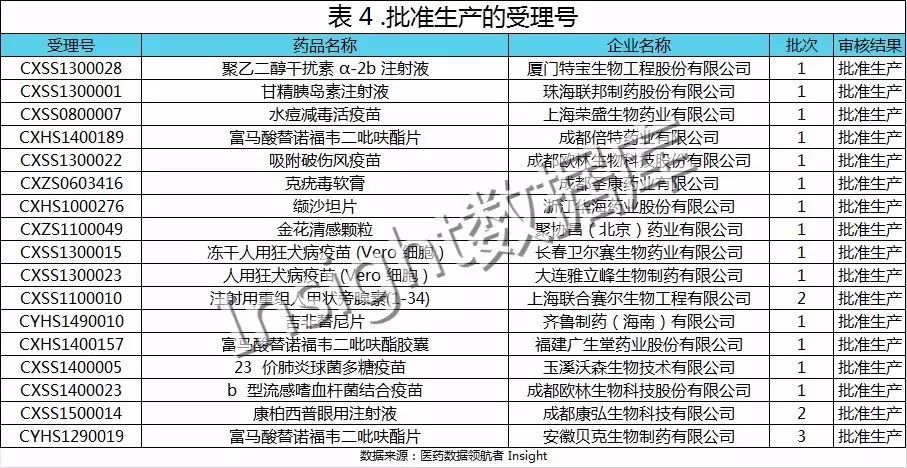
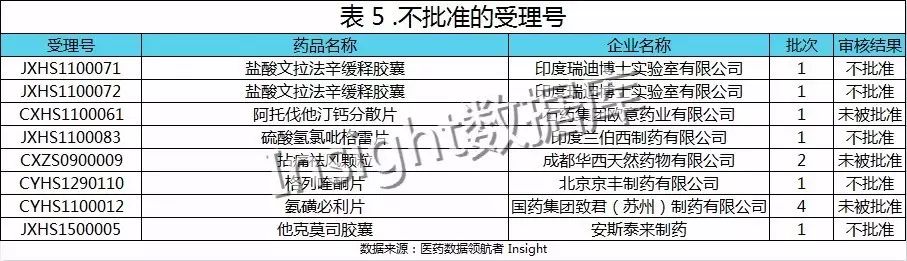
而不被批准的受理号,目前共有 8 个,具体信息如下:
我们对每一批次要求企业自查的受理号最早进入到 12 个现场核查计划的时长做了一个统计,结果如下表:
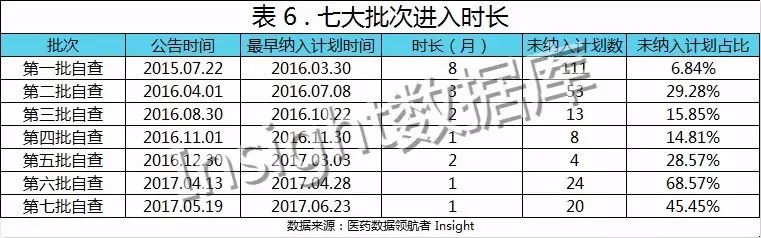
从表 6 可以看出,如今,7 大批次自查名单的受理号纳入到现场自查计划的时长越来越短,可见国家局现场自查工作步伐也在逐步加快。我们可以推测,在要求自查名单发布后,该名单内的品种最快一个月的时间被列入到现场核查计划。
同时值得一提的是,发布最早的第一批自查名单中至今仍然有 100 多个受理号未纳入计划,在后续的现场核查计划中应该还会有第一批的身影。
未列入现场自查计划
先说明一点,本次统计的未纳入现场核查计划的受理号是指,当前还未结束审评审批流程,且尚未在现场核查计划中出现的受理号。
未纳入现场自查计划的受理号国产进口占比情况如下:
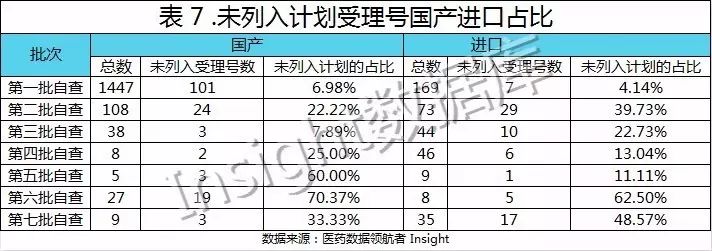
按成分词筛选后,未列入现场自查计划的品种有 178 个,这些未来将很有可能进入到现场自查计划名单,进而批临床/生产/进口。
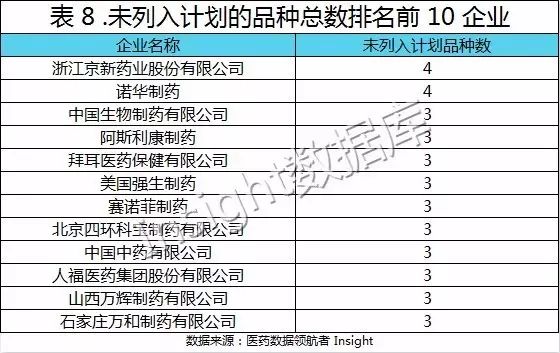
从表 8 中可以看出,在列入计划的品种中,以京新药业和诺华制药的 4 个品种数(按成分词统计)为最多,其中京新药业的盐酸普拉克索片、重酒石酸卡巴拉汀胶囊和瑞舒伐他汀钙分散片申报上市,诺华制药的雷珠单抗注射液、沙库巴曲缬沙坦钠片、盐酸帕罗西汀薄膜衣片和格隆溴铵吸入粉雾剂用胶囊 4 个品种申报上市。
在 Insight 数据库公众号回复关键词「
成绩单
」,即可下载未列入现场自查计划的这 178 个受理号的具体数据信息。

点击「
阅读
原文
」,免费获取 Insight 账号,查看更多临床数据自查核查受理号信息。





