慢性淋巴细胞白血病(CLL)患者依鲁替尼治疗失败后,采用CAR-T细胞输注治疗的效果和安全性如何?美国弗雷德哈钦森癌症研究中心临床研究部Cameron J. Turtle博士对此进行了一项研究,结果表明,CD19 CAR-T细胞治疗在依鲁替尼失败后的高风险CLL患者中高度有效。结果于7月17日在线发表在《JCO》上。
慢性淋巴细胞白血病是最常见的成人白血病。最近,美国FDA批准了一种布鲁顿酪氨酸激酶(BTK)抑制剂依鲁替尼,用作复发和难治性CLL的初始治疗及随后的一线治疗。虽然依鲁替尼的总应答率(ORR)较高,但是完全应答(CR)率较低,并且发生疾病进展的患者具有较短的生存期。一项研究显示,其中位总生存期(OS)仅为3个月。
对于难治性B细胞急性淋巴细胞白血病(ALL)和非霍奇金淋巴瘤(NHL)患者,淋巴细胞删除性化疗后进行CD19特异性嵌合抗原受体T(CAR-T)细胞输注,已经使他们产生了较高的应答率。一项小型研究显示,CD19 CAR-T细胞输注可造成CLL患者持久缓解,但是研究中的患者既往未接受过依鲁替尼治疗。此项研究,旨在评估既往依鲁替尼治疗失败后的CLL患者,使用CD19 CAR-T细胞输注治疗的安全性和可行性。
这是一项I/II期开放性临床试验。CAR-T细胞的输注剂量水平(DL)为:DL1(2×105CAR-T细胞/kg)、DL2(2×106CAR-T细胞/kg)和DL3(2×107CAR-T细胞/kg)。CLL患者的入组标准为,抗CD20抗体和氟达拉滨(Flu)或苯达莫司汀治疗失败。淋巴细胞删除性化疗由环磷酰胺(Cy)、Flu或Cy+Flu组成,化疗后输注CAR-T细胞。
淋巴结应答通过国际慢性淋巴细胞白血病工作组(IWCLL)标准确定。淋巴细胞删除性化疗前和CAR-T细胞输注后4周时获取骨髓活检。使用国立癌症研究所不良事件常见毒性标准对毒性进行分级。
患者特征:
研究入组了24例患者(中位年龄61岁;范围,40~73岁)。淋巴细胞删除性化疗前,具有骨髓异常B细胞的患者百分比的中位值为61.6%(范围:0%~96%)。23例患者具有淋巴结病,2例具有中枢神经系统疾病。进行CT和PET检查的15例患者中,有14例具有氟脱氧葡萄糖(FDG)狂热病。
在接受包含Flu和利妥昔单抗的治疗方案后,23例患者出现难治性或复发性疾病。1例苯达莫司汀+利妥昔单抗治疗的患者出现治疗失败。所有患者都接受了依鲁替尼治疗(中位治疗时间,13个月;范围,0.75~39个月),其中19例患者接受依鲁替尼治疗期间出现疾病进展,3例患者对依鲁替尼不耐受。9/19例疾病进展的患者中,检测到与依鲁替尼耐药相关的突变(47%;BTK,7例;PLCG2,2例)。
淋巴细胞删除性化疗和CD19 CAR-T细胞输注:
4例患者CAR-T细胞输注的剂量水平为DL1,19例为DL2,1例为DL3。初始再分期后,6例疾病持续或复发的患者接受了第二周期的淋巴细胞删除性化疗和CAR-T细胞输注。
体内CAR-T细胞峰值与血液中异常B细胞绝对计数、骨髓异常B细胞百分比、淋巴细胞删除性化疗前肿瘤横截面积之间具有正相关性;FDG狂热病患者中,CAR-T细胞扩增和CAR-T细胞最大标准摄入值之间具有负相关性。≥6个月时,定量聚合酶链反应检测到所有患者的血液中都具有CAR-T细胞(见图1)。
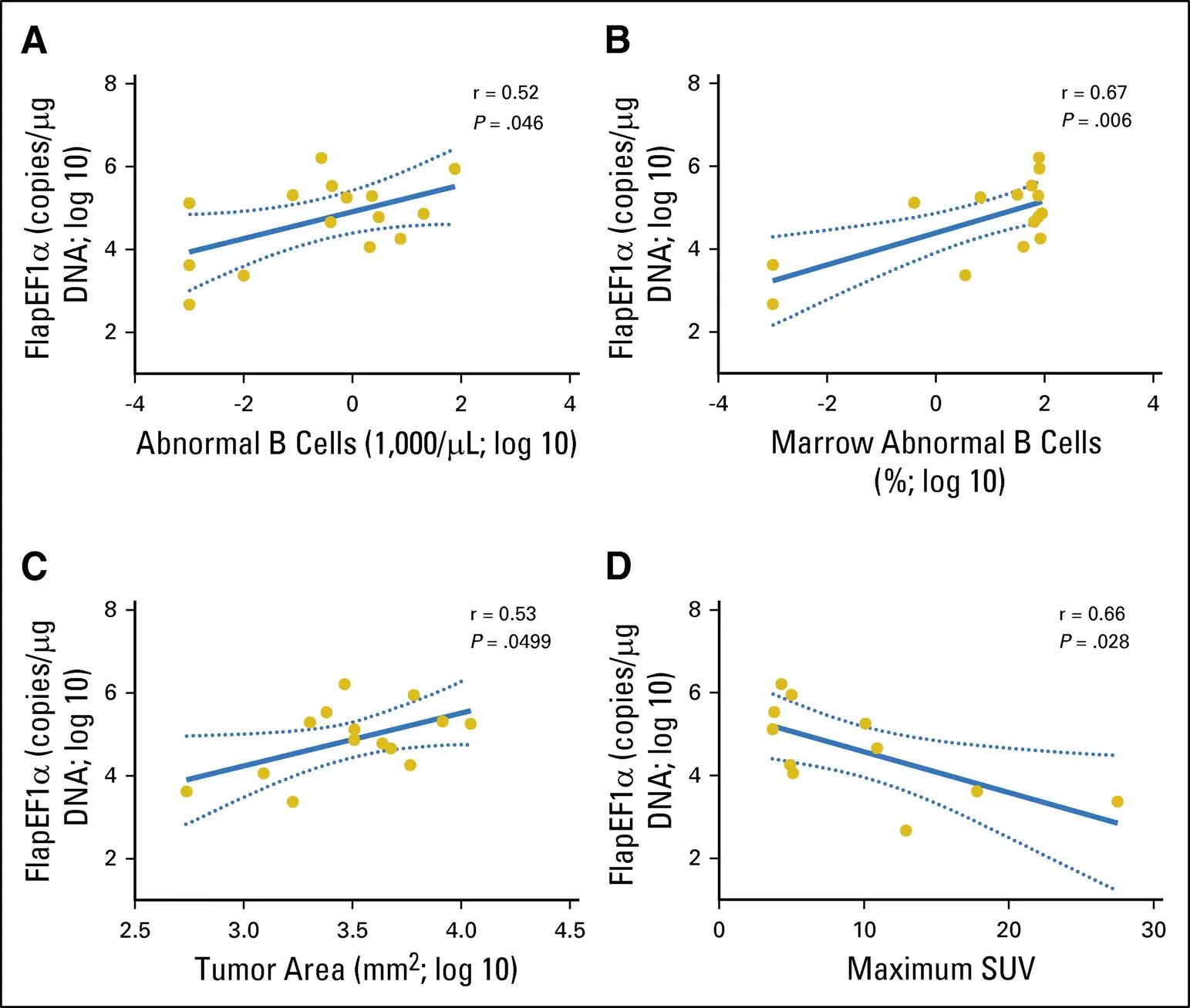
图1:血液中CAR-T细胞峰值与开始淋巴细胞删除性化疗前肿瘤负担的相关性
毒性评估:
多数患者出现了预期的淋巴细胞删除性化疗相关的毒性。20/24例患者出现细胞因子释放综合征(CRS),其中的18例为1~2级,1例为4级,1例为5级。8/24例患者出现神经毒性,其中的2例为1~2级,5例为3级,1例为5级。所有发生神经毒性的患者也发生了CRS。2例患者需要重症监护,其中的1例在输注2×106CAR-T细胞/kg后发生致命性神经毒性。其他患者的神经毒性可逆。
与CRS和神经毒性相关的因素:
单变量分析中,CAR-T细胞输注后的首个48小时内,发生≥2级神经毒性的患者具有较高的γ-干扰和白细胞介素-10水平。逐步多元回归分析中,也表现出了γ-干扰(P=0.034)和白细胞介素-10(P=0.045)与≥2级神经毒性之间的相关性(见图2)。
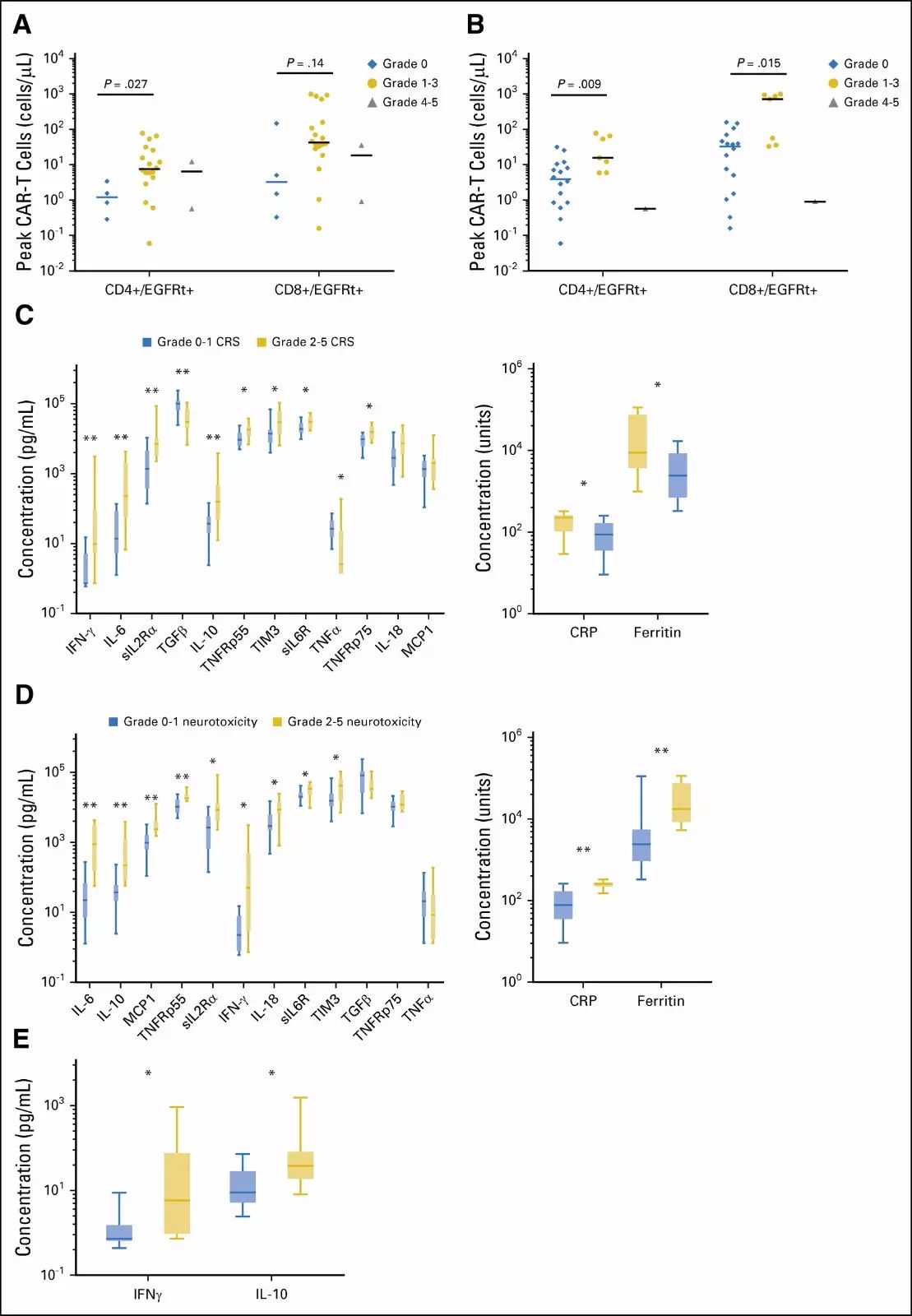
图2:与CRS和神经毒性相关的因素
淋巴结应答率:
CAR-T细胞输注后4周,IWCLL标准确定的总应答率(包括完全应答(CR)和/或部分应答(PR))为71%(17/24)。
20例患者接受了Cy+Flu的淋巴细胞删除性化疗,并以最大耐受剂量(≤2×106CAR-T细胞/kg)或以下接受了CD19 CAR-T细胞输注。根据IWCLL影像标准,其中19例患者在 CAR-T细胞输注后4周时,淋巴结应答率为74%(14/19;95% CI,49%~91%),CR率为21%(4/19),PR率为53%(10/19)。
与治疗失败相比,淋巴结应答与较长的无进展生存期(PFS)和总生存期(OS)相关;实现PR的患者,其PFS和OS非劣效于实现CR的患者(见图3)。
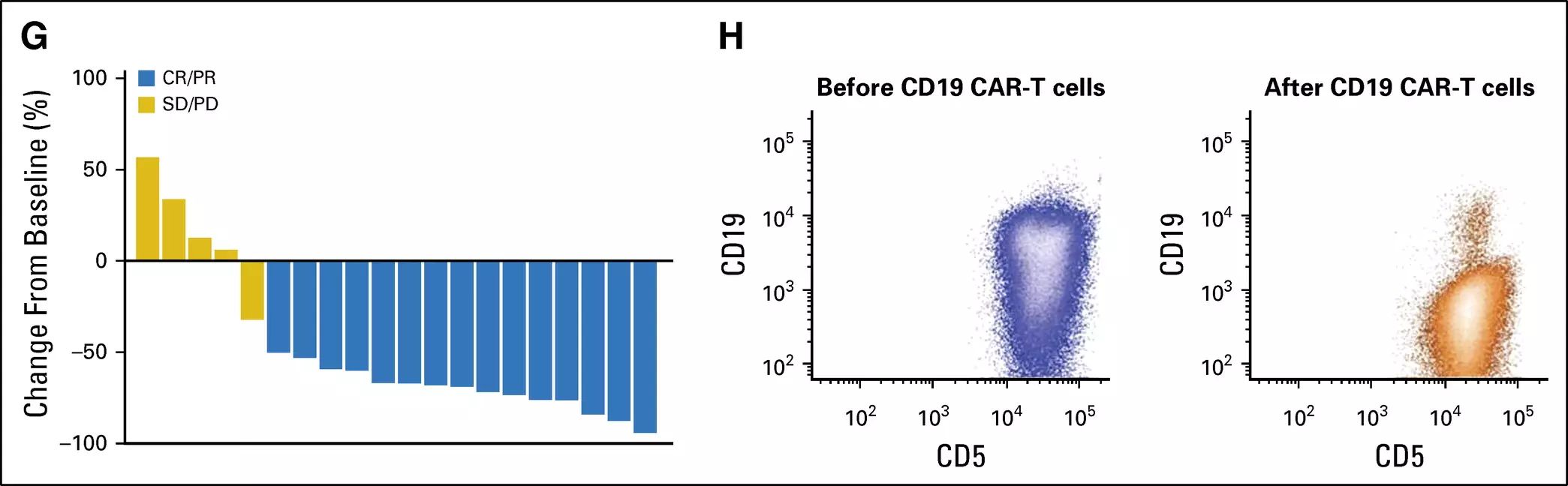
图3:与CAR-T细胞输注应答相关的因素
IGH序列与PFS和OS:
15/17例(88%)CAR-T细胞输注前骨髓受累的患者在CAR-T细胞输注后,流式细胞仪检查显示,骨髓病变完全清除。12例患者经深度IGH测序,其中7例患者(58%)的骨髓中未检测到恶性IGH序列。IWCLL标准确定具有应答的CLL患者中,骨髓中无恶性IGH克隆与CAR-T细胞免疫治疗后100%的无进展生存率和总生存率相关(中位随访6.6个月)。IWCLL标准确定的淋巴结PR或CR患者中,无进展生存率相似(见图4)。
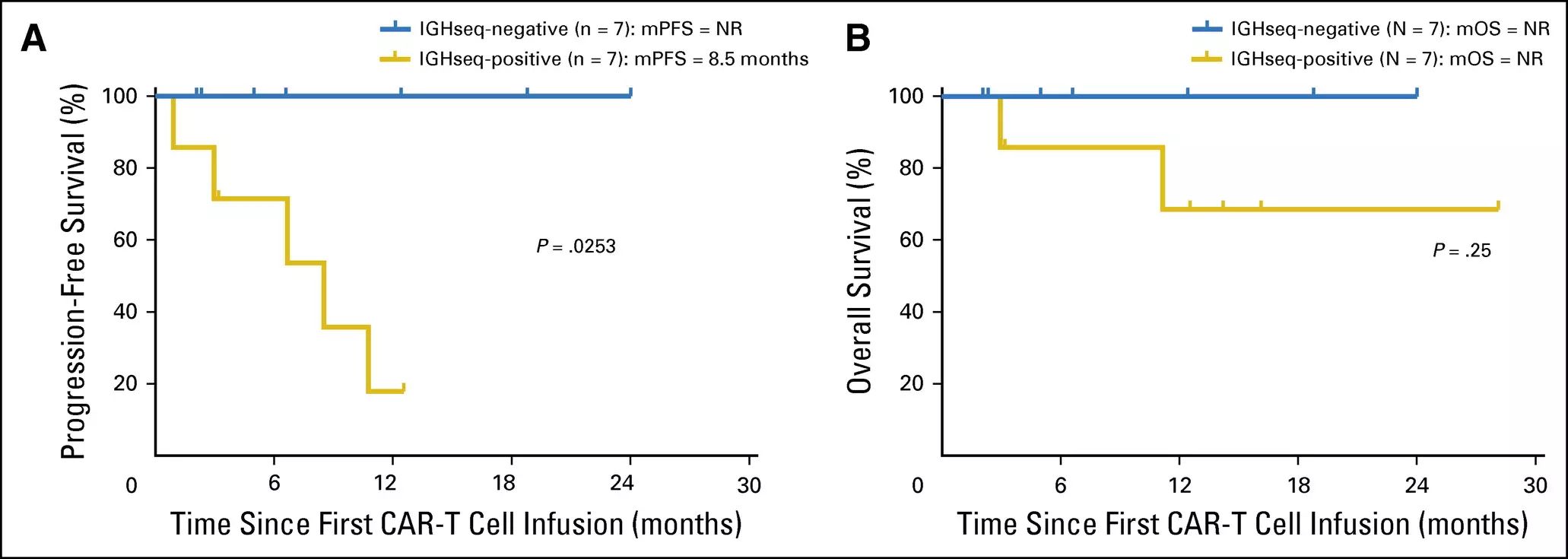
图4:IGH序列与PFS和OS之间的相关性
CD19 CAR-T细胞输注在依鲁替尼治疗失败后的高风险CLL患者中高度有效。
具有复杂细胞遗传学的复发和/或难治性CLL患者中,依鲁替尼治疗后具有较短的预期生存期。此研究表明,CAR-T细胞输注4周后,仅根据肿瘤大小而过早的对疾病再分期,并不是预后的最佳决定因素。需要进行额外的研究来确定,诸如IGH测序、PET影像或CAR-T细胞免疫治疗后延迟再分期等策略,能识别可从额外的CAR-T细胞输注中获益从而改善结局的患者。
虽然骨髓疾病对CAR-T治疗高度应答,但并不常见完全清除淋巴结病,这表明恶性淋巴结环境可能存在有损CAR-T细胞浸润和/或功能的因素。
本研究显示,肿瘤负担与CAR-T细胞扩增、CRS和神经毒性相关。因此,调整与肿瘤负担相关的CAR-T细胞输注剂量将进一步改善CLL患者的结局。
Durable Molecular Remissions in Chronic Lymphocytic Leukemia Treated With CD19-Specific Chimeric Antigen Receptor–Modified T Cells After Failure of Ibrutinib
http://ascopubs.org/doi/full/10.1200/JCO.2017.72.8519
19个肿瘤相关临床试验招募患者
点击下方图片即可查看详情














