正文

势不可挡的Checkpoint inhibitor:抗CTLA-4和抗PD-1/PD-L1系列药物,其神奇的疗效目前已经广为人知,国内外的各家药企早已经开始在多个瘤种中广泛开展临床研究,在黑色素瘤和肺癌中,免疫治疗更是取得了令人振奋的结果,已经成为一线治疗选择,其他实体肿瘤,如:淋巴瘤、胃,肠癌,肝癌,胰腺癌等瘤种也已经,或即将开展相关的临床研究,一片如火如荼的景象。
在临床研究中,药物相关不良反应的管理,被临床医生和各研发机构视为重中之重,其关注程度甚至超过了疗效本身。在机理上,免疫检查点抑制剂是针对宿主的治疗,与已有的化疗、靶向治疗、抗血管生成治疗等方式有着根本的不同。说白了,先前的治疗是在讨论如何直接消灭敌人,而现在的思路则是如何释放机体被抑制的免疫力,提高宿主自身的防御力。
抗CTLA-4和抗PD-1/PD-L1因其机理不同,分别作用于T细胞活化和杀伤肿瘤的不同阶段,打个比方来说,抗CTLA-4的作用是“动员预备役部队”,增加现役部队的数量;而抗PD-1/PD-L1则旨在增强现役部队的战斗力,增加肿瘤杀伤力度。两者作用的部位都在外周,抗CTLA-4主要作用在“兵营”---淋巴结,而后者则在“主战场”---肿瘤微环境中发挥作用。因此,两者引发的不良反应程度和类型也有差别。
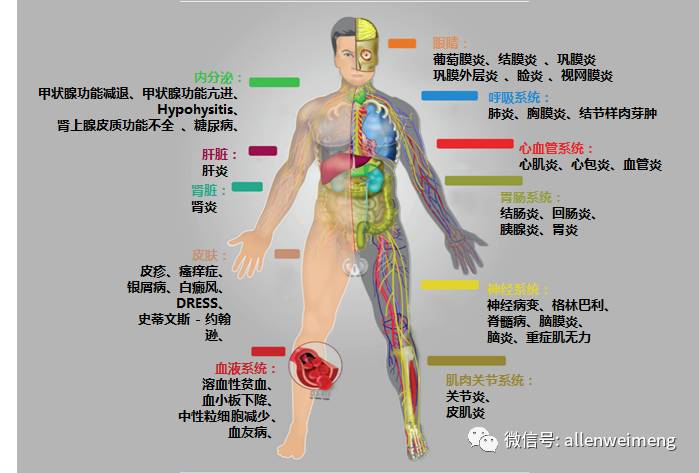
相比较而言,抗CTLA-4的不良反应发生率更高,涉及器官和系统更多,不良反应持续时间也更长。以ipilimumab为例,在3mg/kg体重的剂量下,大约60-85%的病人会发生不良反应,其中发生3-4级不良反应的患者占10-27%,在其第一个III期研究中,2.1%的病人因药物发生死亡。大部分不良反应发生在初次用药后的8-12周,最早发生的是皮肤反应。
对于抗PD-1/L1,最常见的不良反应是疲乏,发生率在两类药物中有微小差别,抗PD-1为16-37%,抗PD-L1为12-24%,前者略高,其中仅有很小的一部分的原因与甲状腺功能减退有关,目前两类药物造成疲乏和发生率差别的具体原因尚不清楚。无论是抗PD-1还是抗PD-L1,3-4级不良反应发生率都要低于抗CTLA-4,nivolumab治疗肺癌的CHECKMATE17&57的研究数据显示,3-4级不良反应发生率为10-19%左右;pembrolizumab治疗黑色素瘤的KEYNOTE-002研究中,3-4不良反应发生率为14%,在肺癌的KEYNOTE-010研究中数据相仿,对于2mg/kg和10mg/kg组分别为13%和16%。在Pembrolizumab获批一线治疗的扛鼎之作---KEYNOTE-024研究中,实验组为200mg定量,3周给药,3-4级不良反应发生率较前升高为26.6%,对照化疗组为73.4%,仍在可接受范围内。
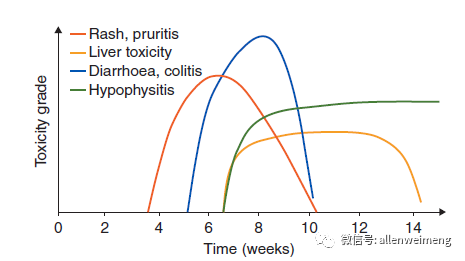
当anti-CTLA-4和anti-PD-1/L1联合应用时,严重不良反应的发生率会大幅提升,可达55%,而全部不良反应发生率为95%,可以说到了让人望而却步的地步。不仅如此,不良反应除了在药物联合应用的早期发生,当停止用药后,很多系统的不良反应仍会持续,不同系统不良反应的持续时间可见下图:

可见,皮肤、胃肠道及肝脏毒性都可以持续很长时间,尤其是在联合用药组。因此,免疫联合治疗目前仅仅在转移性黑色素瘤的治疗上获批,人们对于联合用药的安全性尚存很大顾虑。总体上看,irAE发生的时间一般都在用药后的数周到3个月内,但已有的经验显示首次不良反应发生时间最晚可能在停药后1年左右。另外,目前一些意见倾向于对于涉及器官(肝、肾、肺等)发生3-4级的不良反应需要依据组织活检进行确诊,而相关的组织活检诊断标准上还远未成形,包括取材的时机、部位、多少在内的流程,不同中心差别很大,因此,当临床一线需要参考病理医生的意见做出诊断时,提前告知病理医生是非常必要的。
另外,在开始治疗之前,对于病人的选择以及病人基线状态的评估,也是极其重要的,这在很大程度上关系到病人治疗的转归。举例来说,有文献表明,既往曾有自身免疫性疾病或正在接受治疗的患者,接受免疫检查点抑制剂治疗后,原有疾病加重的风险会显著增加;既往接受anti-CTLA4治疗出现不良反应的患者,再次接受anti-PD-1/L1治疗,发生不良反应的风险也会升高,vise versa,研究显示,3-4级不良反应发生率超过20%。















