近期发表在《Lancet Oncology》的III期、随机、安慰剂对照ACT IV试验,rindopepimut较安慰剂未显著改善生存,未达到主要研究终点。据悉,rindopepimut为针对EGFRvIII蛋白的免疫肽类疫苗,到此免疫疫苗治疗胶质瘤的尝试宣告失败。
前一阵热映的电视剧《我的前半生》中,最强丈母娘薛珍珠所患疾病为胶质瘤,这是脑部最常见的恶性肿瘤。对于脑胶质瘤,其标准治疗是尽可能切除肿瘤,同步放疗后替莫唑胺维持治疗,中位生存期15个月,随治疗的进展OS可延长至20.5个月。复发患者治疗手段包括二次手术、再放疗、烷化剂化疗。胶质瘤预后差,相关因素包括PS评分低、老年、切除不完全、DNA修复基因启动子的甲基化。因而胶质瘤亟需新的治疗,而免疫治疗成为临床研究重要的领域。
临床显示,超过40%胶质瘤存在EGFR基因扩增,最常见是外显子2~7的缺失突变,即表皮生长因子受体III型突变体(EGFRvIII),其中20%~30%胶质瘤存在EGFRvIII过表达。因EGFRvIII突变具有免疫原性,所以靶向定位肿瘤特异分子EGFRvIII的免疫治疗疫苗rindopepimut得以开发。
在Ⅱ期研究中,rindopepimut治疗胶质瘤的中位PFS为15个月,OS为24个月。而其III期(ACT IV研究)随机、安慰剂对照试验,目的是对比标准替莫唑胺,rindopepimut联合替莫唑胺是否延长生存期。
该研究纳入22个国家165家医院
。
患者年龄≥18岁,且为新诊断EGFRvIII表达胶质瘤,RT-PCR法检测EGFRvIII。最大程度切除肿瘤,完成标准同步放化疗(60Gy,替莫唑胺75mg/m
2
/天)。
放化疗期间疾病进展、额外抗肿瘤治疗、地塞米松使用剂量超过2mg、ECOG评分3分或3分以上、弥漫性脑膜转移。利用脑MR进行独立影像学评估。
DNA修复基因启动子的甲基化(MGMT)、EORTC递归分割分析类(Ⅲ、Ⅳ对比Ⅴ)。1:1随机分组,所有患者均接受标准替莫唑胺维持治疗(150~200 mg/m²,d1~5,28天一周期),rindopepimut组剂量500 µg+150µgGM-CSF,对照组给予150µg蓝白血清。
为微小残留病灶(MRD放化疗后<2cm
2
=患者的OS。
1. 2012年8月~2014年12月,筛查患者4652例,有足够标本进行EGFRvIII表达分析4519例,EGFRvIII表达阳性患者1345例,阳性率30%。研究纳入患者745例,其中,不可评价2例,微小残留病灶(MRD)405例,显著残留病灶(SRD)338例。随机分组对照组374例,rindopepimut组371例。
2. 2015年10月24日进行中期分析,rindopepimut组与对照组比较OS的HR为0.99,提示OS无获益试验提前终止。2016年4月29日进行最终分析,死亡523例。在MRD患者中,两组OS无差异,rindopepimut组和对照组中位OS分别为20.1个月和20.0个月(HR1.01,P=0.93),见图1。整组患者中,rindopepimut组和对照组中位OS分别为17.4个月和17.4个月(HR0.89,P=0.22),见图2。在SRD人群中,rindopepimut组和对照组中位OS分别为14.8个月和14.1个月(HR0.79,P=0.06)。
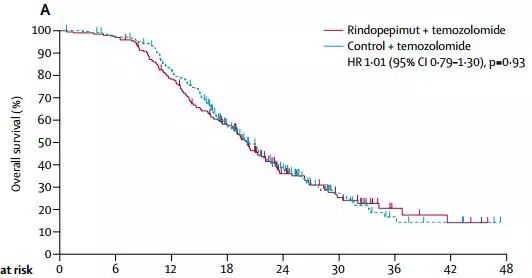
图1:在微小残留病灶患者中rindopepimut组和对照组OS曲线
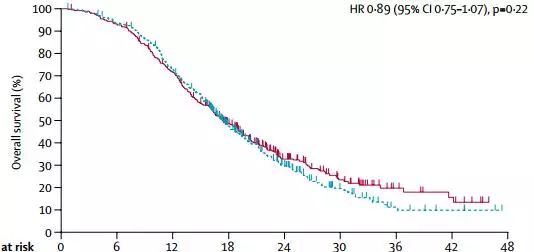
图2:在整组患者中rindopepimut组和对照组OS曲线
在探索性分析中,rindopepimut组和对照组2年生存率分别为30%对比19%(P=0.029)。
在MRD患者中,rindopepimut组和对照组中位PFS分别为8.0个月和7.1个月(HR1.01,P=0.91)。整组患者中,rindopepimut组和对照组中位PFS分别为7.1个月和5.6个月(HR0.94,P=0.51)。在SRD人群,rindopepimut组和对照组中位PFS分别为3.7个月和3.7个月(HR086,P=0.28)。
3. 最常见3~4级不良事件:rindopepimut组和对照组血小板减少发生率分别为9%对比6%,乏力2%对比5%,脑水肿2%对比3%,惊厥2%对比2%,头痛2%对比3%;严重不良事件惊厥5%对比6%,脑水肿2%对比3%,治疗相关死亡16例(rindopepimut组和对照组发生率分别为4%对比3%)。1例64岁男性rindopepimut治疗11个月后出现肺栓塞考虑与治疗有关。
Rindopepimut未能改善新诊断胶质瘤生存期,下一步将考察其与免疫治疗联合的效果。
临床失败的治疗性疫苗不止rindopepimut一个!
ICT-107的III期临床研究,因开发这一疫苗的美国生物技术公司未能获得研究所需的资金而停止;
另一进入III期临床研究的DCVax疫苗,包含激活的经训树突细胞,能够调动成百上千的T细胞和其他免疫细胞,产生持续的免疫反应,强力清除体内的肿瘤细胞。临床研究证实,使用DCVax的脑瘤患者生存期延长了1倍以上。此外,DCVax疫苗没有明显的副作用。
2014年在英国获得突破性药物资格,三期在进行
。
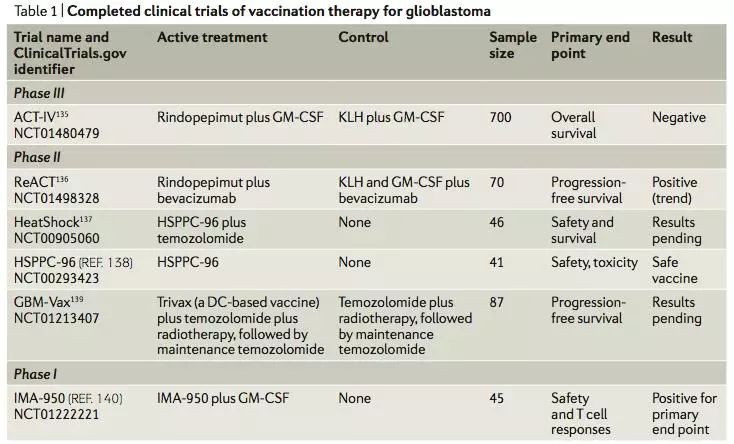
2. 正在进行的胶质母细胞瘤的治疗性疫苗的临床试验
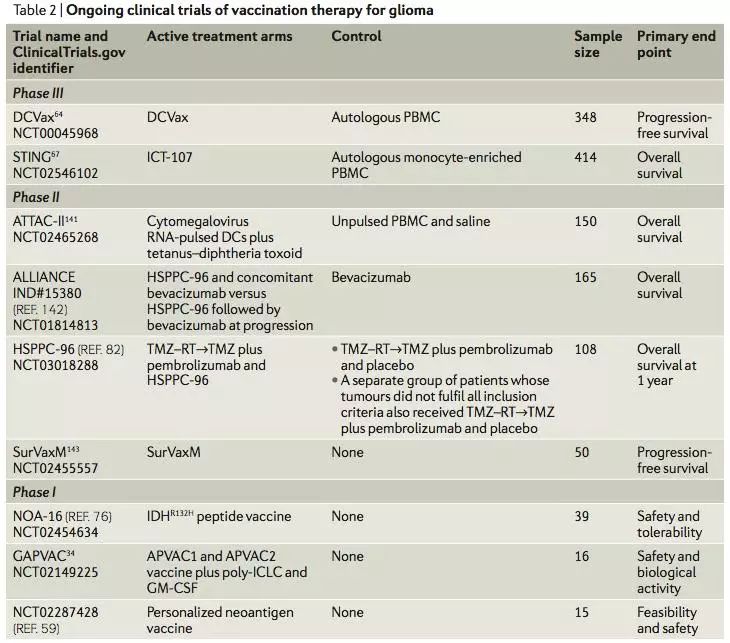
如树突状细胞疫苗,HSPPC-96,特定的IDH
R132H
疫苗,巨细胞病毒蛋白等。
ACT IV试验没有达到首要研究终点,即Rindopepimut治疗EGFRvIII阳性微小残留病灶的胶质瘤失败。在该研究中MRD定义为<2cm,既往研究定义为<1cm。接受Rindopepimut治疗患者中位OS为20.1个月,与既往同类人群非随机对照研究类似,但是对照组数据好于既往研究。对照组使用蓝白血清是否对免疫功能有影响目前还没有结论。该研究失败原因可能有:
第一
,利用历史数据来推算对照组数据可能不可靠,因为患者选择难以控制;
第二
,EGFRvIII表达在放化疗后可能出现丢失,目前还没有明确数据;
第三
,既往体液反应作为疗效预测指标,该研究未证明此结论;
第四
,生物标准物不稳定,多肽疫苗Rindopepimut劣于非多肽疫苗。
1. Rindopepimut with temozolomide for patients with newly diagnosed, EGFRvIII -expressing glioblastoma (ACT IV): a randomised, double-blind, international phase 3 trial. Lancet Oncology.Published:22 August 2017.
2. Vaccine-based immunotherapeutic approaches to gliomas and beyond. NatureReviewsNeurology. 2017.5.12. doi:10.1038/nrneurol.2017.64
19个肿瘤相关临床试验招募患者
点击下方图片即可查看详情






