来源:
黑龙江省食品药品监督管理局
2017年06月29日,
黑龙江省食品药品监督管理局发布《
关于督促生化药品生产企业对生产条件进行升级改造及摸底调查的通知》,详情如下:
关于督促生化药品生产企业对生产条件进行升级改造及摸底调查的通知
全省生化药品生产企业:
根据《药品生产质量管理规范(2010年修订)》第三百一十条规定,国家食品药品监督管理总局于
2017年3月16日
发布生化药品附录,作为《药品生产质量管理规范(2010年修订)》配套文件,将于
2017年9月1日起正式施行
。与之前生化药品生产要求相比较,《生化药品GMP附录》的颁布,对企业在
供应链管理、厂房与设备、病毒去除/灭活及验证等方面进行了细化,对质量管理体系建设提出了新的硬性要求。
鉴于此,从附录的颁布到正式实施,总局给予了企业
6个月的升级改造时间。
自9月1日起,生化药品的生产必须符合该附录的相关要求。
附录颁布以来,省内部分生产企业主动谋划、积极应对,对照附录提出的新标准、新要求,对现有的软硬件条件进行了升级改造,已基本上完成了相关工作。但也有一部分企业行动迟缓,对附录的颁布没有引起充分的重视,对今后的监管形式没有一个清醒的认识。对于这部分企业,要尽快对现有生产软硬件条件进行充分的评估,采取有效措施以符合规范要求。
企业对现有生产车间、生产线的改建,如触及国家总局《药品生产质量管理规范认证管理办法》
第八条规定的
,
应向我局提出药品GMP认证申请,通过认证后,方可在改建后的生产车间、生产线上生产药品。
省局将密切跟踪国家总局关于生化药品出台的工作政策、要求和指南,并将在第一时间转发至相关企业。
为全面了解省内
生化药品企业改造进度和存在的问题
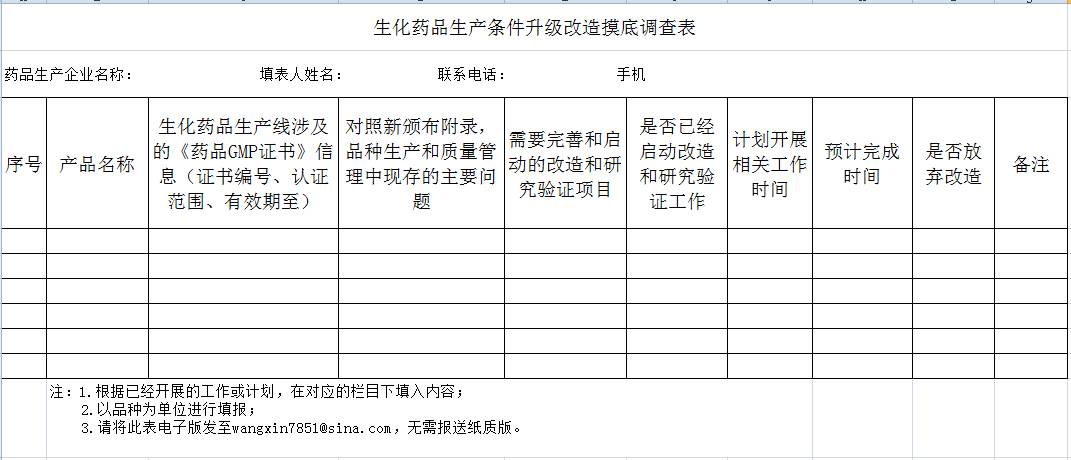
,省局决定对企业升级改造情况进行摸底调查,
请生化药品生产关企业于7月14日前将调查表(附后)电子版发送至[email protected]。
黑龙江省食品药品监督管理局
2017年6月29日