在2017ASCO年会“转移性非小细胞肺癌”壁报专场上,4项关于EGFR突变型晚期NSCLC靶向治疗优化和耐药机制探索的摘要入选壁报讨论,并邀请韩国安明珠教授进行现场点评。以下展示研究内容和专家点评。9017 奥希替尼对比多西他赛联合贝伐珠单抗(A+T)用于EGFR T790M突变型NSCLC的三线治疗
这一III期研究,入组既往接受过EGFR-TKI和一线化疗的EGFR突变型晚期非鳞NSCLC,组织或血浆检测EGFR T790M突变的患者。1:1随机接受奥希替尼(80mg/天)或T(75mg/m2)+ A(7.5mg/kg),用药直至疾病进展或不可耐受的毒性。A+T组患者进展后可交叉接受奥希替尼。主要终点为无进展生存期(PFS),次要终点为客观缓解率(ORR),毒性和总生存期(OS)。
【编者注】这项研究是中国青岛中心医院/青岛大学的研究者完成的
147例患者接受治疗,奥希替尼组和A+T组分别有74和73例;两组中位PFS分别为10.2m和2.95m(HR 0.23;95%CI,0.12-0.38;P<0.0001)。奥希替尼组的ORR和DCR分别为61.6%和87.6%;A+T组分别为8.3%和43.0%。
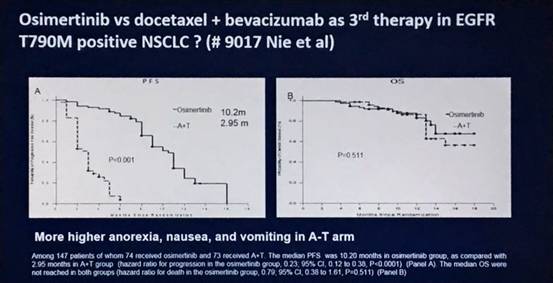
结论:EGFR T790M突变的NSCLC三线治疗,奥希替尼的ORR和PFS均显著优于A+T。
点评
对比既往临床研究数据(AURA I期、AURA II期研究汇总分析和AURA3),这一研究中奥希替尼组用于EGFR T790M突变NSCLC三线治疗的ORR(61.6%)和PFS(10.2m)与之相当。据AURA3的阳性结果,奥希替尼应被推荐作为EGFR-TKI耐药后T790M突变NSCLC的二线治疗。这一研究中,A+T组的疗效不佳,这一方案用于EGFR-TKI耐药后T790M突变NSCLC三线治疗的作用不详。

9018 血浆中突变型EGFR的完全清除预测奥希替尼疗效
入组AURA I期研究中EGFR-TKIs耐药后,组织或血浆检测EGFR T790M突变的患者。收集基线和奥希替尼(20-240mg)治疗6周后的血浆,采用BEAMing 数字PCR检测血浆中的EGFR突变(Ex19del,L858R和T790M)。在基线可检测到EGFR突变的患者中,对比治疗6周后血浆中有或无EGFR突变患者的疗效。
160例基线T790突变的患者,143例基线血浆检测到EGFR突变。这一队列的中位PFS为9.3m(95%CI:8.2-9.7)。治疗6周后,92例患者血浆中突变型EGFR完全清除(92/143,64%),这些患者的中位PFS(10.8m)显著优于血浆中仍存在突变EGFR的患者(4.2m);两组ORR亦有显著差异(74% vs. 41%)。
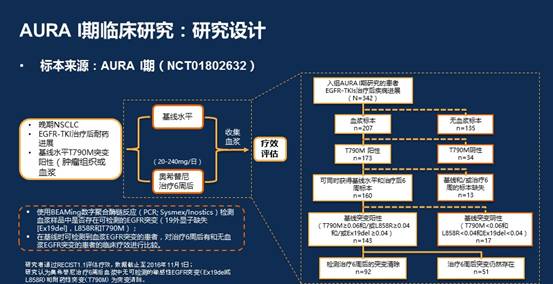
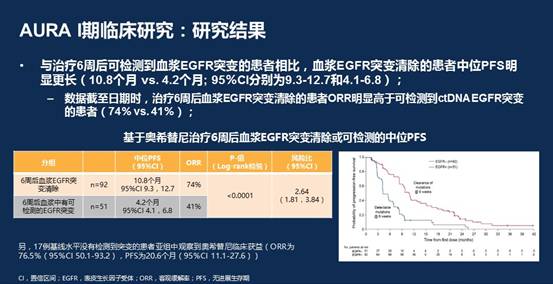
结论: EGFR T790M突变患者接受奥希替尼6周后,如血浆中突变型EGFR完全清除,预示更好的ORR和PFS。
点评
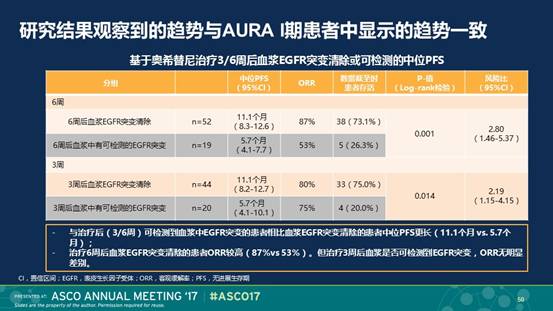
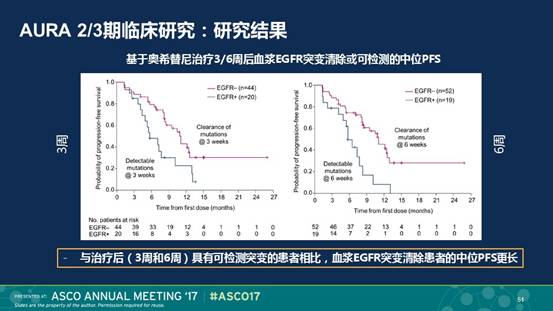
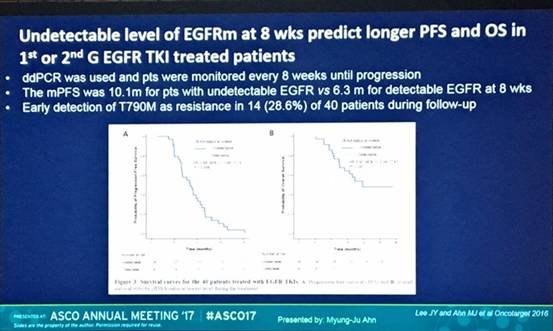
AURA 2/3的探索分析也发现奥希替尼治疗3和6周后,血浆中突变EGFR清除与未清除的患者,ORR和PFS存在显著差异(3周:11.1m vs 5.7 m, 80% vs 75%; 6周:11.1m vs 5.7m, 87% vs 53%)。另一个在2016年发表的奥希替尼治疗8周后血浆中EGFR突变清除情况的比较也支持这个结论。
基于此可提出假设,一或二代EGFR-TKIs耐药后EGFR T790M突变患者存在异质性。有些患者可能同时合并其他耐药突变,接受奥希替尼治疗的PFS较短,治疗过程中,非EGFR T790M突变的耐药克隆介导早期耐药。
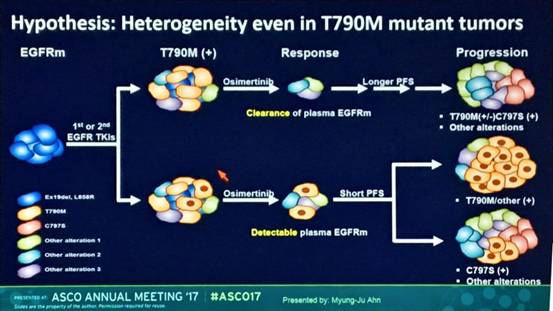
小结:奥希替尼治疗6周后,血浆中突变型EGFR的有无可预测其临床疗效。然而,本研究的样本量较小,仍需更多的研究来验证。耐药患者仅检测EGFR T790M突变是不够的,尤其是6周后血浆中仍存在EGFR突变的患者,明确是否存在共存的耐药机制,可指导后续治疗。
9019 随机开放的II期研究:EGFR突变型晚期NSCLC接受一线的厄洛替尼(E)8周诱导治疗后,疾病稳定的患者1:1分配接受E联合或不联合MET单抗emibetuzumab(Emi)治疗
EGFR突变型晚期NSCLC接受一线E 8周诱导治疗后,稳定患者1:1随机接受Emi(750mg,IV,q2w)+E或E单药。分层因素包括ECOG PS评分,种族,MET表达水平和诱导治疗的疗效。主要终点为随机后的PFS,次要终点包括安全性、OS、PK和探索性分析MET表达的患者。入组181例患者,141例参与随机(Emi+E组71例;E组70例)。ITT人群中,Emi+E组的中位PFS为9.3m,E组为9.5m,无显著差异(HR=0.89;90% CI 0.64-1.23; p = 0.534)。探索性分析MET高表达的患者(定义为≥90%的肿瘤细胞MET 3+;n=24),可从Emi+E治疗中显著获益(EMI+E: 20.7 m;E: 5.4 m [HR: 0.39;90%CI: 0.17-0.91])。而其他患者,两组PFS无差异(HR:1.1[95%CI:0.7-1.7])。ITT人群中,两组的中位OS均未达到。MET高表达的患者中,E组的中位OS为20.6m(90%CI:8.87,NA);Emi+E组未达到(90%CI:NA,NA)。这一研究,ITT人群未发现PFS的显著差异。探索性分析发现MET高表达,接受E单药治疗的患者预后较差,提示这类患者可能会从Emi+E联合治疗中获益。
点评
在EGFR突变型NSCLC中,MET高表达是预后更差的标志物。既往研究,回顾性分析1199例NSCLC,探索MET表达与EGFR-TKI疗效的关系。发现c-MET无表达,表达+,2+,3+的患者比例分别为10.8%、41%、32.5%,15.7%。其中262例EGFR突变的患者,83例接受了一线EGFR-TKI治疗。EGFR突变对比野生型患者,c-MET表达更强。c-MET阳性的患者对比阴性患者,接受EGFR-TKI治疗的中位PFS显著更短(4.3m vs. 11.9m,P=0.015)。
以上研究进一步支持MET高表达是厄洛替尼的负性预测标志物。但在未加选择的EGFR突变型NSCLC一线治疗中,联合治疗并不能改善PFS。尽管MET高表达的患者能从联合治疗中获益,但探索性分析的结果因谨慎解读。应进行后续研究探索,采用相应的生物标志物来筛选合适的EGFR突变患者,接受MET和EGFR抑制剂的联合治疗。
9020 MET扩增是奥希替尼的耐药机制之一
23例奥希替尼耐药患者,组织和血浆ctDNA分别进行NGS检测,并用FISH法检测组织中的EGFR和MET扩增。其中,13例患者在奥希替尼前接受过3代EGFR-TKI治疗(rociletinib 11例,ASP8273和EGF816各1例)。标本类型:组织(16例),血浆(18例),两者均有(11例)。
奥希替尼耐药后的组织或血浆检测结果见下表1。所有患者仍检测到EGFR突变, 15例(15/23,65%)患者在奥希替尼治疗后T790M消失。常见的耐药机制为MET扩增(7/23;30%)和EGFR C797S突变(5/23;22%)。SCLC转化,PIK3CA E545K/PIK3CA扩增和FGFR1 D60N/FGFR扩增患者各1例。

2例有不同部位的活检组织的患者,存在耐药异质性。第8例患者血浆和肺结节均有C797S/T790M突变,但纵隔淋巴结活检两位点均为野生型。第22例患者胸腔积液有MET扩增,但肺病灶未发现。同时有组织和血浆的11例患者中,2例患者在血浆中发现的耐药突变,但组织中未发现。7例MET扩增的患者,3例接受了EGFR/MET TKI的联合治疗,均取得了PR。
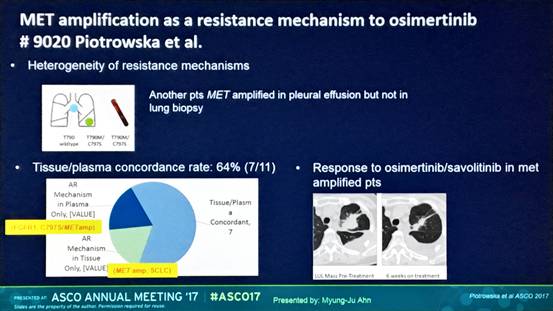
在这一奥希替尼耐药队列中,MET扩增发生率高于一线TKIs耐药的患者,且患者对EGFR+MET TKIs的联合治疗有反应。耐药的异质性,强调了组织和血浆检测互为补充的重要性。
表1.奥希替尼耐药后的组织或血浆检测结果
表1.奥希替尼耐药后的组织或血浆检测结果

点评
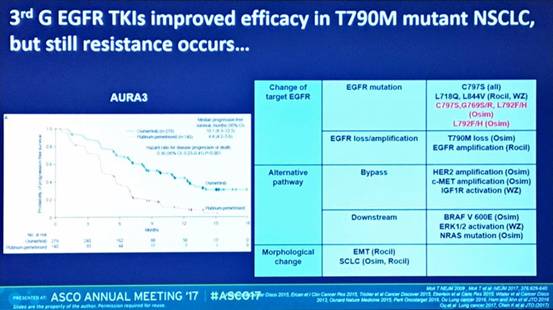
目前3代EGFR-TKI报道的常见耐药机制包括:1. EGFR位点改变:3次突变(如C797S),EGFR T790M消失和EGFR扩增;2. 旁路激活:HER2扩增,c-MET扩增;3. 表型改变:EMT,小细胞转化。
这一研究采用NGS检测23例奥希替尼耐药后的患者肿瘤组织和外周血(并不是所有患者都有配对的组织和血浆),发现MET扩增是最常见的耐药机制,占30%。比较组织和血浆标本,或不同部位的组织标本,发现患者存在耐药异质性。值得注意的是,3例MET扩增的患者,接受奥希替尼+savolitinib联合治疗后,均取得PR。这一研究与既往报道稍有不同。Oxnard GR等对67例奥希替尼耐药患者检测发现:48%患者T790M突变消失,30%为T790M(+)/C797S(-),22%为T790M(+)/C797S(+)。15例患者进行血浆NGS,发现HER2扩增,MET扩增和BRAF突变的患者各1例。
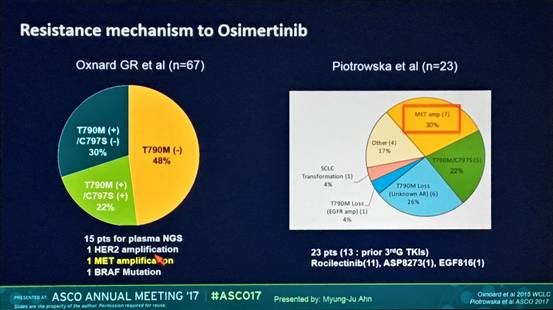
在本研究中,c-MET扩增是奥希替尼最常见的耐药机制。我们需要注意到13例患者既往接受过其他的3代TKI治疗,意味着研究队列是一类异质性更大的群体,可能不能代表奥希替尼真正的耐药机制。基于c-MET扩增较高的发生率,后续需要进一步评估奥希替尼联合c-MET抑制剂联合治疗用于耐药患者中的疗效。对于3代TKI耐药的患者,应鼓励进行重复活检,明确耐药机制,并根据耐药机制进行后续的研究。目前,奥希替尼用于EGFR突变型NSCLC一线治疗的研究正在进行(FLAURA研究),其耐药机制可能不同于二线或以上治疗,同样值得研究探索。
点评总结
EGFR突变型NSCLC进行联合靶向治疗的临床研究时,需重视基于生物标志物的入组人群筛选。
EGFR T790M突变的NSCLC是一类异质性较大的群体,需明确患者是否合并其他共存的耐药突变。
第3代EGFR-TKI的耐药机制较为复杂,明确是否同时存在不同的耐药突变,并据耐药机制寻找合适的新的治疗策略,加以验证。
版权属肿瘤资讯所有。欢迎个人转发分享。其他任何媒体、网站如需转载或引用本网版权所有内容须获得授权且在醒目位置处注明“转自:肿瘤资讯"















