▎药明康德/报道
礼来(Eli Lilly)和Incyte公司近日宣布,将在2018年1月底之前,向美国FDA重新提交其潜在重磅新药baricitinib的新药申请(NDA)。Baricitinib是一种还在试验中的口服药物,用于中度至重度类风湿性关节炎(RA)的治疗。

2017年4月,美国FDA颁发了关于baricitinib上市申请的完全回应函。在参考FDA修改建议的基础上,此次重新提交的申请材料包括baricitinib的全新安全和功效数据。据两家公司预计,FDA会将该申请划入II类重新提交这一类别,这意味着baricitinib将经历一个六个月的审查周期。
类风湿性关节炎是一种全身性自身免疫性疾病,其特征是炎症和关节的逐渐损伤。全球有超过2300万人患有类风湿性关节炎,其中女性患者的数量是男性患者的三倍。当前,类风湿性关节炎的治疗手段包括使用非甾体抗炎药,口服型的常规合成疾病缓解性抗风湿药物(csDMARDs),以及可注射的生物性疾病缓解性抗风湿药物(bDMARDs)。尽管目前针对类风湿性关节炎的治疗方案有很多,但许多患者的症状并没有得到持续缓解。因此,我们仍然需要新型的治疗手段,来改善该疾病患者的整体状况。
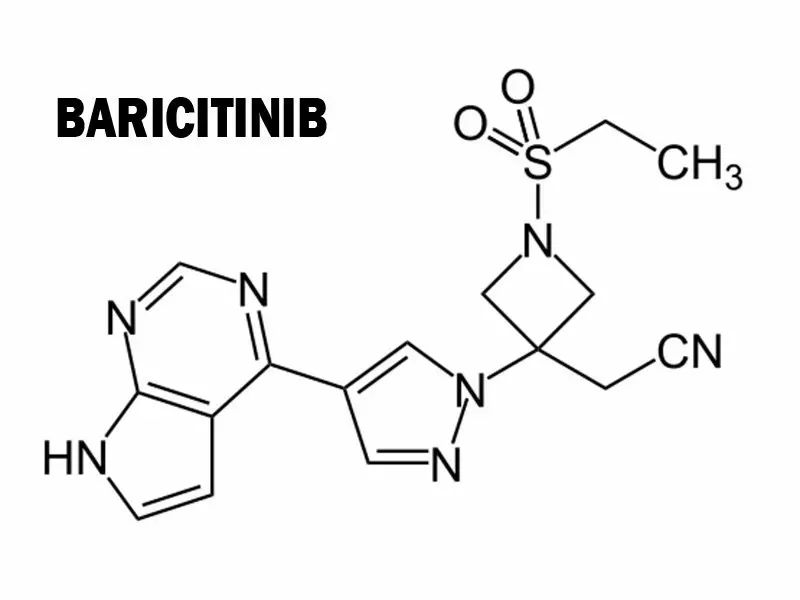
▲Baricitinib的分子结构(图片来源:piktochart)
Baricitinib是一种每日一次的口服JAK抑制剂,目前处于针对炎性和自身免疫性疾病的临床研究阶段。已知的JAK酶一共有四种:JAK1,JAK2,JAK3和TYK2。 JAK依赖性细胞因子与许多炎性和自身免疫性疾病的发病机制有关。这一特性表明,JAK抑制剂可用于炎症的广泛治疗,这其中也包括类风湿性关节炎的治疗。
礼来和Incyte公司在中度至重度活动性类风湿关节炎患者中进行了四项关键性3期临床试验,并且都取得了成功。在这四项研究中,其中两项是和已经批准的疾病缓解性抗风湿药物(DMARDs)的比较试验。最近,两家公司又结束了另外一个3期临床试验,以支持baricitinib在中国的临床开发。这些临床试验计划面向广大患者,包括了那些对甲氨蝶呤无反应、对甲氨蝶呤反应不足、对cDMARD反应不足或对TNF抑制剂的反应不足的患者群体。参与并完成任意一个3期研究的患者都可以参加一个长期的扩展研究。
2009年12月,礼来和Incyte公布了一项独家全球许可合作协议,用于baricitinib和某些后续化合物的开发和商业化,以造福患有炎症和自身免疫性疾病的患者。 2016年,baricitinib已经在美国、欧盟和日本市场提交了上市批准,用于治疗类风湿性关节炎。到目前为止,baricitinib已分别于2017年2月和2017年7月在欧盟和日本获得上市批准。

▲礼来高级副总裁Christi Shaw女士(图片来源:礼来官网)
“我们致力于为类风湿性关节炎患者提供更好的生活。尽管现有的治疗方法有很多,但是仍然不能满足对这类使人衰弱的疾病的治愈需求,”礼来公司高级副总裁Christi Shaw女士表示:“我们很高兴有重新递交baricitinib上市申请的机会,同时也希望继续与FDA合作,早日将baricitinib带给患有类风湿性关节炎的患者。”
感谢礼来和Incyte研发人员永不放弃的精神。同时,我们也希望baricitinib可以顺利通过FDA的上市审批,从而造福更多患有类风湿性关节炎的患者。
参考资料:
[1] Rejected Only A Few Weeks Ago, Eli Lilly (LLY) Will Resubmit NDA App For Potential RA Blockbuster In Just 5 Months
[2] Eli Lilly and Company官网
















