原料药:共18个评价指标,分为4个否决项、8个较大缺陷项、6个一 般缺陷项。
制 剂:共39个评价指标,分为6个否决项、8个较大缺陷项、25个 一般缺陷项。
原料药: 合成路线、Ⅰ类溶剂使用、起始原料工艺和质量标准、生产工艺过程控制、关键工艺步骤、中间体控制、样品试制和工艺验证等。评价提交的工艺研究资料是否完整,研究项目的缺失是否会影响到申报资料的可评价性。
制剂: 辅料证明性文件和内控标准、与制剂性能相关的原料药关键理化性质研究、处方筛选、原辅料相容性研究、注射剂灭菌/无菌工艺验证、包材相容性、容器密封性等。
原料药关注点之一:工艺路线的选择
原料药关注点之二: 起始物料控制
原料药关注点之三: 关键步骤和中间体的确认
原料药关注点之四:工艺过程监控与验证
1) 提供工艺路线的选择依据,重视对基因毒性杂质的分析与控制。
2) 提供详细的研究资料(包括研究方法、研究结果和研究结论)以说明关键步骤、工艺参数关键中间体质控参数确定的合理性。
3) 详细说明在工艺开发过程中生产工艺(包括批量、设备等)的主要变化及相关研究资料。
4) 提供工艺研究数据汇总表。
5) 如现有设备与批量与大生产不一致,则应在此部分提供必要的放大研究资料。
1) 未提供工艺路线的选择依据。
2) 未提供相应的研究资料来以说明关键步骤确定的合理性以及工艺参数控制范围的合理性,或资料不够详细。
3) 未详细说明在工艺开发过程中生产工艺的主要变化,或未提供相关的支持性研究资料。
4) 工艺研究数据汇总表中的数据不全面,缺乏工艺筛选、优化与放大研究阶段的数据。
1、工艺路线的选择和优化
文献报道本品的合成路线主要有以下两条:略----
因相关文献报道的合成工艺较长,工艺较难控制。故采用起始物料1与三甲基硅基咪唑反应,一步合成消旋体,并通过拆分,和盐酸盐转化,最后合成XXXX盐酸盐。起始原料简单,条件易控,操作简单,产品质量和收率较高。
2、优化的工艺包括如下步骤
1)第一步偶联反应,优化了反应温度,制备了一些异构体杂质和其他可能的杂质,并开发了手性分离方法和纯度检测方法。
2)第二步化学拆分,优化了拆分试剂L-酒石酸的用量,溶剂的用量,以及升降温的速度和搅拌的速度对产品手性纯度的影响,将降温速度控制在3小时以内降温到0±3℃,搅拌的的速度控制在200~300转/分钟。确定了最优的合成工艺,提高了拆分的效率。
3)第三步盐酸盐置换,因为该药物是注射剂,产品中的灰分对质量影响很大,故在合成工艺中通过多次水洗的方法将灰分控制到很低,满足了制剂的要求。并重点研究了水分对产品晶型的影响,确定将水分控制在0.5%以下,可得到稳定的晶型。
工艺研究数据汇总表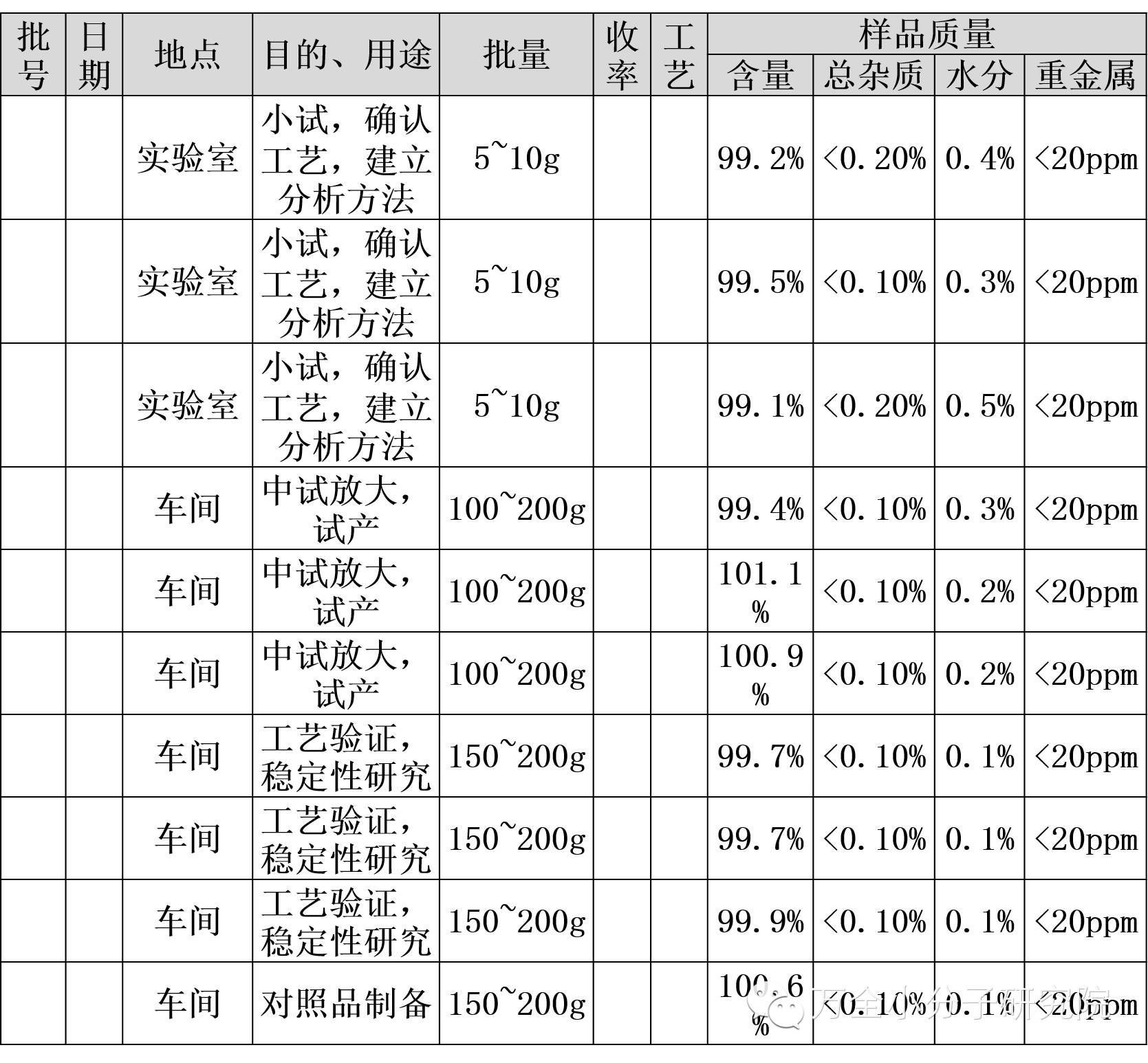
存在问题:
1)工艺路线优化过程较粗略,未提供相应的研究资料说明关键步骤确定的合理性, 关键工艺参数控制范围的合理性;
2)未说明工艺开发过程中,生产工艺有哪些主要变化,进行了哪些支持性的验证研究。
1. 文献合成路线汇总
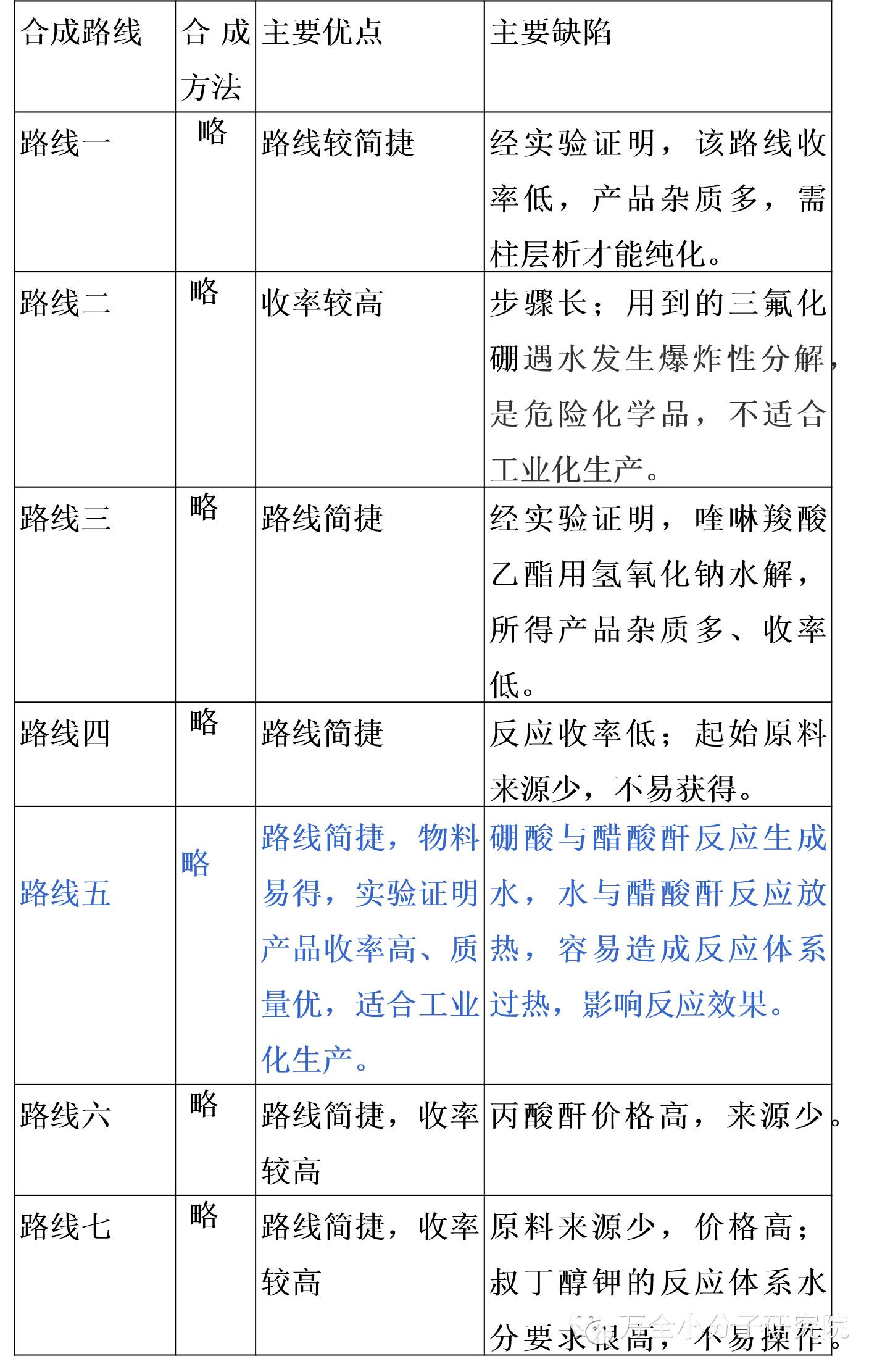
2.工艺的选择与优化
1)环合反应工艺参数摸索过程和结果汇总
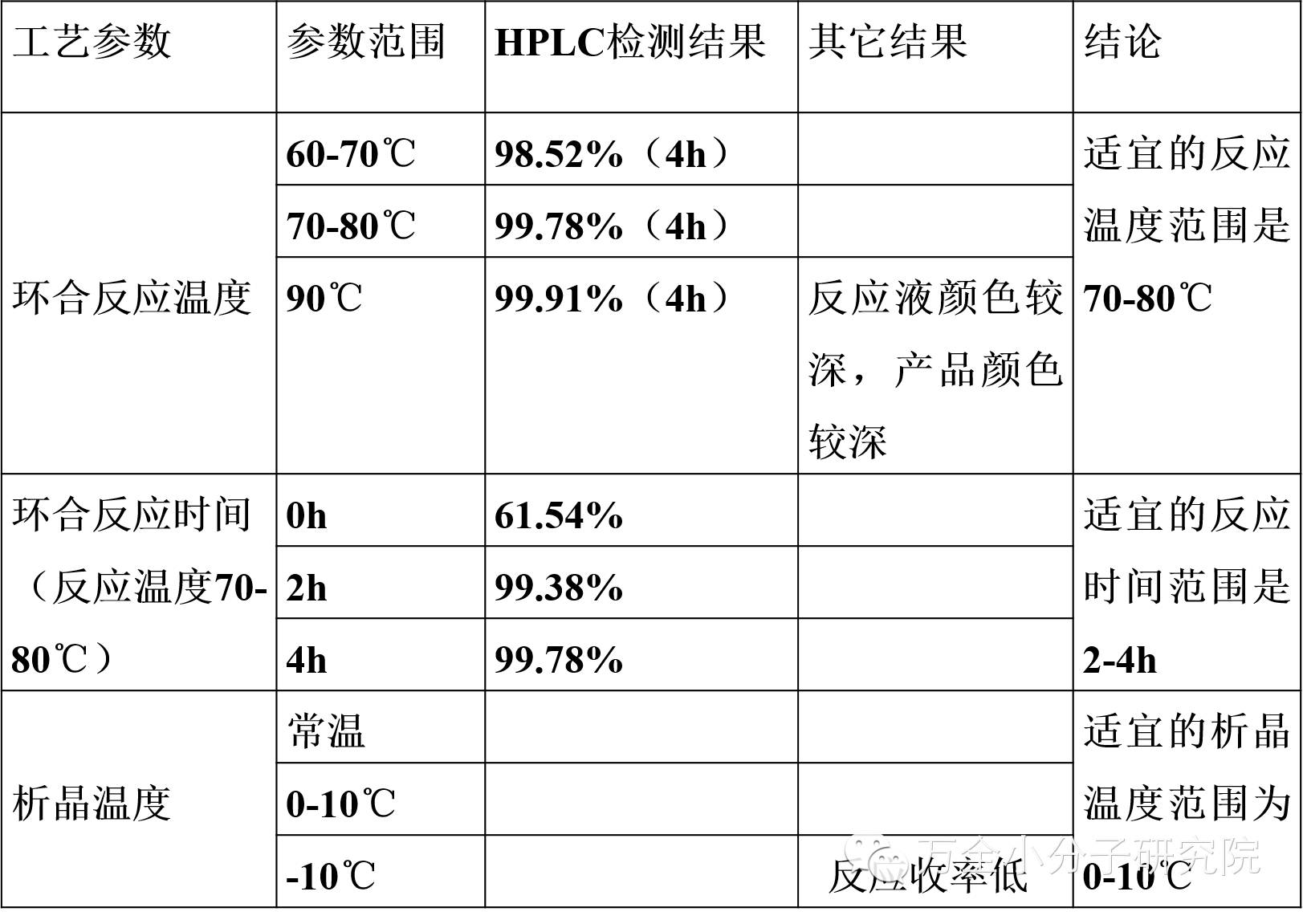
环合反应优化后的工艺参数汇总

2)缩合和粗品制备反应工艺参数摸索过程和结果汇总
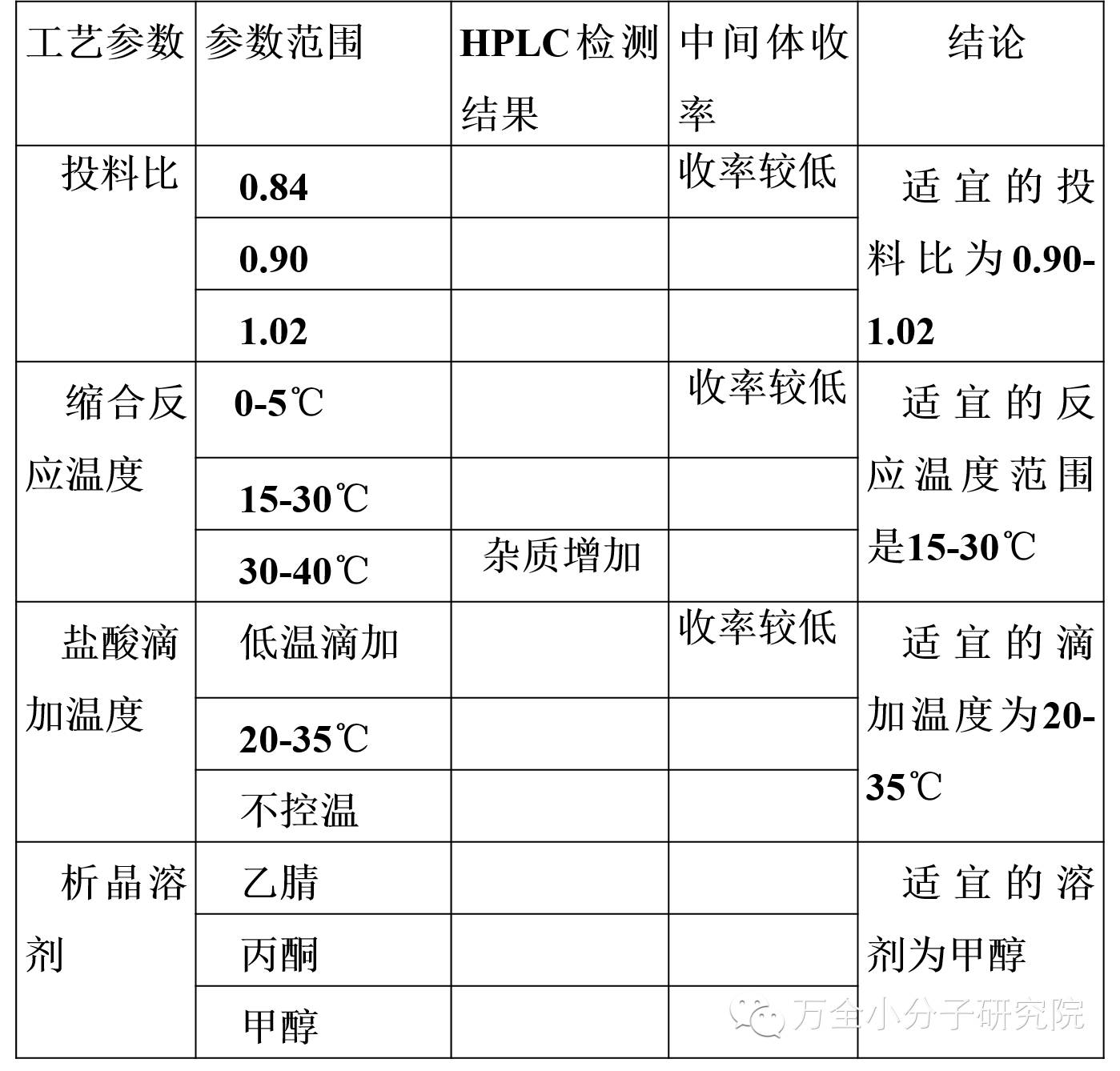
缩合和粗品制备反应优化后的工艺参数汇总
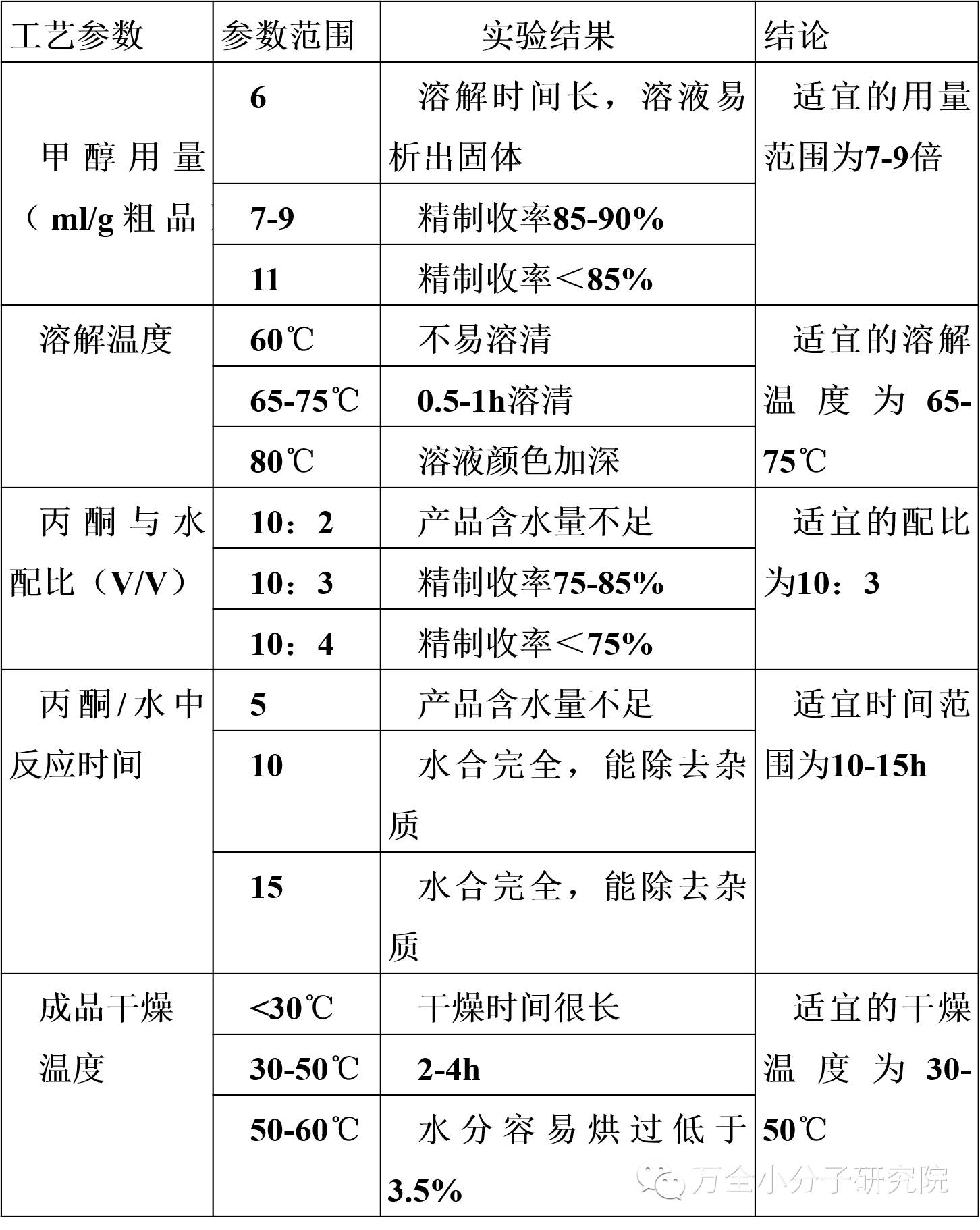
3)精制反应工艺参数摸索过程和结果汇总
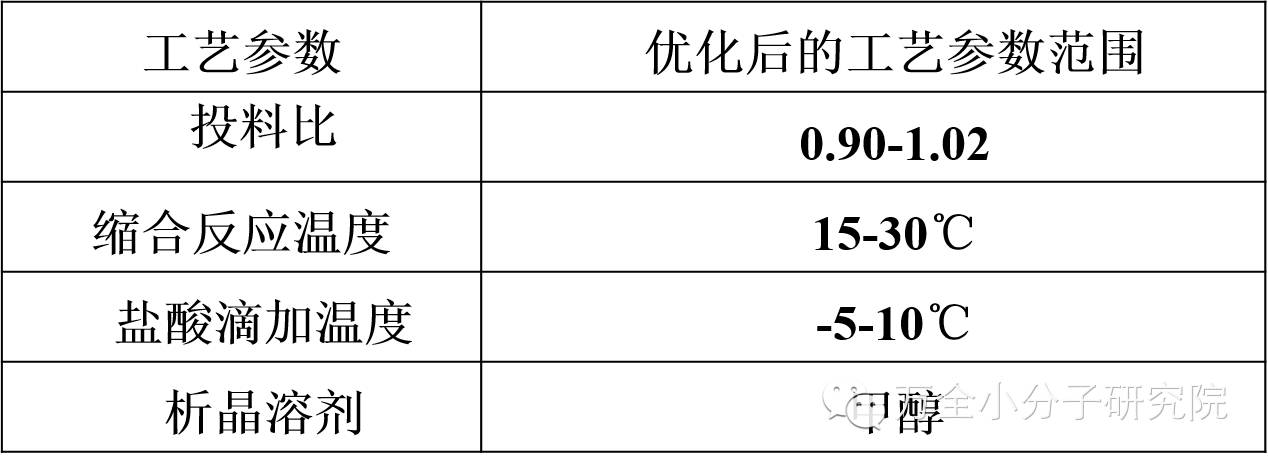
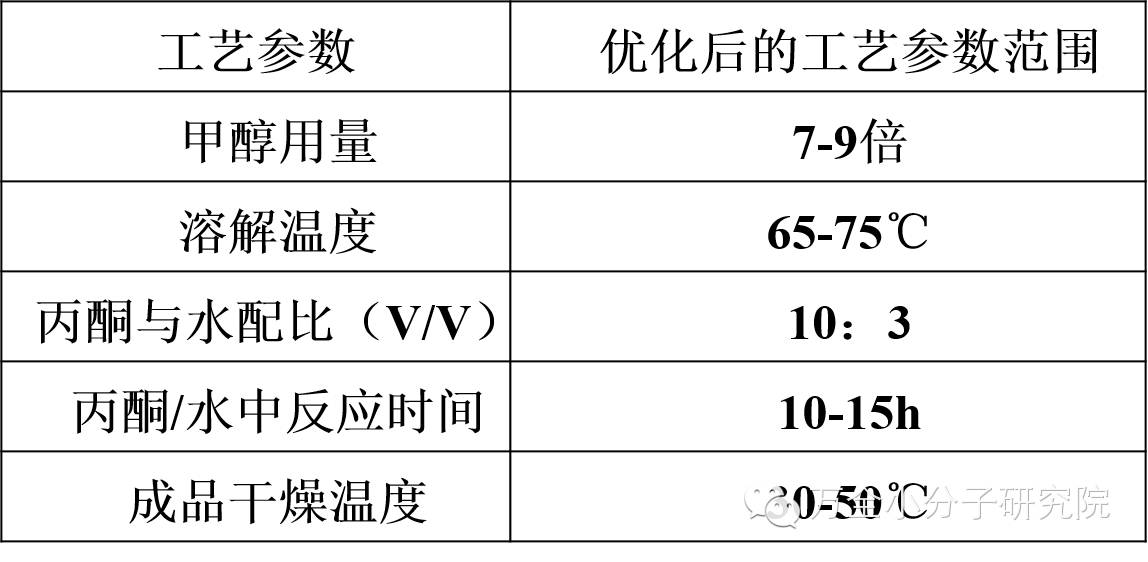
精制反应优化后的工艺参数汇总
3 .关键工艺参数的确定
通过对各步工艺研究和主要工艺参数的风险评估(详见3.2.S.2.4),将粗品定为关键步骤,该步骤的关键工艺参数为:滴加盐酸的温度(-5~10℃)。
经工艺过程控制研究及成品检验结果发现,粗品制备滴加盐酸的过程中,反应体系会急剧升温,当升至一定温度时,终产物会发生异构反应,生成杂质M。温度偏高时,杂质M会明显增高,可能导致成品质量不合格;而控制温度范围偏低时,滴加时间较长,会降低生产效率;因此可得出滴加温度对此步工艺的影响显著的结论,故将步骤中滴加盐酸的温度定为关键工艺参数。
评估判定后,通过小试工艺确认和中试生产工艺验证,可认为本品的工艺能够达到日常控制和稳定生产的要求,支持关键工艺步骤及参数确定的合理性。
4 .工艺放大研究
生产工艺的主要变化及相关批次研究数据参见下表:
1). 批量变化情况

2).设备及工艺参数变化情况
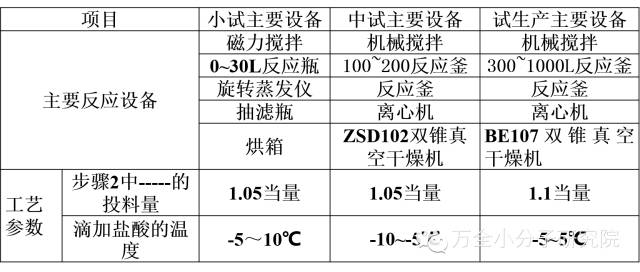
3).代表性批次工艺参数研究数据
 注意:主要生产设备信息,应提供型号、生产厂、重要技术参数的信息
注意:主要生产设备信息,应提供型号、生产厂、重要技术参数的信息
实例 1
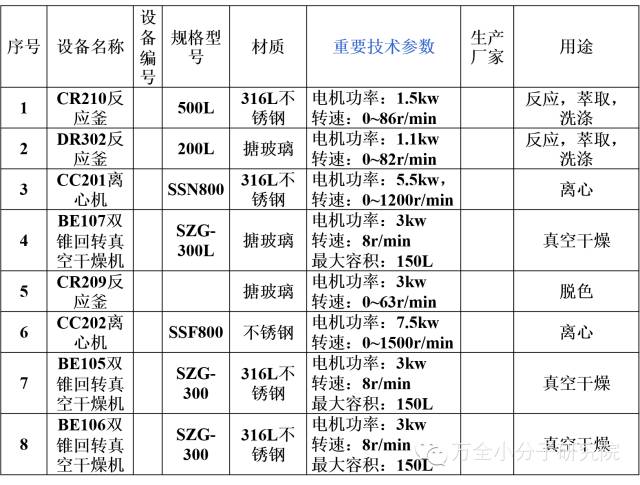 实例 2
实例 2
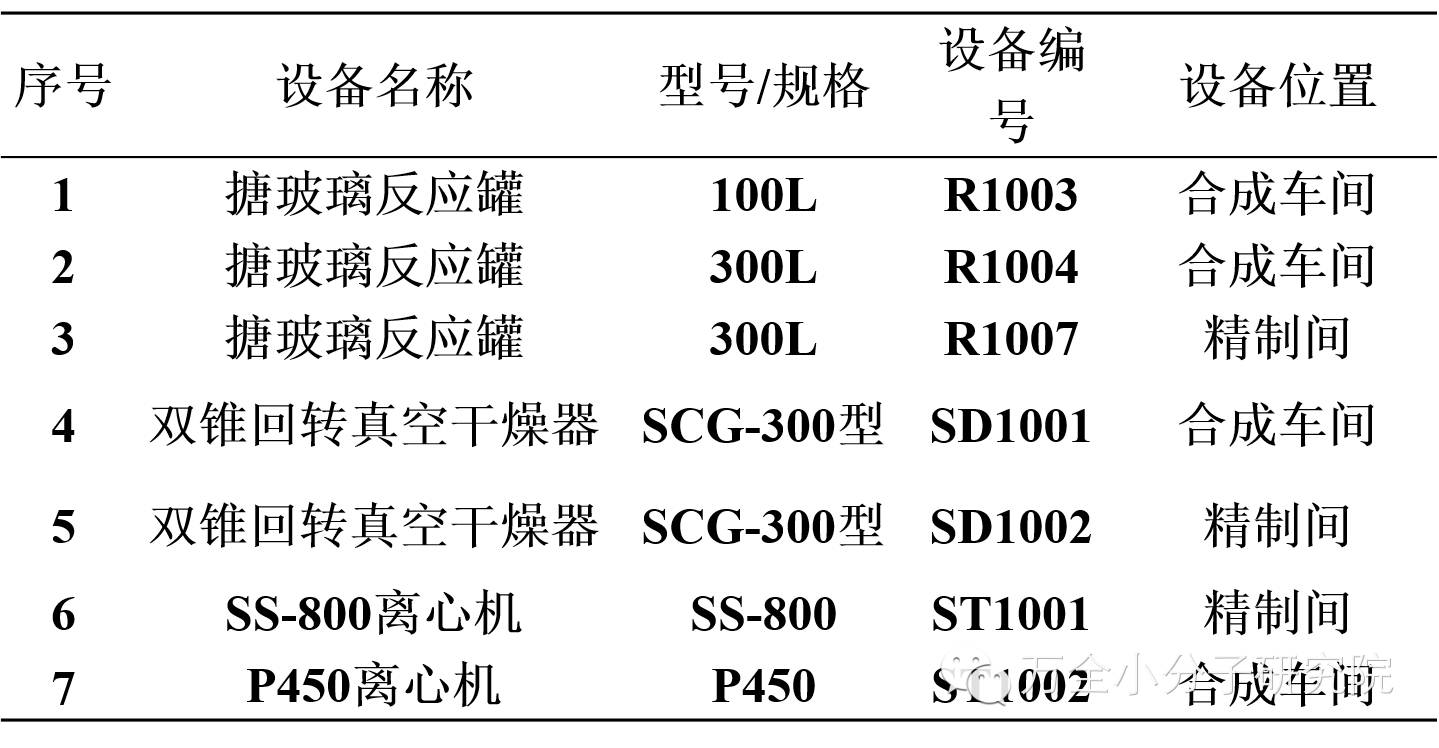
以上表中信息不全,特别是缺:重要的技术参数。
该资料的目的是证明工艺的大生产可行性
技术要求:
* 无菌原料药应提供工艺验证资料(针对无菌操作步骤,如除菌过滤等的验证),包括工艺验证方案和验证报告。
*其他原料药可仅提供工艺验证方案和批生产记录样稿,以及上市后对前3批商业生产批进行验证的承诺书
存在问题:
只简单的提供工艺验证方案编号和工艺验证报告编号,没有实质内容。
建议:还应简要介绍工艺验证报告/方案的主要内容,包括工艺验证的时间、具体的生产线及地点、批次、规模、明确关键步骤、对哪些关键工艺参数进行了验证及验证结果等必要的信息。
1)工艺验证相关信息

2)工艺验证项目及验证结果

3)工艺验证所提交的相关文件
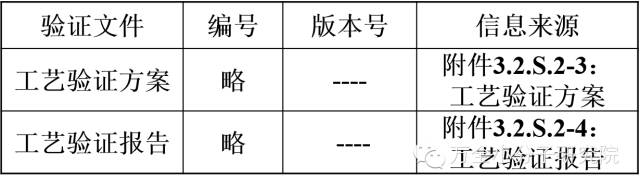
结论:证明使用所选取的工艺参数、工艺条件、设备和物料等进行生产,能持续有效地生产出符合预定标准的中间体以及成品。并确定工
艺规程及相关标准操作规程的适用性。
本公司郑重承诺该产品上市前进行三批生产规模产品的工艺验证,产品质量控制严格按验证方案进行。
编辑:梅希
本文来源:万全小分子研究院,药事纵横转载此文仅用于学习与交流,我们对文章的内容保持中立的观点,如有版权问题请联系我们删除。我们给出原文链接,以方便广大朋友溯源。

药事纵横是一个开放,由自愿者组成的团体,现有成员14名,分别为Voyager88,雷诺岛,三分话,Herman,梅希,文竹,duke,巉石,ISAL,yhqqqqq,鲁礼炎,占小兵,越下里两毛,溜溜,欢迎有志之士加入我们团队。投稿、合作请加微信442015666。

















