
余永国 博士
从“试错模式”到“一击即中”,NGS助力遗传病研究及诊疗发展
嘉宾简介:
余永国,儿科学博士,副主任医师,副研究员,硕士生导师,上海交通大学医学院附属新华医院儿科内分泌/遗传科副主任医师,同时兼任上海市儿科医学研究所分子诊断平台负责人、课题组PI,浦江学者,美国哈佛大学博士后。近年来,余永国承担多项国家级及市级课题;发表SCI论文30余篇(总影响因子>100分),回国后,成功搭建了基因芯片和二代测序诊断与研究平台。
随着医疗技术水平的提高,人类的疾病谱已发生了巨大的变化。近些年,国内新生儿死亡率持续下降,而出生缺陷问题却日益凸显。神经发育障碍、遗传性代谢病、重要脏器结构畸形等严重影响婴幼儿的生存和生活质量,成为导致儿童死亡和病残的主要原因。这些病童如同来自遥远的外太空,就像“星星的孩子”,承受着其脆弱的身体不可承受之重,精准诊断及治疗儿童遗传病成了至关重要的一环。
在基因测序技术蓬勃发展的当下,基因测序市场日益繁荣,基因技术改变了传统的医疗观念,也为遗传病的检测提供了更加简便而有效的手段,NGS等新兴技术也发挥着愈发强大的作用。日前,测序中国专访了上海交通大学医学院附属新华医院、上海市儿科医学研究所余永国博士。面对儿童遗传性疾病日益严峻的形势,余永国博士畅谈了当前遗传病的诊疗现状,就NGS数据的解读、数据共享以及遗传咨询等热点问题发表了独到的的见解,并就测序技术在遗传病中的应用进行了详细的临床案例分析。
测序中国:能否向大家介绍一下您的团队,以及新华医院儿科研究所主要针对哪些人群进行遗传研究或检测?
余永国博士:我们团队是上海交通大学医学院附属新华医院,上海市儿科医学研究所儿童内分泌/遗传科,我们科室分成四个平台——医生平台、生化平台、分子平台和细胞平台。
医生平台目前有11位内分泌/遗传科的医生,一方面主要负责儿童内分泌遗传代谢性疾患、遗传咨询、儿童遗传及产前咨询等诊断和治疗,另一方面负责实验室报告的审核和签署;生化平台主要进行特殊生化检测,包括新生儿筛查,血、尿串联质谱,代谢性疾病的酶学测定(戈谢病、粘多糖、脑白质病及溶酶体病等)以及检验科不开展的特殊激素和生化检测等;分子平台主要负责患者的分子诊断和产前诊断,包括一代测序(Sanger)及其衍生技术、新一代测序(NGS)技术和基因芯片技术等;细胞平台主要负责孕妇无创产筛、羊水培养、染色体核型、FISH检测等。
目前,我们的团队主要针对儿童内分泌遗传病因比如矮小、性早熟、性腺发育不良,代谢性疾患如氨基酸代谢、有机酸代谢、糖代谢及脂肪代谢障碍性疾患,儿童出生缺陷的遗传病因及产前遗传咨询等领域进行研究、诊断和治疗。
测序中国:在您的实验室,哪些疾病可以通过NGS技术受益?
余永国博士:传统的遗传性疾患诊断策略是“试错模式”,医生必需预先诊断,再通过基因检测验证,由于不同的医生对不同的疾病认知不同,同样的患者在不同的医生那里得到的诊断和检测差次不齐。随着现代生物医学新技术,尤其是NGS技术在临床研究中的应用,传统的诊断策略将被颠覆,诊断模式可以一步到位,变得更加精准,无需医生预先诊断,筛查结果会提示疾病表型,适用范围扩大到人类数千种遗传病,甚至可发现新的疾病,诊断过程也转为由里到外,先筛查基因,得到答案,再用其他实验室检查验证。
比如对于内分泌常见的疾患,如两性畸形和尿道下裂,传统来说我们的思路是综合患者的外观性别、激素性别、器官性别、基因性别、基因突变分析及心理性别来进行综合判断。但实际上导致性腺发育不良的基因众多,目前已知的就有200~300个,传统的诊断思路不可能一下子就通过临床和生化检测判断是哪个基因导致的。所以在很长一段时间中,传统的诊断思路就是“试错”,通过一代测序先检测一个基因,如果结果是阴性再检测另外一个基因,然后以此类推,反复检测。
这种传统的“试错”模式不但延缓了诊断时间,而且需要反复取样,既增加病人的痛苦又提升了检测成本,同时也需要技术人员进行重复劳动。随着NGS技术的发展,这个弊端会消除,通过基因Panel测序或者全外显子测序,只需要一次取样并进行一次实验,就可以将目前已知的导致性腺发育不良的200~300个基因,甚至全基因组层面与遗传病相关的几千个基因,乃至新的致病基因都挖掘出来。这不但可以在成本可控的前提下提高通量,而且一次取样就可以得到大量信息,极大减轻了患者痛苦,加快了由样本到报告的流程,为进一步治疗争取到了宝贵的时间。所以NGS可以说是现阶段可以使用,未来也更值得期待的技术。

余永国 博士
测序中国:对于NGS从前期样本制备到测序及数据分析,您怎样评价目前市面上的相关产品,在这些环节中您最关注的是什么?
余永国博士:NGS涉及的流程众多,主要包括三个大的环节:建库和捕获、测序、数据分析。
在建库和捕获环节中,相关产品众多,如在儿童遗传病领域,有全外显子相关产品,也有基因Panel等,目前主流的有Illumina的TruSight-One和全外显子组建库产品、Agilent的全外显子组和常见遗传病产品、Roche的NimbleGen全外显子组、IDT的全外显子组等相关产品等。这些产品在临床诊断功效上大同小异,其设计主要基于目前我们对已知疾病、数据库及文献的认知,比如Illumina的TruSight-One,其所涉及的4800多个基因涵盖遗传病、代谢病、肿瘤、心脏病、血液病、癫痫、感官及其他神经退行性疾病。其基因组目标片段是根据多方面的信息确定的,包括人类基因突变数据库(HGMD)、在线人类孟德尔遗传数据库(OMIM)、GeneTests.org网站、Illumina TruSight系列测序组合及市场上其他的测序组合试剂盒。综合这些来源的数据,一次检测基本可以覆盖目前临床研究背景下关注的重要基因。
儿童遗传病新一代测序环节现在市面上主要使用的是Illumina和Thermo Fisher公司的测序仪器和相关试剂,性能占优且占市场绝对领导地位的是Illumina公司。以TruSight-One搭配不同通量的Illumina测序平台为例,MiniSeq及MiSeq一次运行可以做3个样本,刚好是一个家系,可以满足最基本的遗传病研究。如果样本量比较大,可以选择NextSeq或NovaSeq这种中高通量测序平台。
数据分析领域目前市面上参差不齐,比较混乱,有些厂家的解决方案自带数据分析,还有众多专门进行数据分析的公司。
我最关注的正是数据分析领域,因为这个领域是最终解决问题的环节。
从全外显子角度,每一个人大约都携带几百个和正常人不同的罕见变异。对于临床医生,不能以一个患者的任何一个变异,貌似和临床有些符合就断定某一疾病,给孩子和家庭扣上遗传病的帽子,这会造成很多的“冤假错案”,也给患者带来不必要的痛苦。任何一个变异,都需要从临床表型、生化检测、遗传规律、致病性等多个方面综合考虑。
此外,我还很关注数据库的共享。当前,不同实验室的数据以及不同医院的数据,都是一个孤岛,没有很好的共享机制。这导致同一患者在不同的地方重复进行相同的检测,也导致同类的疾患做同样重复的验证工作,造成极大的人力和财力的浪费。
测序中国:您在生物信息分析方面有自己专业的队伍,他们做了非常出色的工作,也开发了一些软件,可否简要介绍一下您的团队在数据分析方面的独特优势或者经验?
余永国博士:在NGS领域,我们主要依靠自己的生物信息团队所建立的Pipeline,目前主要由两个海外博士负责,一个是荷兰莱顿大学医学中心人类和临床遗传学中心的博士和博士后,有Nature Genetics和美国人类遗传等顶级刊物的一作论文,另外一个是美国Emory大学的神经学博士,也有Nature Neuroscience一作的论文,他们两个在NGS和基因芯片领域有着极其丰富的经验和体会。
同时,我们的团队拥有丰厚的临床资源,可以说形成了“医生→技术员→平台工作人员→患者”的一体化团体。
我们现在的NGS流程是,技术员先进行建库和捕获后测序,数据产生后运行Pipeline,然后由平台人员进行两个独立的复审讨论汇总。对于我们的NGS分析,其最大的特色是遗传学临床医生的判断,汇总后的变异需要经过临床医生尤其是开单医生的复审和确认,然后再进行一代测序验证,这样的变异是经过临床论证和检验的,所以结果可靠。
测序中国:您利用外显子测序开展了非常出色的研究,您能否就NGS在其他应用方向比如转录组测序、甲基化测序以及全基因组测序在临床研究中的潜力谈谈您的看法?
余永国博士:因为我主要专注于儿童出生缺陷的临床应用研究,所以更多地关注DNA水平、基因Panel等。目前,外显子和全基因组的应用较多,但是转录组、甲基化等领域的NGS应用及发展也非常迅猛,但是目前还是主要应用于基础研究,离临床诊断和应用还尚有距离。
测序中国:您曾于美国哈佛大学医学院进修分子诊断多年,这段经历带给您最大的收获是什么,有什么一直影响至今?根据您丰富的临床经验,是否可以分享一下怎么将新技术与中国独特的大量样本资源及大量数据充分结合,产生最大的价值?
余永国博士:相较于国内,国外的遗传体系和制度非常成熟。有相应的专业和职称体系,有成熟的医生、实验室及产品以及仪器考核和认证系统,在这些方面国内还很欠缺。
但是目前国内有大量的病人资源,现在国内的遗传咨询培训、技术培训、第三方检测公司、国外遗传机构、遗传医师体系和职称等蓬勃发展,大家都是想把国内的遗传事业做大、做强。相信在不久的将来,中国内地遗传病的研究将是世界遗传事业的主战场之一。
测序中国:您怎样看待中国目前精准医疗的发展?在您看来,NGS技术在未来将对临床诊疗产生怎样更多的影响?针对目前国内遗传咨询医师的相对匮乏的现状,您有怎样的个人理解?
余永国博士:现在精准医学的概念十分火热,可谓“如火如荼”,甚至被炒作得较为严重。当前,有院士层面的大精准:综合环境、生化、DNA水平、RNA水平、蛋白质水平、甲基化水平、药物反应等因素,这个精准听起来非常“高大上”,但是实施起来却非常困难;也有实际应用的精准:精准的分子诊断,药物靶点等;当然还有个别具有“忽悠”成分的商业精准,如个别意义不明的肿瘤体检、健康体检等。不管是什么样的精准及分子技术,但不可否认的是NGS高通量技术已经走入了我们的生活,相信在不久的将来,基因诊断会像我们现在的胸片、血常规一样,成为各个专业领域和方向的常规检测,成为有效诊断疾患的强大武器。
目前中国遗传咨询市场发展迅猛,这是非常好的事情,有助于培养专业团队和人才,做大市场,但也需要不同的人群分工协作。
首先,对于遗传咨询医师,这需要卫计委、中国医师协会、国家考试中心联合,先解决专业代码和职称体系。目前已经有了医学遗传学专业,并列于内科、外科和儿科,但是没有遗传医师这个职称体系。那么问题就来了,医学遗传学专业的学生进入临床岗位,不能晋升,只能通过其他体系比如儿科体系、内科体系、检验体系晋升职称,这无疑限制了医学遗传学的发展。有了专业和晋升体系,后面就是建立题库和培训师资及专科人才的培养,这样遗传咨询医师才能和国外一样形成规模并系统化。
其次是遗传咨询师,主要服务于遗传咨询医师、第三方检验公司及患者的遗传咨询,目前国内对这一领域的关注度很高,其发展还是很好的。
此外,未来还需要国家药监局和相关的质控中心的积极合作,以解决试剂和仪器的认证问题。国内和国外的体制不一样,如美国是采用实验室资质认证,只要实验室有资质就可以开展各类检测,而国内需要经过主管部门的审批,而这个审批要考虑人员的资质、场地的资质、试剂的资质和仪器的资质,即使四证齐全,除此之外,还需要有收费代码。这样繁琐的流程导致目前很少有NGS产品能合法合规地在国内大规模应用,这也在无形中限制了其发展。
最后,在医疗保险方面,目前分子诊断的检测费用较为昂贵,如在美国等发达国家,这些昂贵的检测大多由保险覆盖,但中国目前都是由患者买单,这也相对制约了新技术的发展。
测序中国:感谢您接受我们的专访!
余永国博士:谢谢!
在专访后,余永国博士还就测序技术在遗传病中的应用进行了详细的临床案例分析,以下为案例分析的详细内容。
实际案例分享一:对单基因病临床表现不明显的补充确诊
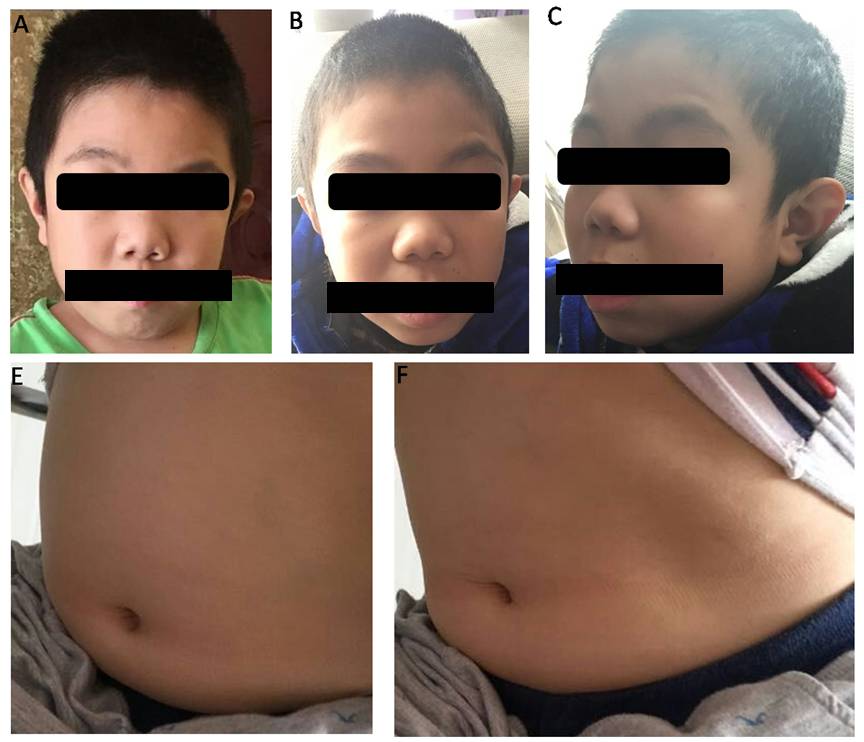
男孩,9岁,身高5cm(矮小),体重27.8kg;出生史无特殊;1岁会走路,2岁会说话,3岁上幼儿园;5岁时家长感觉明显退步;就诊时表达意思不清楚,好动,不与人沟通,不会写字;辅助检查:8岁IQ小于40;染色体正常;血尿串联正常;甲状腺功能正常,生长激素完全缺乏;MECP2 Rett综合征基因检测未见异常;基因芯片检测未见异常;脆性X综合征未见异常;在某医院给予干细胞脑注射治疗,效果欠佳,9岁时智力接近于0;辅助检查:脑电图正常;脑MRI:右额叶多发软化灶,双侧脑室宽,脑沟增宽。
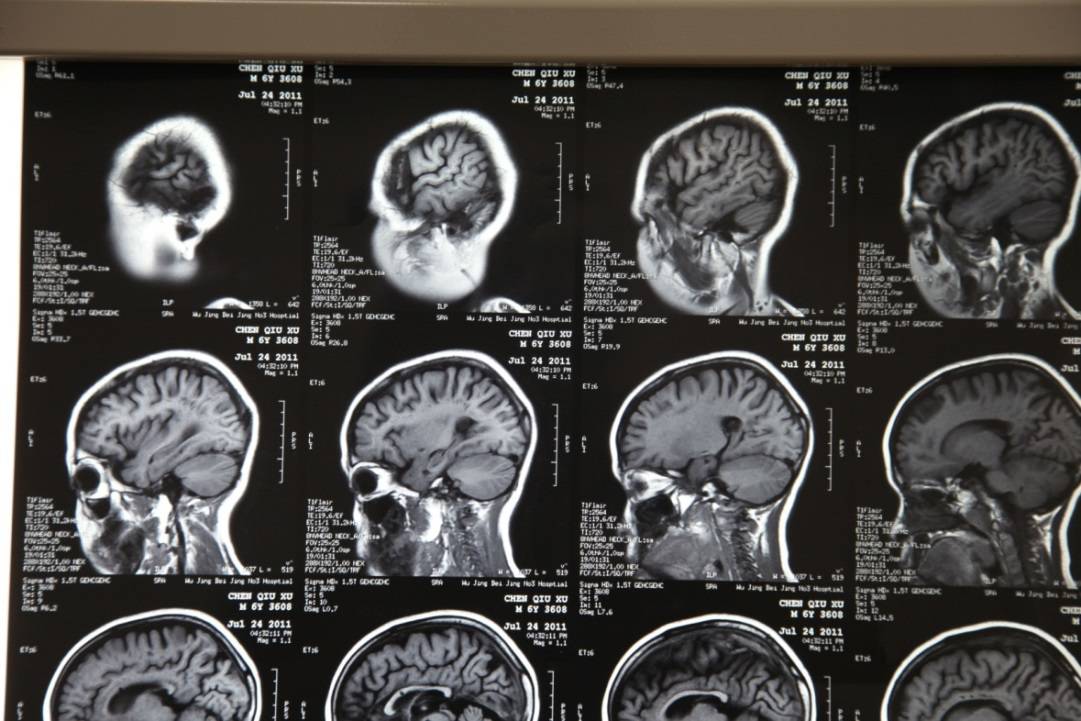
像这样的疾患,临床表现不典型,从疾病的认知角度不知道是什么基因的变异,通过Illumina测序平台检测后发现是不典型的III型粘多糖:

并经过一代测序和酶学确诊。
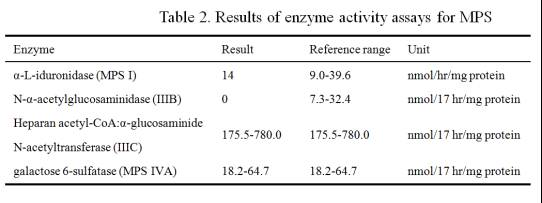

实际案例分享二:对复杂疾患的精准诊断:
对于不明原因及一时没有诊断思路的患者,NGS是一个很好很强大的武器。
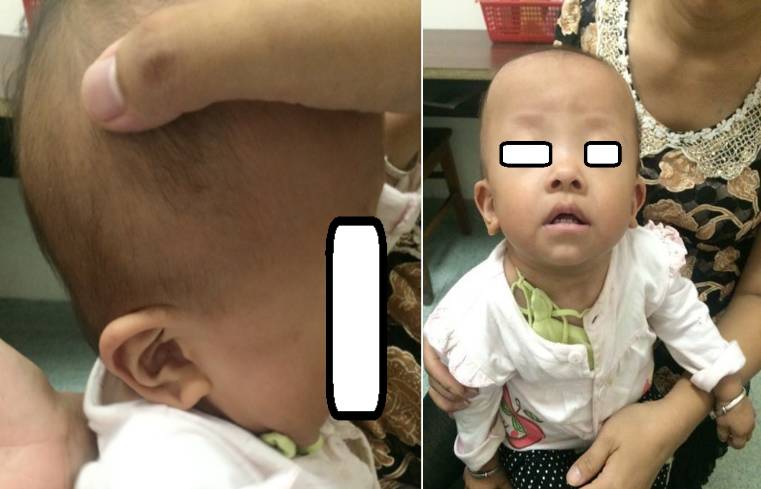
患儿,女,1岁3月就诊;发育迟缓,眼睑下垂,有先心史;出生时有青紫吸氧史,BW 3.5;身高<-3SD,体重<-2SD;头围正常,特殊面容(双眼上睑下垂,遮盖上1/4瞳孔),心前区Ⅲ°收缩期杂音;心彩超:房间隔缺损(Ⅱ,筛孔样);二尖瓣病变伴轻-中度反流;三尖瓣病变伴中度反流;左右心室壁稍肥厚;肺动脉高压;GESELL提示发育稍落后(动作能DQ粗74细99;应物能DQ89;言语能DQ80;应人能DQ89);染色体正常;尿粘多糖定性电泳:弱阳性,DS区带;酶活性检测阴性;全基因组芯片检测阴性。
初步诊断:矮小;发育稍落后;双眼上睑下垂;先心(房缺、瓣膜病变、室壁肥厚,肺动脉高压),有家系血。
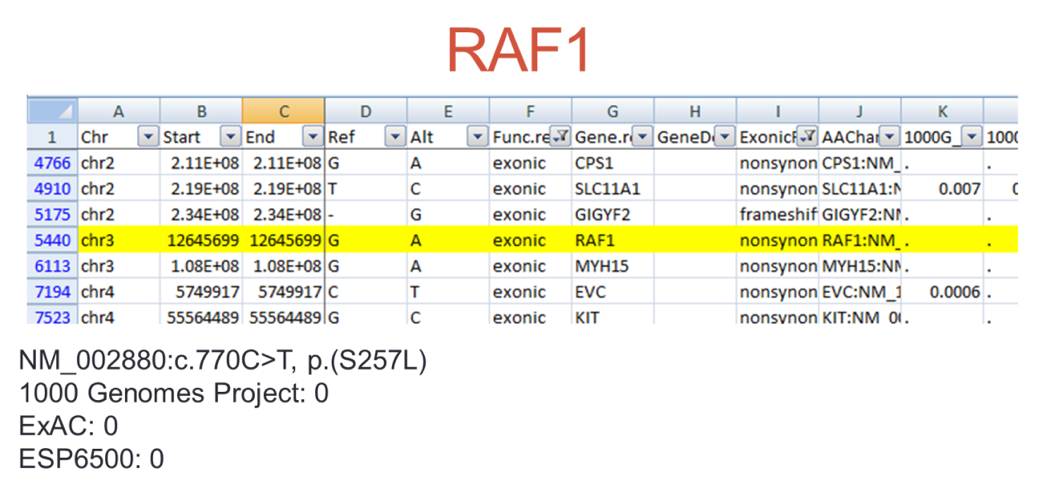
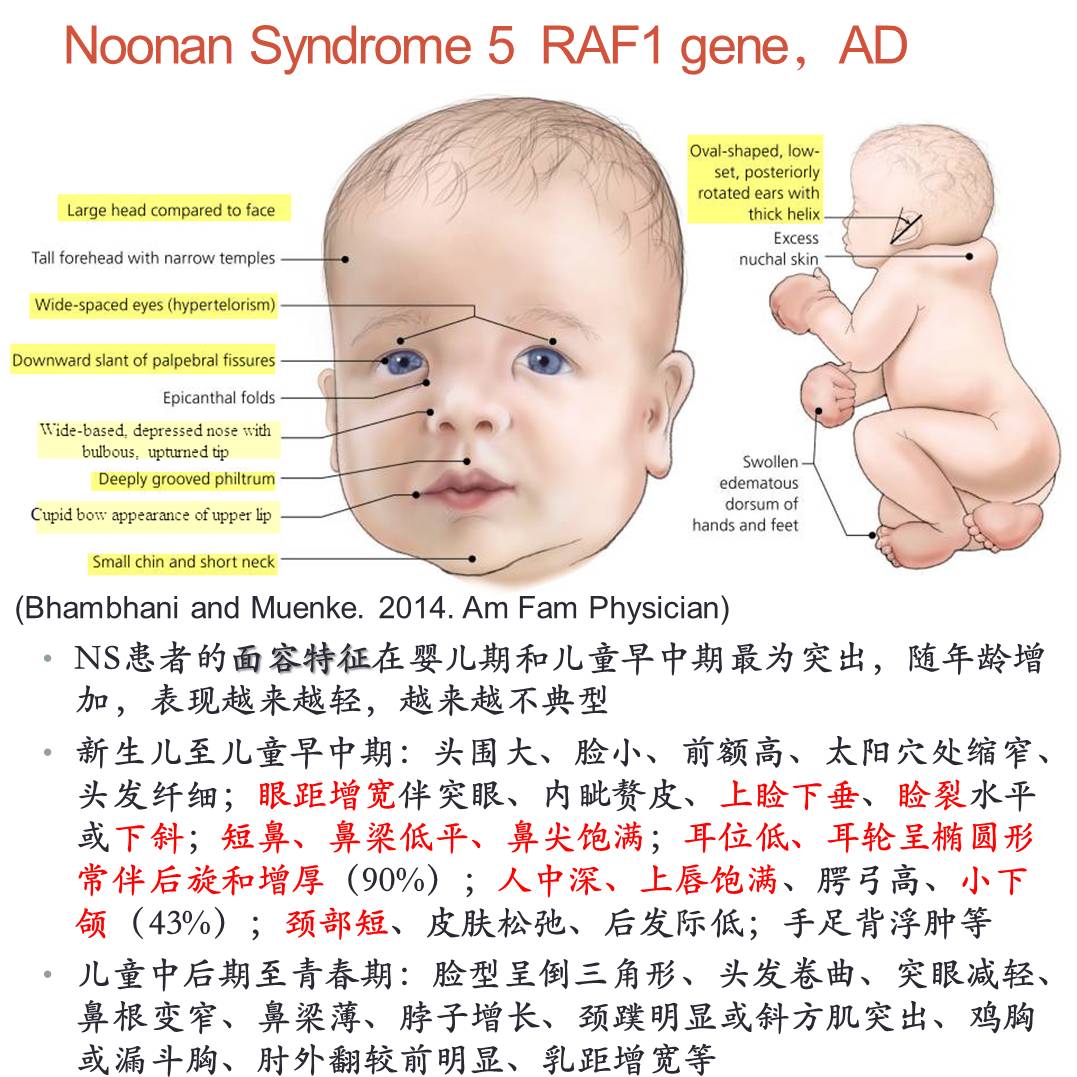
通过前两个案例我们不难发现,都是在没有典型临床表现,以及经过传统方法检测后仍然没有诊断思路的情况下,最终通过NGS获得了精准的信息,打开局面,再用其他方法验证,最终明确诊断思路及下一步方案。
实际案例分享三:不能过分的依赖高通量测序
但是我们也不能过度的依赖高通量测序,而丢失了我们基本的医生诊断思路。
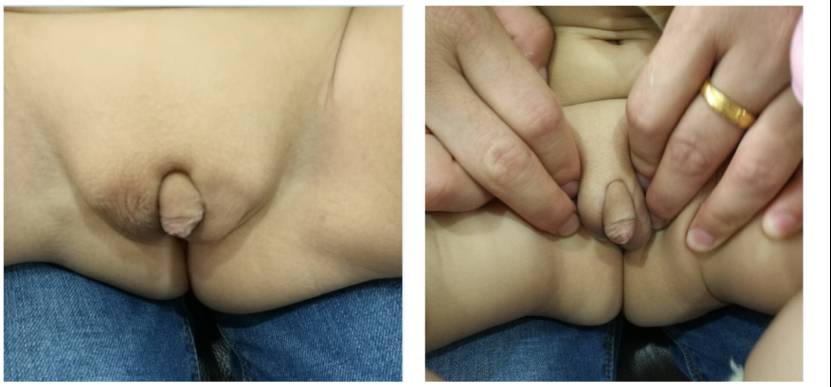
患儿,男,14个月;身高2cm(正常),体重10.7kg(正常);智力正常;骨骼无畸形;体型匀称;面部外观正常;染色体46,XY;尿道下裂,生殖器外观异常,尿道开口于阴囊水平;新生儿筛查17羟孕酮(17OHP)高278(正常值低于30);电解质正常,ACTH 231(高),皮质醇8.95(低);皮肤黑,出生后一直按照肾上腺皮质增生症(CAH)给予口服9a氟氢可的松和醋酸氢化可的松治疗至今,控制可,皮肤颜色正常,生化在正常值范围;肾上腺B超未见肾上腺皮质增生;睾丸B超质地欠佳,13X7X9,未见卵巢;有一姐姐,新生儿筛查17羟孕酮高;19个月因一次发热后抽搐,脑炎肺炎死亡。
问题是这个患者:肾上腺皮质增生症诊断是否成立?尿道下裂如何处理?治疗有什么措施?后续如何进一步诊治?
这个患者在外面先后做了几次基因检测,第一次是392个相关代谢病Panel,呈阴性:392个代谢病相关Panel未见致病性变异;CYP21A2未见变异,CPY11B2只发现一个变异位点,AR疾患;其他变异位点临床不支持。

然后扩大做了764个代谢病基因全面筛查Panel,未见致病性变异:CYP21A2只发现一个变异位点。

然后继续更换方向,做了219个性发育基因的Panel,未见致病性变异:CYP21A2未见变异,HSB3B2只发现一个变异位点,AR疾患;其他变异位点临床不支持。
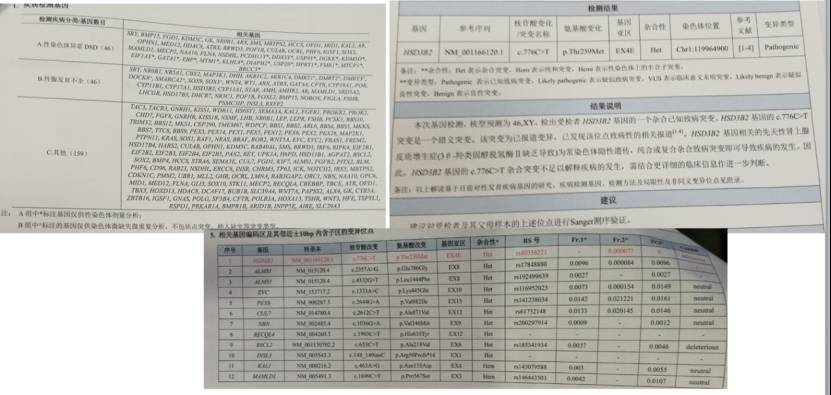
最后做了全外显子,也是阴性。
事实上根据临床表现和生化特点,导致17羟孕酮高而且还有尿道下裂的只有HSD3B2基因突变导致的3B-羟类固醇脱氢酶导致的CAH,以及POR基因突变导致的细胞色素P450氧化还原酶。而患者没有骨病表现,所有患者只能是HSD3B2基因突变导致的3B-羟类固醇脱氢酶导致的CAH,那么问题就简单了,现在发现了HSD3B2基因一个位点突变,而这个疾患是常隐的疾患,存在缺失的可能,我们最后做了一个QPCR就证明了这件事情。

· END ·















