
▲扫描二维码下载
HP007是一种基于寡聚脱氧核苷酸(CpG-ODN)的免疫激动剂,通过特异性地刺激Toll样受体9(TLR-9),诱导体内的细胞免疫和体液免疫,增强机体免疫应答,在疫苗佐剂和肿瘤治疗等领域具有良好的应用前景。
4月5日至10日在美国圣地亚哥举行的美国癌症研究协会(AACR)2024年年度会议报告中,SYNC-T作为一种研究性疗法,在肿瘤部位进行冷冻设备诱导肿瘤死亡,模拟原位肿瘤疫苗接种,并与瘤内输注肿瘤免疫药物与由
华普生物技术(河北)有限公司(下简称华普生物)
独特的HP007相结合,在转移性去势耐受性前列腺癌患者中表现出卓越的临床反应, 总应答率达84.6%!在晚期实体瘤治疗领域,实属罕见。
美国Lankenau医学研究所的副教授、Syncromune的联合创始人兼执行主席Charles Link医学博士表示,对激素治疗没有反应的转移性前列腺癌(mCRPC)患者几乎没有治疗选择,死亡率很高。前列腺癌具有免疫“冷”肿瘤微环境,这对现有的免疫疗法提出了挑战,这些疗法在前列腺癌患者中表现出低应答率和高毒性。
Link及其同事开发了一种新的治疗方法,以刺激mCRPC的系统抗肿瘤免疫反应。他们的疗法被称为SYNC-T,首先使用直接插入原发性或转移性肿瘤的探针来冷冻肿瘤的一部分,这会导致肿瘤细胞破裂(溶瘤)并释放刺激免疫的新抗原。从本质上讲,这种方法产生了一种个性化的原位癌症新抗原疫苗,用于激活免疫系统。将探针插入前列腺的成像和程序技术与泌尿科医生进行前列腺活检的常规方法相似。
在溶瘤步骤之后,同时将一种名为SV-102的研究性多靶点药物输注到肿瘤的溶解区域。SV-102是一种固定剂量的药物组合,由多种活性药物成分组成:包括
HP007(由华普生物设计并生产,具有一系列全球知识产权的疫苗佐剂和肿瘤免疫治疗佐剂)
、PD-1抗体、CTLA-4抗体和CD40激动性抗体。SV-102同时阻断了两种不同的免疫抑制机制,并激活了两种截然不同但又互补的免疫增强机制,使疫苗诱导的T细胞能够激活并产生系统性抗肿瘤免疫反应。
在一项I期临床试验中评估了SYNC-T的安全性和有效性,该试验招募了15名患者(12名mCRPC患者和3名选择退出激素治疗的转移性前列腺癌患者),其中13名患者已评估了疗效。60%的患者为白人,33%为西班牙裔,7%为黑人,中位年龄为61岁。在13名可评估的患者中,
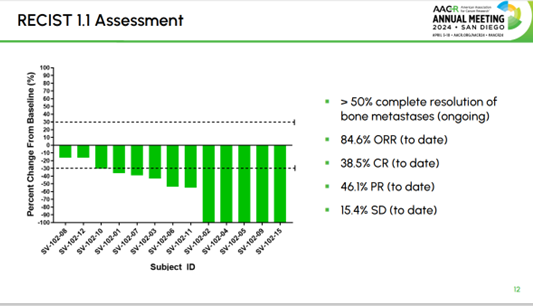
11人出现了客观响应,其中5人为完全响应(CR),6人部分响应(PR),总响应率(ORR)达84.6%
。在数据分析时,另外两名可评估的患者病情稳定。6名患者出现轻度至中度治疗相关不良事件,包括发烧、僵硬、疲劳、发汗、血尿、尿路感染、急性尿潴留和肝酶升高。
Link指出:“SYNC-T的毒性似乎远低于之前在前列腺癌患者全身免疫疗法中观察到的毒性”。
他总结道:“我们的研究结果表明,SYNC-T在最初的这组患者中具有高反应率,而不会产生严重毒性,这为扩大免疫疗法在mCRPC中的作用开辟了机会”。此外,这种方法使用了泌尿科医生和放射科医生已经采用的标准程序,这意味着这种治疗方法可能会被治疗医生迅速采用。
此疗法中使用的HP007为华普生物技术公司自主开发的新型C型CpG,作为TLR9激动剂类的抗肿瘤新药,其可与TLR9受体结合,激活pDCs、CD8+T细胞和NK细胞,从而调动免疫系统的抗肿瘤活性以有效清除肿瘤细胞和阻止肿瘤转移。HP007通过激活人体自身的免疫反应,使免疫反应迟缓者产生肿瘤免疫反应,因此具有治疗多种癌症的潜能。SV-02的成功给华普的HP007提供了坚实的临床验证,为将来的肿瘤免疫治疗开辟了一条新途径。此外,华普生物已在2023年9月获批HP007 IND,I期临床试验正在中国开展。
信息来源:
AACR News Release:A Biologic Drug-Device Combination Immunotherapy Shows Promise for Patients with Metastatic Prostate Cancer. April 7. 2024
主题1:
CAR-T therapies, from concepts to cGMP manufacturing
时间:
2024年4月25日
19:30-19:55
1. The general requirements for the development of CAR-T therapies
2. General approaches to gene modification of T-cells
3. High level discussion of GMP manufacturing workflows
4. Regulatory considerations for clinical application of these therapies
嘉宾介绍:
Kenneth Warrington 博士
宜明生物 北美战略开发总监
Kenneth 博士在以AAV、LVV为载体的基因治疗,干细胞、CAR-T 等细胞治疗等领域有20余年的产业经验。对细胞和基因治疗药物的研发生产,质检放行,以及北美GMP法规监管要求等有着深刻的理解。曾 Meridian Life Science、SGS Life Science、药明康德和金斯瑞蓬勃生物等公司技术运营管理和业务开发负责人,Biostem Life Sciences的运营和业务发展高级副总裁,AAV基因疗法公司Lacerta Therapeutics的联合创始人兼首席技术官。
时间:
2024年4月25日
19:55-20:20
1. 全球细胞治疗市场的特点
2. 中美市场IND注册申报的异同
3. cGMP细胞产品的本地化生产交付
Jeffrey Hung 博士
宜明生物 全球首席商务官
Jeffrey Hung博士在生物创新药领域具有从药物研发到CXO服务的深厚行业经验,特别是在基因和细胞治疗领域拥有丰富的产业化服务经验。Jeffrey Hung博士在基因和细胞治疗的专业领军能力被全球再生药物联盟Alliance of Regenerative Medicine(ARM)认可,应邀成为权威的A-Gene和A-Cell再生药物联盟的行业标准教科书的作者和编辑,同时担任AAV基因药物(Drug Product)的主要作者,并参与慢病毒生产文章的撰写和编辑。Jeffrey Hung博士曾任职于治疗癌症的生物技术公司Exelixis,担任研究科学家,在治疗癌症的创新小分子药物开发方面积累了丰富的研究经验。他在生命科学服务领域的经历起于Harvard Bioscience,并陆续在Invitrogen、QIAGEN、ATCC、GenScript等跨国生物技术企业担任商务高管、集团副总裁等职务。
20:20-20:30
Q&A
江苏宜明生物科技有限公司(uBriGene,简称“宜明生物”),成立于2015年,是一家致力于细胞与基因治疗(CGT) 技术的开发和应用、提供一站式CDMO整体解决方案的研发生产型生物技术公司。
依托经验丰富的国际化专家团队和中美两地GMP生产基地,宜明生物能够为全球CGT企业提供从早期研发到商业化生产的全流程工艺开发和生产交付服务。目前,宜明生物已承接/交付IND、IIT、临床Ⅰ、Ⅱ 期产品百余批次,帮助全球CGT企业完成多项CGT药物IND获批并进入临床,北美基地完成近百批次临床级产品的制备并经审计合格。
(请注明姓名+公司
 )
)















