
药明康德/报道
最近,爱荷华大学(University of Iowa)的研究人员发现,
一种脂肪细胞用于感知自身体积变化的蛋白也可以控制一个关键的信号通路,以使得脂肪细胞吸收和储存体内多余的葡萄糖。
缺少这种名为SWELL1的蛋白质的小鼠,在高脂饮食下比正常小鼠增重的程度要明显更少,但也会发展出糖尿病。这一成果发表于《自然》子刊《Nature Medicine》上。
“虽然我们通过敲除SWELL1蛋白,
构建了一种能抵抗体重增加的小鼠
,”文章通讯作者Rajan Sah教授:“
但它并不健康,存在着胰岛素抵抗和葡萄糖不耐受等问题。
”
▲
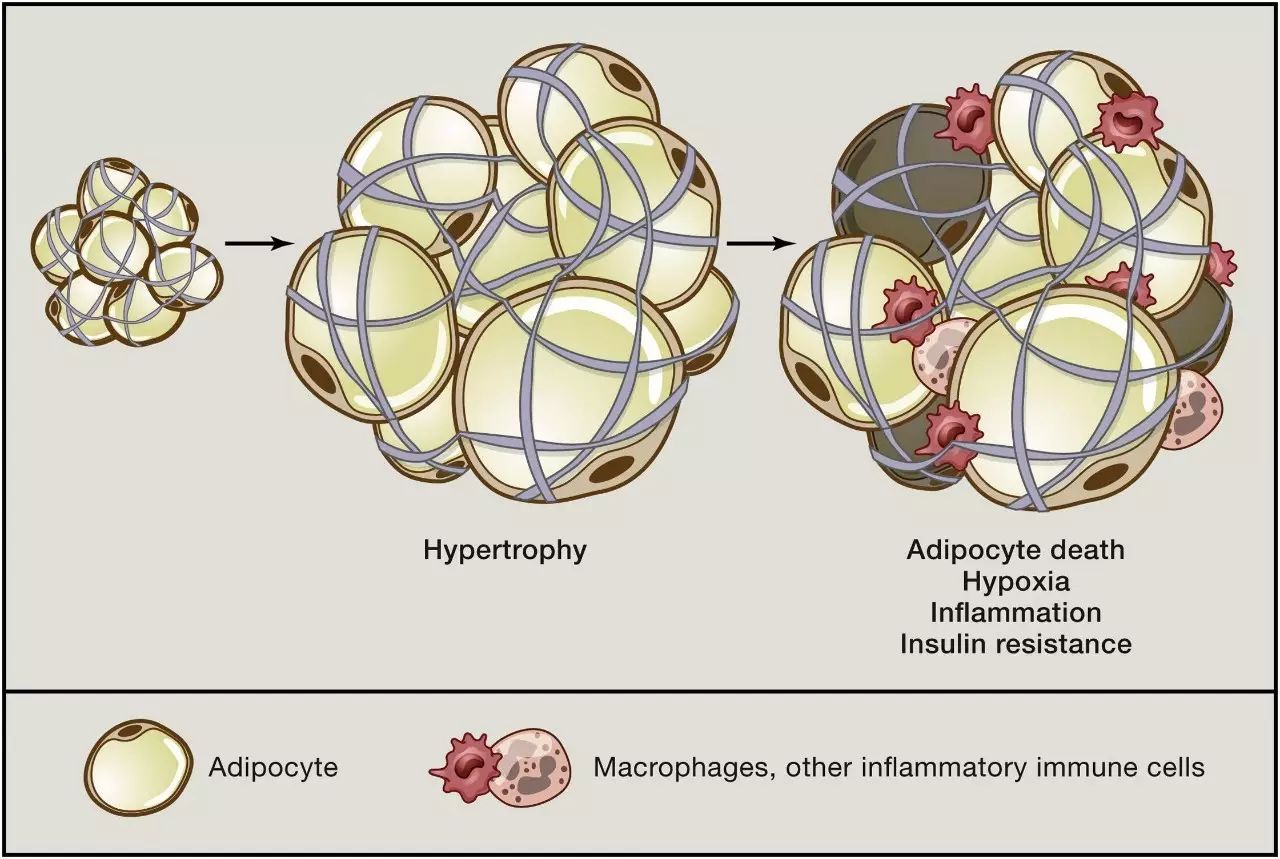
脂肪细胞的扩张和病变
(图片来源:《细胞》)
脂肪细胞具有巨大的体积扩张能力,尤其是在身体肥胖的情况下,可达到其正常体积的30倍。已有证据表明,脂肪细胞的体积变化会改变了其胞内信号传导,后者调节器在胰岛素影响下对葡萄糖的摄取。在本研究中,科学家们发现SWELL1是脂肪细胞表面体积敏感性阴离子通道VRAC的关键组分之一,当细胞扩张时会促使VRAC开放。
▲
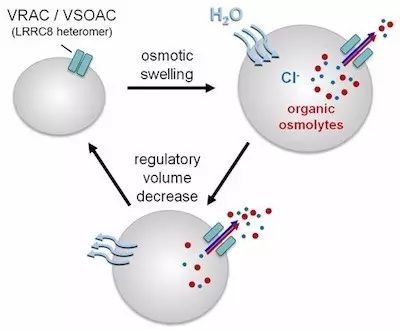
VRAC工作机制
(图片来源:mdc-berlin)
“我们认为,
可能正是SWELL1蛋白将这两个过程联系在一起:脂肪细胞的体积感应机制和通过改变胰岛素敏感性来响应体积大小变化的信号通路
,”Rajan Sah教授说。
实验显示,人或小鼠脂肪细胞的体积扩张,不管是因为人为处理还是机体的肥胖症,都会激活SWELL1信号传导通路。当SWELL1被敲除后,从小鼠脂肪细胞的这种体积感应信号也就不复存在,且脂肪细胞用来摄取和储存过量葡萄糖的insulin–PI3K–AKT2–GLUT4信号通路的正常活性也出现缺失。
缺少SWELL1的小鼠具有较小的脂肪细胞,但也会发展出胰岛素抵抗和葡萄糖不耐受。
进一步研究发现,SWELL1必须以其C端富含亮氨酸的重复结构域与GRB2/Cav1结合成复合物而实现上述调控作用的。



