浙江大学生命科学研究院教授朱永群团队最新发表在Science杂志上的1篇论文推动了人们对于病原菌致病分子机制的深入理解,将有助于研发针对创伤弧菌和霍乱弧菌等致病菌的新型抗菌药物。
本文转载自“浙江大学”,原标题:浙大朱永群团队《科学》发文揭示病原菌攻击宿主细胞的新机制。
创伤弧菌是一类让人类谈“菌”色变的病原细菌,俗称“吃人肉细菌”。处理海鲜时如不小心扎了手,创伤弧菌就有可能趁虚而入,迅速引发败血症、组织坏死等,致死率极高。浙江大学生命科学研究院教授朱永群团队近日发现这类病原菌的一项“攻术”:它分泌的毒素会“放冷枪”,定向“冻”住宿主细胞的信号通路,让细胞动弹不得,甚至“散架”。
相关论文Nε-Fatty Acylation of Rho GTPases by a MARTX Toxin Effector在10月27日上线的Science(《科学》)杂志发表(http://science.sciencemag.org/content/358/6362/528),该项研究推动了人们对于病原菌致病分子机制的深入理解,将有助于研发针对创伤弧菌和霍乱弧菌等致病菌的新型抗菌药物。

朱永群团队
故事的主角是两位“R先生”,一位叫RID,一位叫Rac1。RID是MARTX毒素的效应因子,Rac1是宿主细胞的关键信号分子。
创伤弧菌、霍乱弧菌等病原菌会分泌一类MARTX毒素,这类毒素“块头”很大,由4000多个氨基酸残基组成,它穿过细胞质膜时,会把自己“切割”成一小段一小段,成为“小个头”的效应因子进入到细胞质中,RID就是其中的一个,它在MARTX毒素家族中广泛存在。
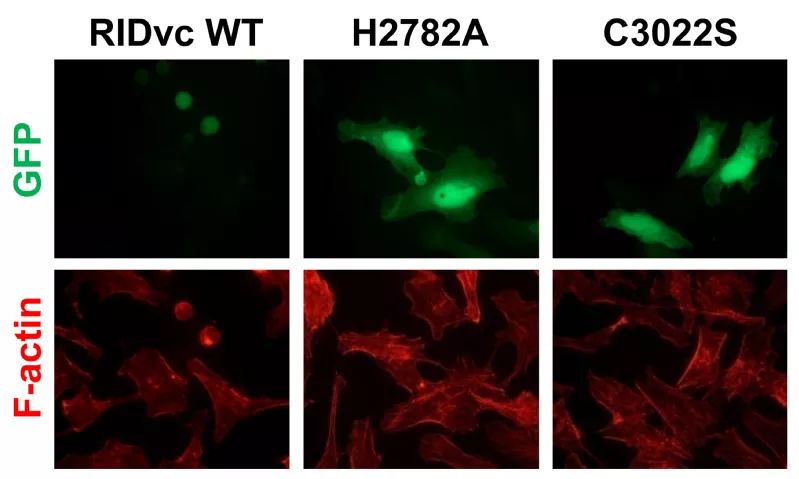
朱永群团队的研究指出,RID在细胞里实施的坏事就是锁定并“冻住”Rac1。Rac1平时循环于细胞膜和细胞质之间,作为一种关键信号分子,参与肌动蛋白细胞骨架的信号调节。就像人类有了骨骼才能运动,肌动蛋白细胞骨架不但支撑出细胞的形状,并为其实现迁移、变形等功能提供了基础。此外,Rac1还参与细胞产生抗菌氧自由基的过程。
RID特异地识别Rac1后,会对其进行修饰。修饰后的Rac1“变样”了,多了一些长长的“脂肪链”。这些“链条”不但让Rac1滞留在细胞膜不能动弹,还屏蔽了Rac1重要的功能区域,阻断了它与上下游的信号传递。这样一来,关键信号分子Rac1就像被RID点了穴,束缚了“手脚”,无法调节肌动蛋白细胞骨架的信号通路,从而破坏了宿主细胞的结构和功能。