
目前,仿制药一致性评价工作正在全国如火如荼地开展着,参比制剂的确定作为一致性评价工作开展的前提,也受到企业的格外关注。截至目前,CFDA共先后四次公布了六批仿制药参比制剂目录,共涉及228个产品,同时,中检院自2016年9月已分七次对2016年5月20日至2017年4月20日期间企业参比制剂备案信息进行了公布。

根据中检院最近一次公布的2016年5月20日至2017年4月20日近一年的企业参比制剂备案信息,笔者对这份长达135页的表格进行了整理和统计(见附表),结果显示,已公布的备案信息中,涉及289目录品种中的240个品种,非289品种外的698个品种。非289品种中有一些为289目录品种的其他规格产品。也就是说已有80%的289目录品种由企业展开一致性评价工作, 甚至多数企业已开始提前开展非289目录品种的一致性评价工作。
在289目录中,企业备案最多的前十个产品分别为阿莫西林胶囊、辛伐他汀片、头孢氨苄胶囊、奥美拉唑肠溶胶囊、盐酸二甲双胍片、苯磺酸氨氯地平片、头孢拉定胶囊、盐酸雷尼替丁胶囊、甲硝唑片、诺氟沙星胶囊。
但目前仍有49个289目录品种未有企业进行备案,即酚酞片、联苯双酯片、呋喃妥因肠溶片、盐酸金刚烷胺片、氢化可的松片、布洛芬胶囊、阿苯达唑胶囊、醋酸甲萘氢醌片、乳酶生片、甲硝唑胶囊、口服补液盐散(Ⅱ)、氨苯蝶啶片、乙酰唑胺片、替加氟片、五氟利多片、阿昔洛韦胶囊、氨茶碱缓释片、司莫司汀胶囊、替加氟胶囊、齐多夫定胶囊、巯嘌呤片、磷酸伯氨喹片、硫唑嘌呤片、白消安片、布洛芬缓释片、硫酸亚铁缓释片、鞣酸小檗碱片、替硝唑胶囊、奥美拉唑钠肠溶片、苯唑西林钠胶囊、琥乙红霉素胶囊、头孢拉定片、盐酸布桂嗪片、盐酸吗 啡缓释片、苯唑西林钠片、复方炔诺酮片、麦角胺咖 啡 因片、维A酸片、盐酸二甲双胍胶囊、对乙酰氨基酚颗粒、醋酸甲地孕酮片、醋酸氢化可的松片、复方醋酸甲地孕酮片、环磷酰胺片、炔雌醇片、乳糖酸克拉霉素片、盐酸克林霉素片、盐酸氯雷他定胶囊、盐酸氯雷他定片。
值得注意的是,在49个尚无企业备案的289目录品种中,除氢化可的松片、布洛芬胶囊、硫唑嘌呤片、白消安片、麦角胺咖啡因片、醋酸甲地孕酮片6个产品的参比制剂信息已由官方公布外,剩下的未备案产品不乏批准文号数量非常多的品种,如酚酞片,目前有79个批文,联苯双酯片有75个批文,呋喃妥因肠溶片有70个批文。也许是因为参比制剂确定困难,或是因为这些品种市场份额不大,大多数企业还在观望,但无论何种原因,如果照这个趋势持续下去,是否预示着这些品种在被企业评估后选择了放弃,同时将在一致性评价后被迫彻底退市。
同时,在已有备案的289目录品种中,一些品种出现了备案数量与批准文号数大相径庭的现象。如复方磺胺甲噁唑片,产品以895个批准文号位列289品种目录首位,但目前企业的备案数仅有35个,不足4%;又如维生素B6片和维生素B2片,批准文号数分别为479个和464个,但企业备案数仅为7个和4个,尚不足批准文号的零头,由此可以预见这些品种的市场将迎来一次全新的大洗牌,多数企业产品可能会被淘汰。
或许是看重品种的长远市场前景,亦或许是出于说明书标注、药品集中采购、医保支付等相关利好政策的鼓励,从企业参比制剂备案信息中可以看出,企业对于非289品种的备案热情远远超过289品种,虽然中间有些是289品种的其他规格产品。
备案企业数量最多的前十位品种分别为替米沙坦片(36家)、盐酸二甲双胍缓释片(33家)、瑞舒伐他汀钙片(26家)、头孢克肟胶囊(25家)、非那雄胺片(22家)、头孢克洛胶囊(20家)、阿莫西林胶囊(0.5g,20家)、注射用泮托拉唑钠(19家)、阿司匹林肠溶片(18家)、阿托伐他汀钙片(18家)。
就在许多企业被289目录的口服固体制剂折磨的死去活来的时候,许多超前的企业已经开始抢占注射剂的先机,在国家还没有相关法规指导注射剂再评价时,对注射剂参比制剂进行备案,初略统计约有90个注射剂参比制剂备案历历在目,看来先下手为强的企业还真不少呢。
离2018年底一致性评价的大限已近不远了,还在犹豫该放弃哪个选择哪个的企业,应该基于中检院公布的参比制剂备案信息,赶快回头筛选一下自己的产品,看看哪些备案少或者还没有备案的产品是不是还可能拣个漏;已经开始的企业,可以根据参比制剂备案提示的品种的竞争激烈程度,重新考虑一些已选品种是否可以放弃,抓几个重头产品有的放矢,不要千军过独桥,避免浪费资源和金钱。


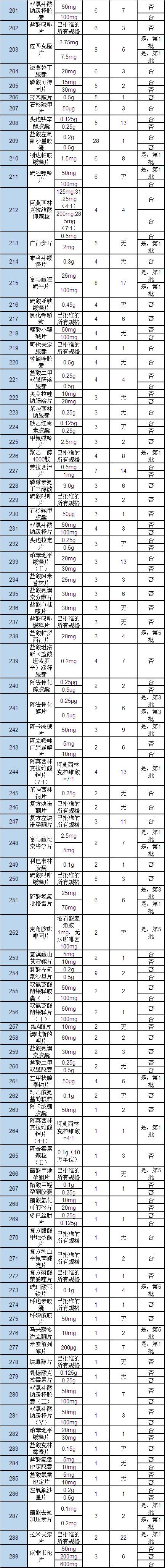
[注1]统计时间:2016年5月31日,数据来源于国家食品药品监督管理总局信息中心(中国食品药品监管数据中心)
[注2] 统计时间:2016年5月31日2017年5月20日;数据来源于中国食品药品检定研究院《企业参比制剂备案情况的信息公开(2016年5月20日至2017年5月20日备案信息)》
内容来源:CPHI制药在线
声明:该文章系转载,登载该文章目的为更广泛地传递医药市场信息,不代表新康界赞同其观点。文章内容仅供参考。
— 精彩回顾 —
点击上图阅读文章






