
“染色体破碎”是剧烈的染色体事件,涉及巨大的染色体断裂和重排,会产生非常灾难性的错误,这种错误的表现形式是大片段的DNA的重排。目前已在各种癌症和先天性疾病中被发现。
上周六,由“VIPaper”与探基学院联合主办的VIPaper文献解读沙龙,邀请了北京大学博士生陈章华来深度解读发表在
Nature
上的一篇“基于染色体破碎事件的胰腺癌进化模型”的文章
。陈章华的研究方向为癌症基因组学,导师白凡博士是北京大学生物动态光学成像中心研究员,生命科学学院研究员,入选第二批“青年千人”计划。已发表多篇高水平论文于《自然》(
Nature
),《科学》(
Science
),《美国国家科学院通讯》(PNAS),《物理评论快报》(PRL) 等世界著名学术期刊。BIOPIC白凡实验室将综合利用单分子生物物理实验手段、单分子荧光显微成像技术、单细胞基因测序技术和系统生物学数学建模方法,研究当前生命科学前沿课题。
下面,让我们一起再来回顾本次沙龙的精彩内容。
肿瘤进化模型-Stepwise progression
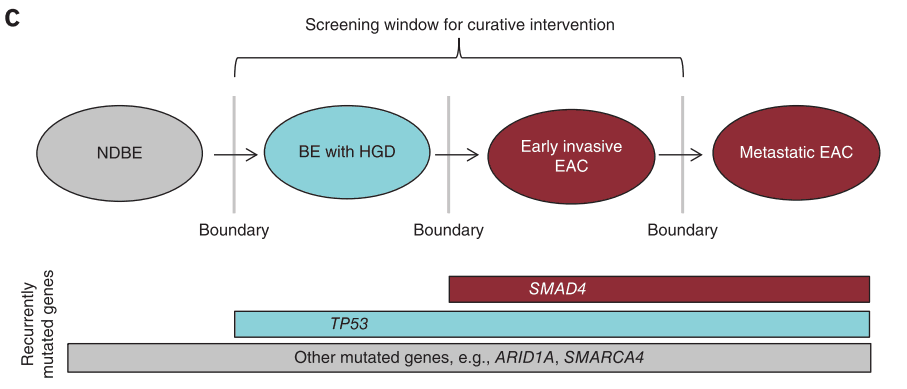
Nat. Genet. 46, 837–43 (2014)
传统的肿瘤进化模型以非常具有代表性的食管癌为例(见上图),在食管腺癌当中有一种食管腺癌特征的组织叫做巴雷特食管,它是由胃部的胃酸反流所导致的,就是在食管位置上面又形成了一层新的腺状上皮的增生。对巴雷特食管、不典型增值及食管癌病人的样本进行分析发现,从正常上皮细胞到巴雷特食管(BE),再到高度的不典型增生(EAC),最终到具有侵袭性特征的EAC,是一个逐渐递增的过程。在这个逐渐递进的过程中,伴随着一些特征性的分子事件的发生,比如在BE阶段就发生了TP53基因的突变,随着BE向不典型增值及侵袭性EAC阶段发展的过程中有SMAD4基因的突变等等。
新的挑战
然而,胰腺癌是一个恶性程度、致死率非常高的肿瘤,而且它会快速的导致转移,所以基于它这种快速转移和非常差的愈后的特点,作者认为胰腺癌的进化模型与前面提到的Stepwise progression模型可能是相对的。因为如果是一步一步发展成侵袭性胰腺癌的,那么在这个过程中应该能找到一个明显的阶段来区分这些侵袭性癌症组织和它的癌前病变的组织。但实际上,在胰腺癌病人中肿瘤的发生都是非常迅速的,所以作者认为在这个肿瘤发生过程当中,并不是遵循Stepwise progression model,它可能存在一些事件会使得肿瘤的发生像一个爆炸一样,这是对现有模型的一个挑战,所以这篇文章基于生物信息学算法,去分析胰腺癌组织中的基因组上DNA 的拷贝数变化,重新探究胰腺癌的演化模型。
1、
多倍性分析工具: Celluloid
鉴于肿瘤细胞并非正常的二倍体,以及肿瘤组织在取样过程中常会受到正常组织的污染等情况,这篇文章用自写的脚本Celluloid 进行校正,并对107例胰腺癌患者的全基因组序列进行多倍性分析,通过可视化图的方式展示肿瘤样本中肿瘤细胞的含量及倍型。(如下图)
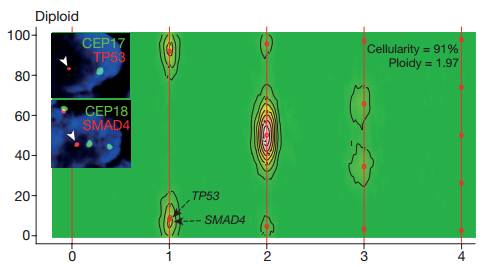

2、
染色体碎裂: Chrom-AL
由于胰腺癌拷贝数变化非常多,文章采用5个标准对染色体碎裂事件进行过滤,最终得到实验分析的结果。

3、
细胞分离方法
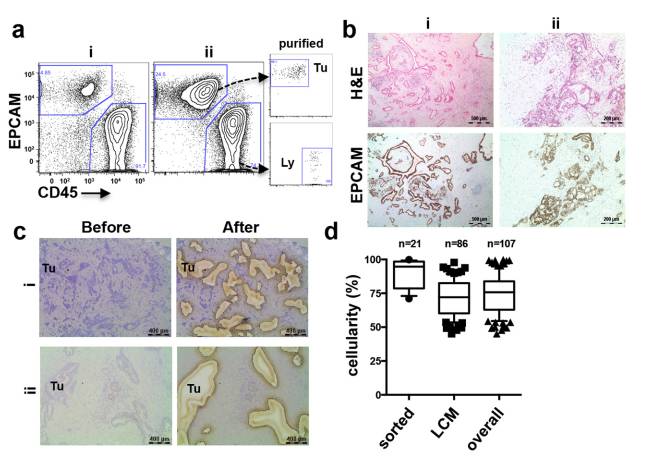
胰腺癌中有很多纤维化的组织,若在采样过程当中不进行处理的话,会对最后的数据分析有很大的影响,新鲜组织样本,采用流式的办法,石蜡样本,采用显微切割的方法,然后对样本中肿瘤细胞含量进行评估,减少正常细胞的影响。
1、大部分突变的积累发生在细胞依然还是二倍体的时候,癌前阶段突变的积累对于肿瘤的发生并没有太大的促进的作用。
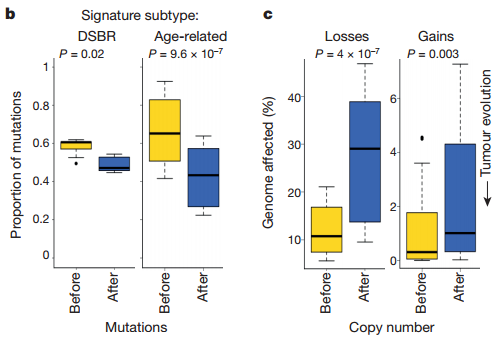
2、拷贝数的变化来自染色体碎裂事件的发生,它是一个非常短期事件,且会伴随着疾病的进程被保留下来,推动肿瘤的发展。
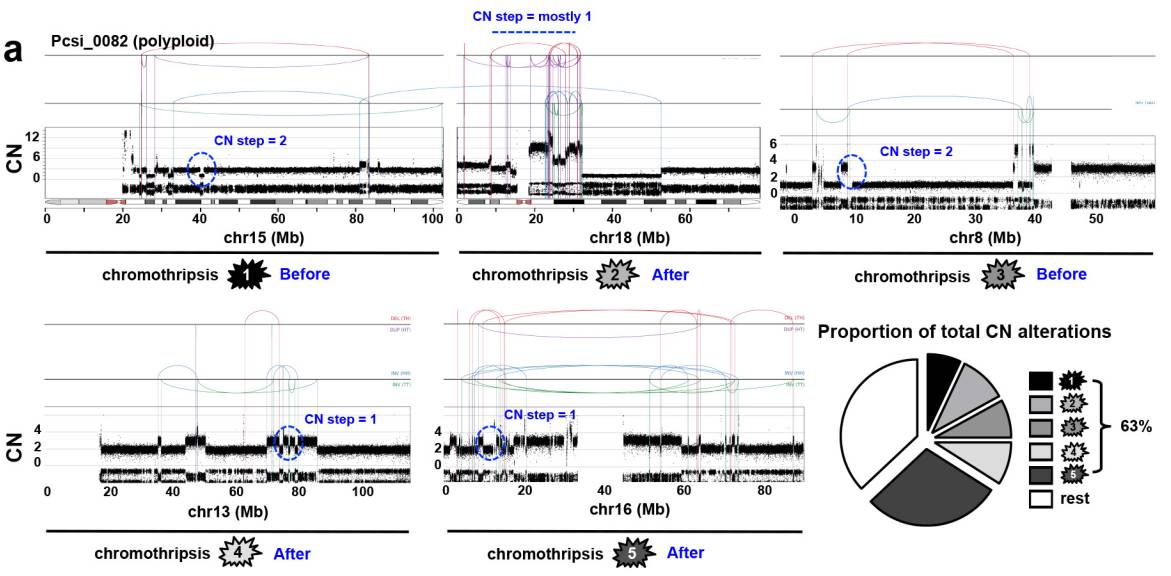
3、染色体碎裂事件的发生会使重要的抑癌基因同时丢失,从而使得肿瘤会突然发展,会突然的转移。
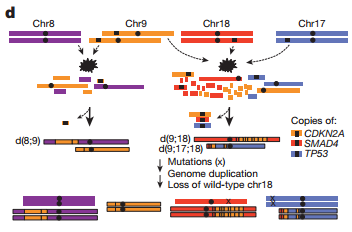
4、一些胰腺癌的发展并不是遵循Stepwise这种肿瘤进化模型,和Stepwise这种肿瘤进化模型相比,它应该是遵循punctuated模型。punctuated模型是说在疾病的进程中,刚开始阶段是一个非常长的潜伏期,但是在这个潜伏期的过程当中,可能伴随着1到2次或者2到3次染色体碎裂事件的发生,使得一些重要的抑癌基因同时丢失,然后会使疾病突然加重或者形成这种转移。
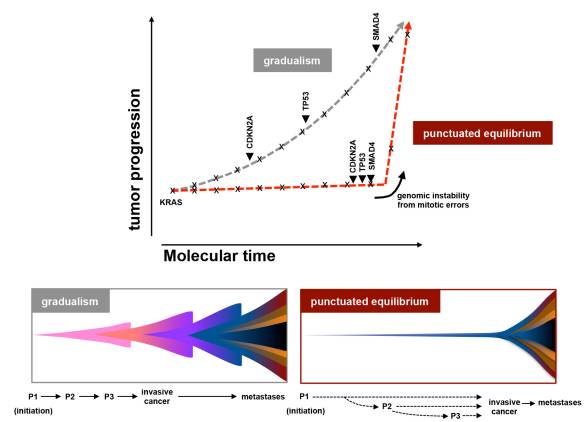
讲者点评
1、故事性非常强的一篇文章,且整个结构的逻辑性也很强。文章中对以往的肿瘤进化模型提出了挑战,并提供了证明胰腺癌进化模型合理性的证据。
2、作者强强联合,有从事消化道肿瘤方向的临床医生,提供稀有的临床样本,还有计算背景的生物学家提出染色体重排的概念。
3、客观因素:2015年测107个全基因的数据,数据量还是很大的。
文章作者简介
这篇文章有两位通讯作者,分别是来自于两个不同的机构,其中第一单位是加拿大的多伦多总医院研究所(UHN),Steven Gallinger是一位临床医生,在本研究中主要提供了临床样本,作为临床医生他主要关注和消化道肿瘤相关的一些疾病,运用genetics和genomics的一些技术探索疾病的发病机制。
第二位通讯作者Peter Campbell,是英国桑格尔研究所的一个PI,作为cancer genomics领域中的领军人物,Peter Campbell在cancer以及ageing相关领域每年都有2~4篇CNS主刊的文章发表。如下列出了和本文相关性比较大的几篇CNS文章,第一篇2013年的发表于cell,这篇文章中运用测序的数据在肿瘤中发现了“染色体碎裂”这种现象,2015年的发表在Science上的文章发现肿瘤的进化可能是一个正向选择的过程;另外本月新发表在Cell上的一篇文章对TCGA涵盖的包括20多种肿瘤,总共7000多个样本中所有的突变,做了一个选择分析,发现不同的肿瘤类型,肿瘤发生过程中所需要的driver mutation的数目。
VIPaper
探索CNS,追踪前沿知识

关注VIPaper,回复“肿瘤进化”获取完整版的课件及语音!
探基学院
聚焦基因科技、精准医学领域的学习互助平台

测序中国
本月最新Cell文章,肿瘤微环境与免疫,北大陈西茜博士倾情解读!
“Tumor and Microenvironment Evolution during Immunotherapy with Nivolumab”。文章通过对67例黑色素瘤病人在经nivolumab免疫治疗前后的外显子组 转录组等的比较,探究了用药期间肿瘤及微环境的进化过程,提示出体内对nivolumab的响应机制。
清华大学古槿、张奇伟课题组联合完成,核酸研究期刊,
单细胞转录组数据分析,第一作者李翔宇亲自解读!
“Network embedding based representation learning for single cell RNA-seq data”。单细胞转录组数据为我们进行细胞异质性的研究提供了强有力的工具,文章中提出了一个基于网络嵌入(network embedding)的表示学习方法SCRL,且实验表明SCRL在多组近期的单细胞转录组数据上都表现卓越。
沙龙时间
2017年11月25日(周六),14:30~17:00
坐标
北京中关村附近
报名方式
扫下方二维码,请备注“姓名+单位+科室”,报名及获取文章全文

· END ·






