-
5 月受理量增加 50%,创去年稳定后新高。
-
诺华制药 5 月受理号 18 个,涉及 10 个品种,居本月受理号排行榜第一
-
恒瑞医药 3 个 1 类化药,均为特殊审批
-
大冢制药泊那替尼片,国内首次申报临床
-
5 月审评审批数量下降 35%,创新化药仅有 1 个品种
-
广生堂替诺福韦抗病毒首仿药上市获批
-
沈阳三生制药再次申报重组人血小板生成素注射液获批临床
5 月受理量增加 50%,创去年稳定后新高
根据丁香园 Insight - China Pharma Data 数据库最新统计, 2017 年 5 月 CDE 共承办新的药品注册申请以受理号计有 419 个,较上月增加 50%,创去年稳定后新高。在受理品种上,共有 277 个品种受理,相比过去几个月,有较高的增长。

以下,分别来分析 2017 年 5 月化药、中药、生物制品的申报受理及审评审批情况。
申报受理情况
一、 化药
根据 Insight 数据库统计,2017 年 5 月 CDE 共承办新的化药注册申请以受理号计有 319 个,受理品种 200 个,对比上月有所增加。化药各序列申报受理情况如下表:
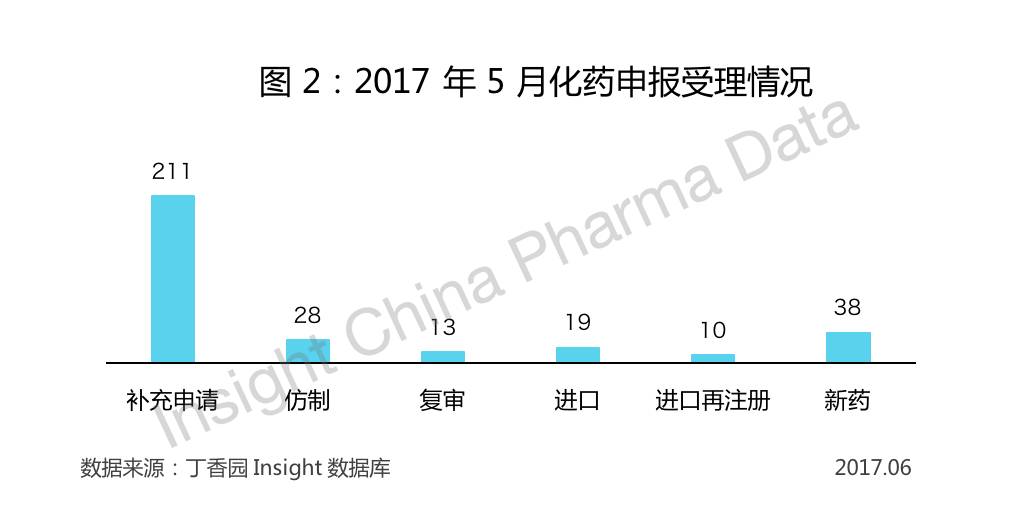
在本月 CDE 承办的新的化药注册申请的受理号中,诺华制药 5 月受理号 18 个,涉及 10 个品种,居药企受理号排行榜第一,其他药企 CDE 化药申报数量排名(前 15 )情况如下:
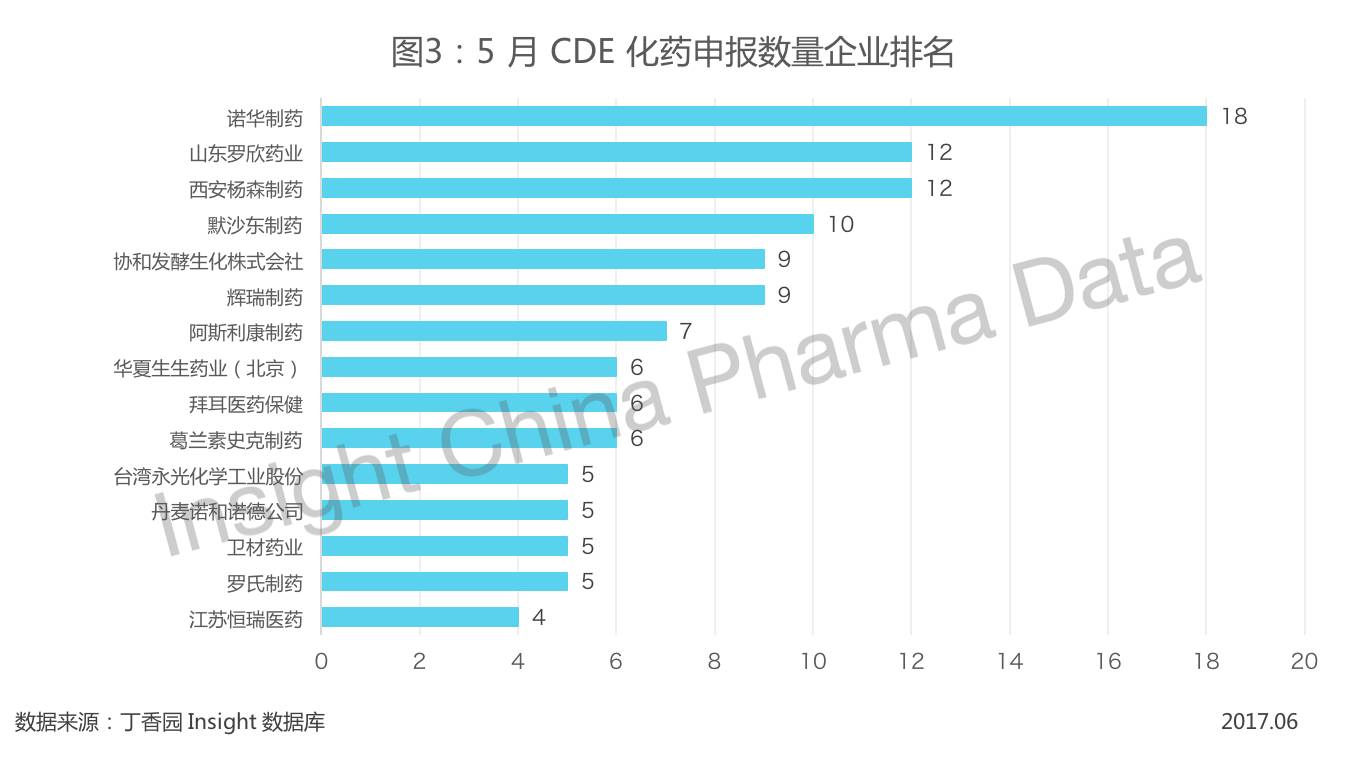
1. 新药
5 月创新药继续回升
根据 Insight 数据库统计, 2017 年 5 月 CDE 共承办化药 1 类新药申请以受理号计有 31 个,涉及 22 个品种,2017 年 3 月创新化药受理 27 个品种,4 月下跌为 10 个,5 月有所回升。
下面让我们来看 17 年 5 月申报受理的具体品种有哪些?
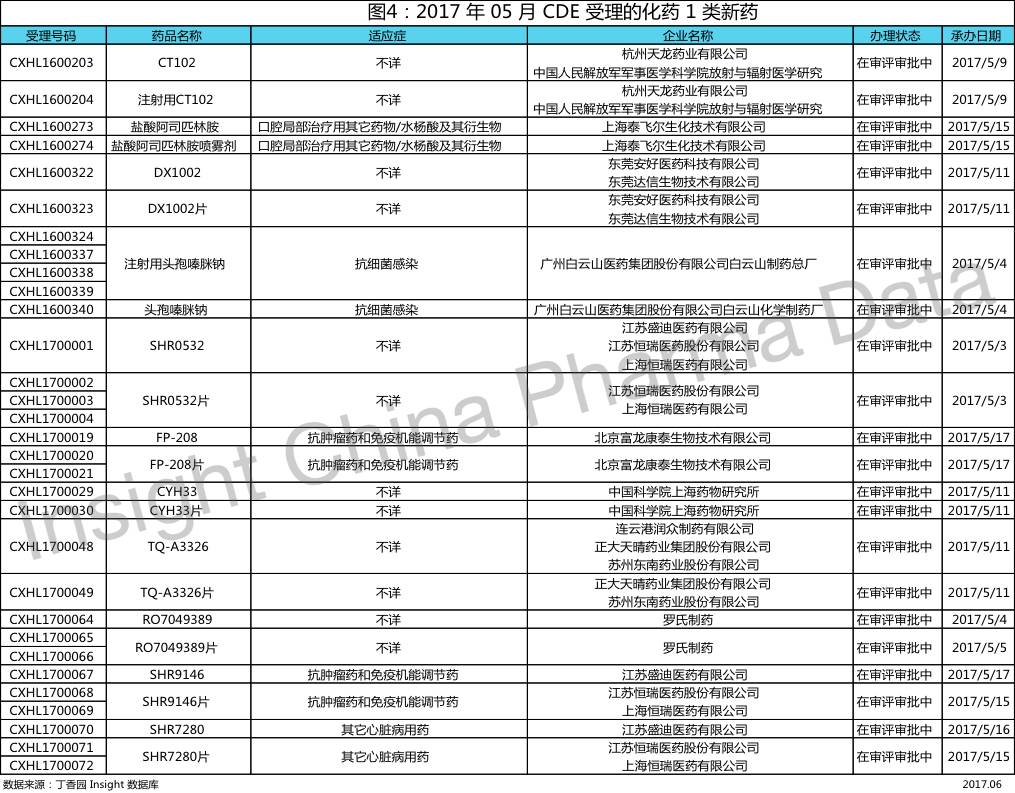
恒瑞医药3个1类化药,均为特殊审批
本月,恒瑞医药有 3 个 1 类化药进入 CDE,均为特殊审批。根据恒瑞 3 月份发布的公告显示,其向 FDA 提交了 SHR9146 临床注册申请并获受理,本品为口服、强效的小分子 IDO 抑制剂。IDO 是肿瘤免疫疗法中重要的小分子调控靶点,该靶点暂无药物上市,研发中的代表药物有 Incyte 公司开发的 Epacadostat。
SHR7280 原料药及其片剂,适应症为其他心脏病用药;还有 SHR0532 原料药及其片剂,适应症不详。
罗氏制药申报 1 类化药 RO7049389 原研药及其片剂,据悉本品是一种抗乙型肝炎病毒新药,为 HBV 衣壳蛋白装配抑制剂。
除此之外,上海泰尔飞生化申报 1 类新药盐酸阿司匹林胺原料药及其喷雾剂,白云山医药申报 1 类化药头孢嗪脒钠及注射剂,富龙康泰生物申报 1 类抗肿瘤靶向治疗新药 FP-208 原料药及其片剂。
其它药物暂无消息。
2. 仿制
2017 年 5 月,CDE 共承办化药仿制药申请以受理号计共有 28 个,涉及 19 个品种,较上月有所增加,其中按旧的 6 类申报的仿制药以受理号计有 16 个,涉及 10 个品种;按新的 4 类申报的仿制药以受理号计有 8 个,涉及 5 个品种。
按新的 3 类申报的仿制药以受理号计有 4 个,涉及 4 个品种。它们分别是:

3. 进口化药
2017 年 5 月,CDE 承办新的化药进口注册申请以受理号计有 19 个,所有申请共涉及 16 个品种,较上月有所下降。其中 5.1 类申请以受理号计有 3 个,涉及 3 个品种。5.2 类申请以受理号计有 8个,涉及 8 个品种。具体情况如下图:

大冢制药泊那替尼片,国内首次申报临床
大冢制药申报 1 类进口化药泊那替尼片,英文名为 ponatinib,于 2012 年底在美国上市。据悉本品属于三代酪氨酸激酶抑制剂,用于治疗慢性粒细胞、急性淋巴细胞性白血病。
诺华制药再次提交 LEE011 的临床申请,受理号 JXHL1700094,注册分类 2.4。据悉,LEE001 是诺华与Astex Pharmaceuticals 联合开发的一种有选择性的周期蛋白依赖性激酶 (Cyclin-Dependent Kinase, CDK) 抑制剂。它能够有选择地抑制 CDK4 和 CDK6 的功能。在此之前,针对本品种在国内申报 6 项临床申报,均已通过。
二、中药
2017 年 5 月 CDE 共承办中药新申请以受理号计有 30 个,其中 3 个新药申请(涉及 3 个品种), 24个补充申请(涉及 24 个品种), 1 个进口再注册(涉及 1 个品种), 2 个复审(涉及 2 个品种)。
三、生物制品
2017 年 5 月 CDE 共承办生物制品新申请以受理号计有 67 个。其中 16 个新药申请(涉及 16 个品种), 9 个进口申请(涉及 9 个品种)、40个补充申请(涉及 18 个品种)和 2 个复审。
本月有 6 个治疗用生物制品 1 类新药,它们是:
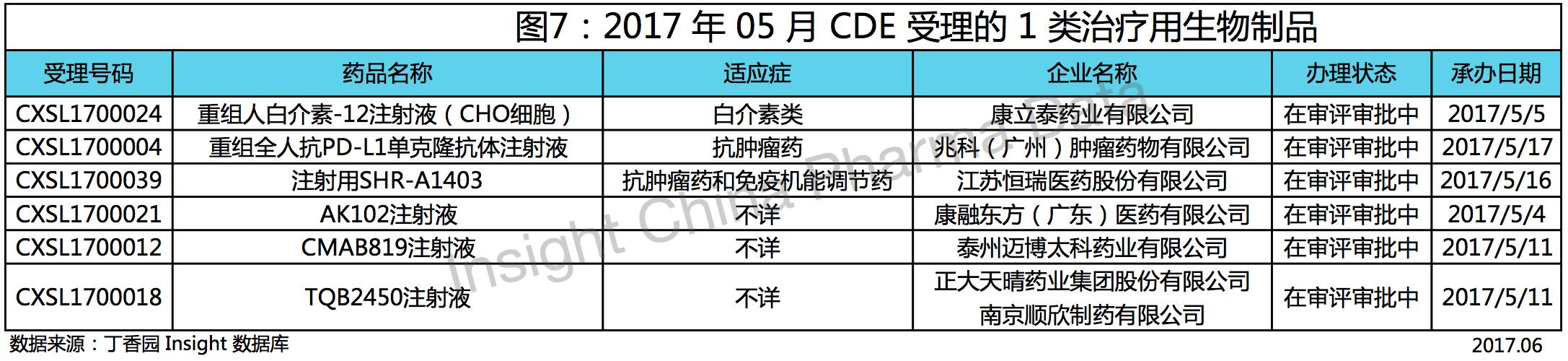
恒瑞医药申报1类生物新药注射用 SHR-A1403
SHR-A1403 为人源化抗 c-Met 单克隆抗体通过化学偶联微管抑制剂之后形成的抗体药物偶联物,可通过与肿瘤细胞表面的 c-Met 结合,将抗体药物偶联物内吞进入肿瘤细胞后,在溶酶体发生降解后释放小分子毒素,起到杀伤肿瘤细胞的作用。在今年 1 月,恒瑞医药向外公布,FDA 允许注射用 SHR-A1403 在美国进行临床试验。据悉,目前国内外尚无已上市的同靶点的同类型产品。
审评审批情况
1. 总体审评审批情况
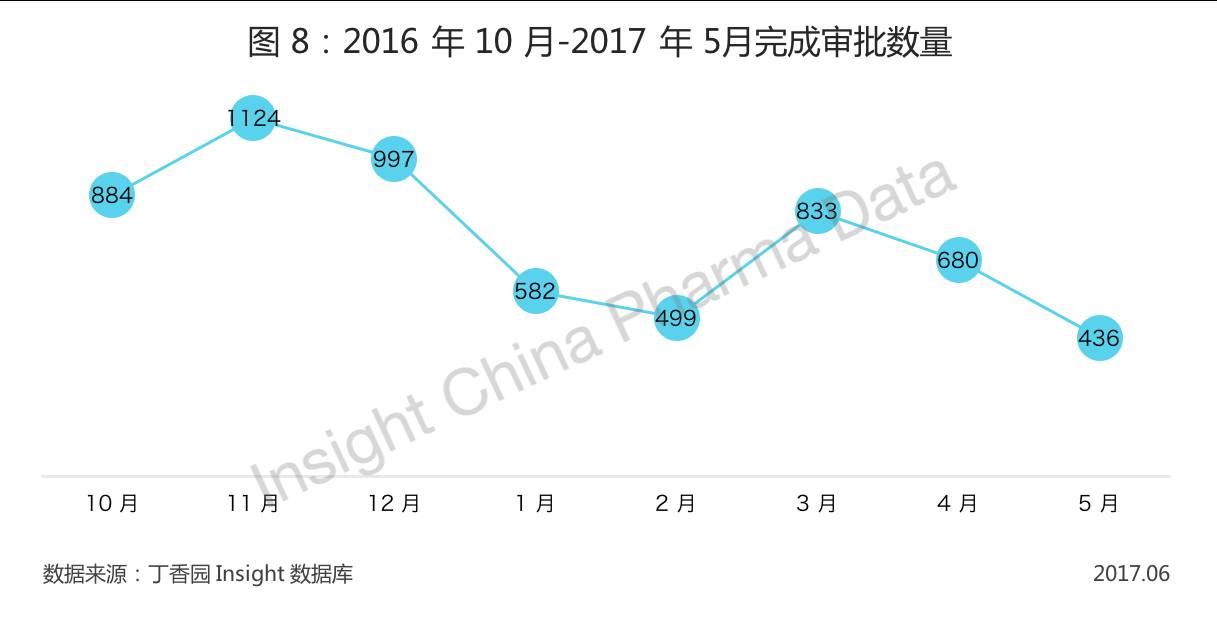
根据 Insight 数据库高级筛选,2017 年 5 月共有 436 个受理号完成审评。相较上月的 680 个,减少了 35%。
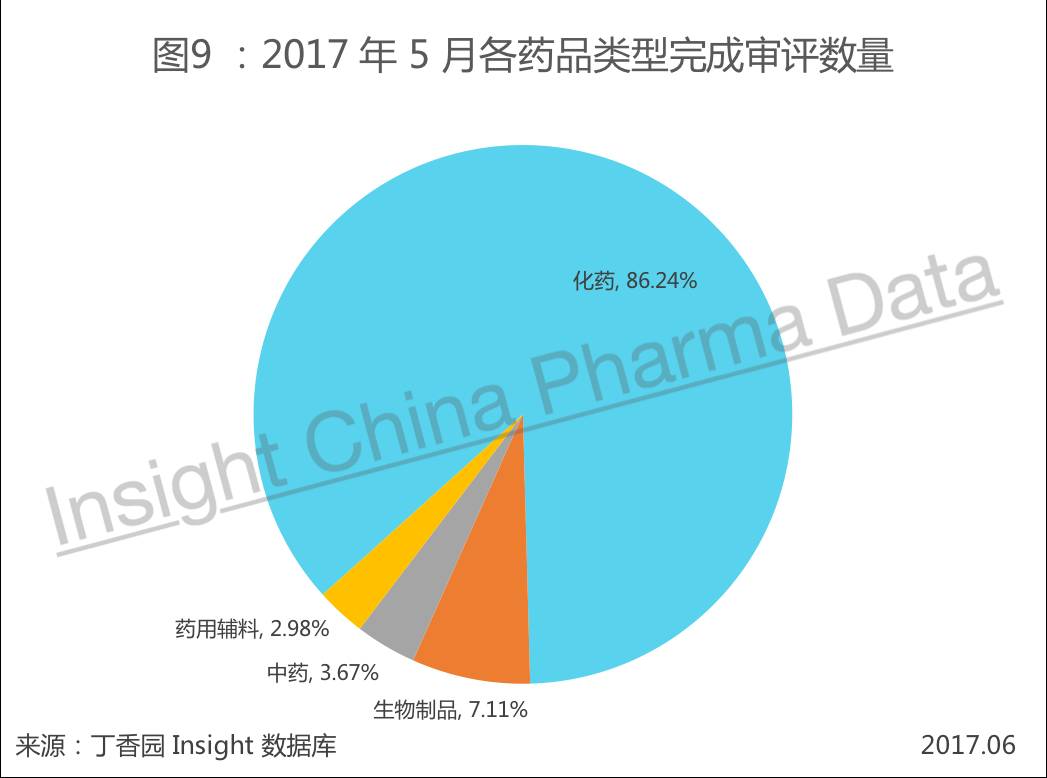
2. 化药各审评序列的审评审批情况
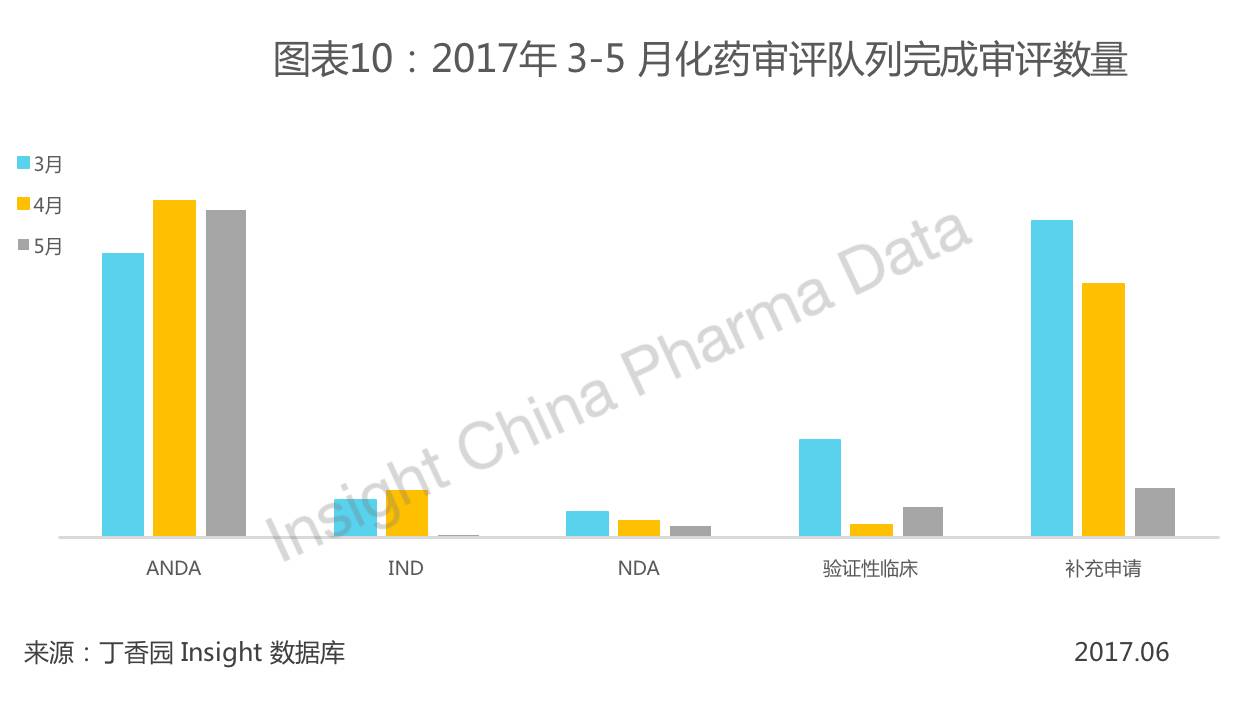
2017 年 5 月共有 363 个化药受理号完成审评。如图表 10 所示, 5 月各序列完成审评数量上与上个月对比, ANDA 和 NDA 审评完成量有所下降,IND 和补充申请下降较大,而验证性临床在 4 月下降的基础上有所上升;
3. 本月重要化学品种
据 Insight 数据库统计,2017 年 5 月离开 CDE 并且获批临床的化药受理号共有 31 个,其中比较重要的品种的具体情况如下:
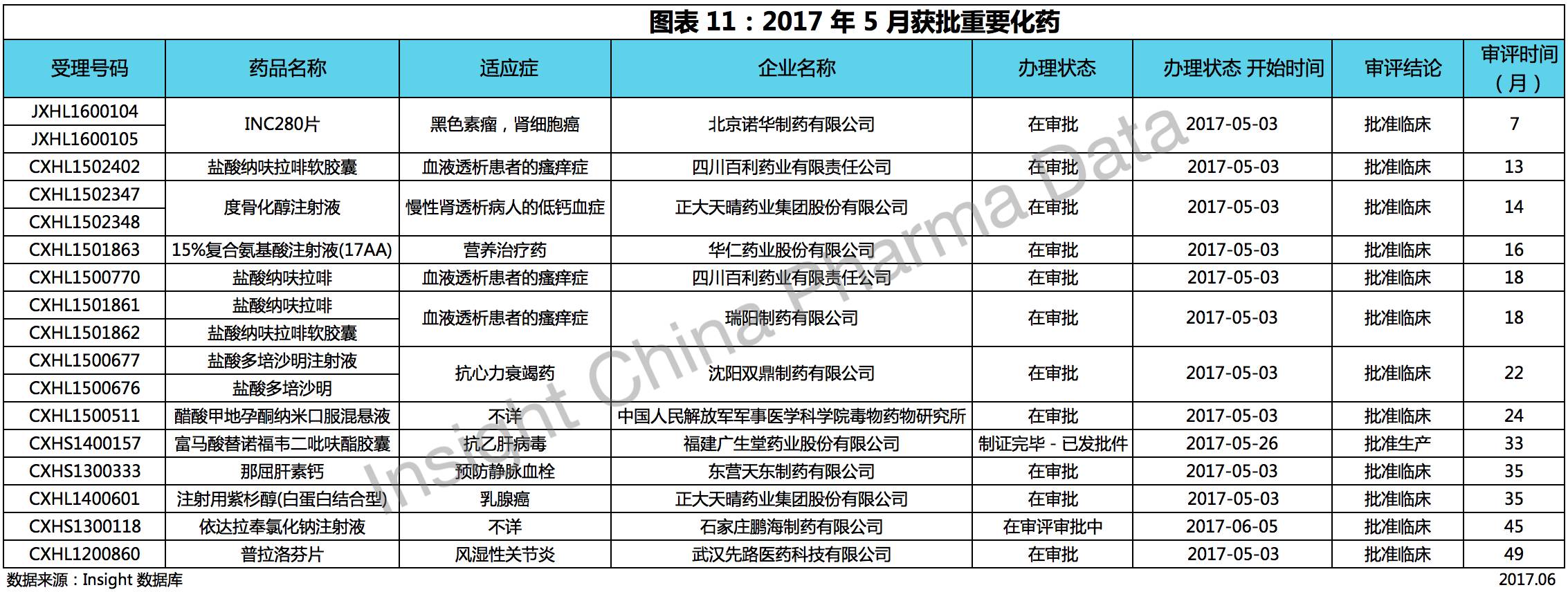
广生堂富马酸替诺福韦二吡呋酯胶囊剂获上市批准
广生堂的富马酸替诺福韦二吡呋酯胶囊剂获 CFDA 生产注册批件,成为国内首个获批治疗乙肝适应症的替诺福韦酯仿制药,但剂型为胶囊剂。
另有,诺华制药的 1 类新药 INC280 片获批临床,是本月唯一获批的 1 类化学新药。本品于 2016 年 9 月 CDE 承办,为特殊审评品种,适应症为用于治疗黑色素瘤和肾细胞瘤。
4. 重要生物制品审评审批情况
据 Insight 数据库统计,2017 年 5 月获批临床的 1 类生物制品有 1 个,涉及 2 个受理号。沈阳三生制药申报的重组血小板生成素注射液获批临床,具体情况如下:

沈阳三生制药再次申报重组人血小板生成素注射液获批临床
重组人血小板生成素注射液为沈阳三生制药独家申报品种,共有申报受理号 17 个,其中上市申请 2个,在 2005 年获批;临床申请 6 个,获批 4 个;补充申请 9个,获批 4 个。
如需下载
2017 年 4 月 CDE 药品审评报告
全文的 pdf 版本,请
在公众号中回复「
201705
」。
本文系 Insight 原创文章,转载请注明「作者:Insight 数据库,来源:Insight 数据库」
↓ ↓ ↓
点击「
阅读原文
」,即可免费获取一个 Insight 账号,以上所有数据均可快速获得,快来体验吧!




