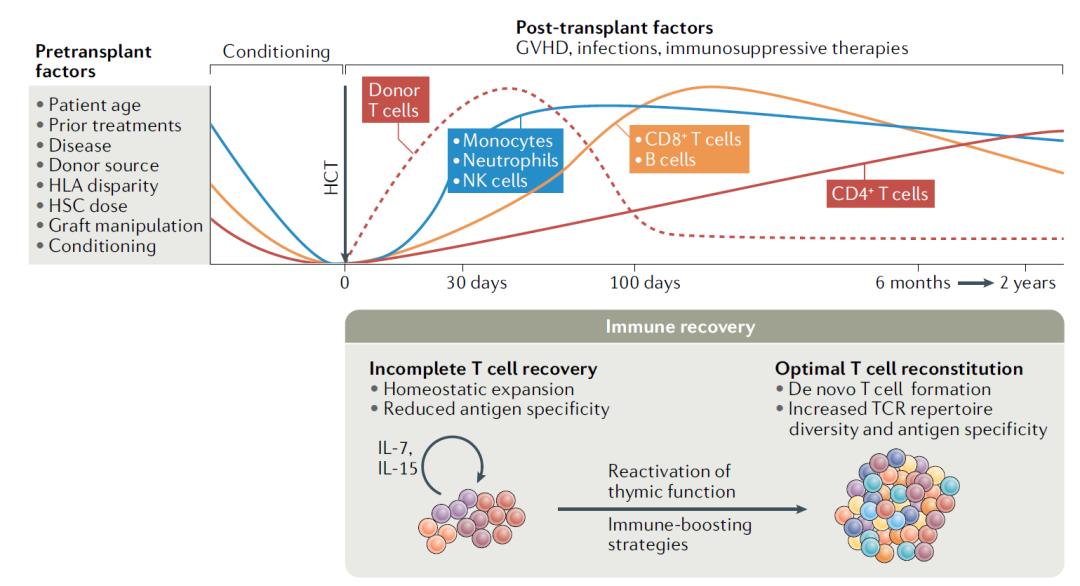
化疗,放疗,感染等,引起免疫系统的损伤,之后免疫系统的重建,尤其是T细胞再生恢复,与病人预后密切相关。但是,损伤之后,适应性免疫,尤其是T细胞的恢复,比起天然免疫细胞要慢很多。
感染
健康机体,免疫细胞通过再生和死亡实现平衡。在感染发生后,这种平衡被打破。
感染发生后,造血干祖细胞(HSPCs)通过模式识别受体直接感知病原体,或者间接通过感知下游细胞的消耗,补充免疫细胞。
急性感染,HSPCs更多分化为粒细胞,在脓毒血症,导致早期胸腺祖细胞清除,淋巴细胞减少。
胸腺细胞和基质细胞本身也是病原体喜欢攻击的目标,尤其是CD4+CD8+双阳胸腺细胞和D24hiCD3lowCD8+单阳胸腺细胞,而成熟的CD24mid/lowCD8+单阳细胞是耐受最好的细胞。应激反应激素(如糖皮质激素),促炎介质(如IFNγ,TNF-α)和凋亡途径(如介导的由BAX,BCL-2,p53,caspase8和caspase9)参与其中。
寨卡病毒,麻疹病毒等,也会攻击胸腺基质细胞(mTECs,cTECs),引起增殖,分化,迁移等改变。
新冠肺炎中,中国科学家也发现,淋巴细胞数量减少和炎症因子(IL-6,IL-8)相关。

急性感染引起的胸腺萎缩通常是暂时的,但是像HIV等慢性感染可能会引起不可逆的胸腺萎缩。
细胞消融疗法
放疗,化疗,细胞清除抗体治疗等方法,被用于清除恶性细胞。造血干细胞移植前,也需清除免疫细胞,尤其T,B细胞,以提高移植成功率。
清除造血干细胞和淋巴祖细胞,会导致胸腺T细胞和骨髓中B细胞的发育长期受损,甚至会加速胸腺的退化。
另外环磷酰胺,放疗,也会清除胸腺基质细胞cTECs 和 mTECs,此二者是T细胞发育阳性选择和阴性选择所需要的。
随着年龄增长,免疫系统衰老,功能下降,易发生感染,同时对于疫苗的免疫应答不足。
免疫功能下降的因素:
-
刺激T细胞发育和扩增:IL-7,IL-12,IL-21,SCF(stem cell factor),KGF7(keratinocyte growth factor),IL-22,FLT3LG等
-
调节激素:类固醇,胸腺肽α1, 生长激素,IGF1,ghrelin
-
淋巴祖细胞的过继转移,以及人工BM或胸腺样移植物。
-
IL-7被归类为1型短链细胞因子对先天和适应性免疫细胞的发育至关重要。
主要分泌细胞为非造血细胞,包括上皮细胞,胸腺成纤维细胞、BM基质细胞、淋巴管内皮细胞,成纤维细胞网状细胞和肠细胞。
Cytheris SA的CYT107,在HIV临床试验,开展到2期,显示可以增加CD4+T细胞数量,后于2013年终止(NCT01241643)。
CYT107也开展了CD4+T淋巴细胞减少症临床(NCT00839436),可以增加循环中CD4+T和CD8+T,以及组织中的CD3+T,在年轻病人(23岁和34岁),可以引起胸腺发生。2015年因为Cytheris破产,临床终止。
国内天镜(TJ107)引入韩国Genexine的GX-I7( IL-7-hyFc),开发肿瘤相关淋巴细胞减少症,以及和PD-1/PD-L1抑制剂联用。
NCT04001075,Investigate the Safety, Tolerability, Pharmacokinetics and Pharmacodynamics of TJ107 in Chinese Patients With Advanced Solid Tumors
KGF是TECs细胞主要的生长因子,由胸腺间充质细胞分泌。KGF通过PI3K–AKT–nuclear factor-κB / p53信号通路促进TECs增殖。
palifermin(Kepivance,帕利夫明),2004年FDA批准恶性血液病的口腔粘膜炎。后续被用于移植后,T细胞重构的临床研究((NCT01233921, NCT03042585,NCT02356159,NCT00593554),目前没有阳性结果。
在一项Alemtuzumab(CD52抗体)治疗MS后,palifermin促进胸腺发生的试验(NCT01712945),也失败终止了。
Somatropin (recombinant human growth hormone)和胸腺肽α1进行了一系列临床试验(NCT00071240,NCT00287677,NCT00119769,NCT00050921,NCT00580450),进行HIV感染后免疫重建以及肿瘤相关的淋巴细胞减少症,最终都没有明确的阳性结果。














