
蛋白质的自组装允许从相对简单的构建块中形成不同的超分子材料。
中国科学院大学郑立飞、刘庆等
利用重组蛋白CsgA开发了一种单组分自组装水凝胶,并证明了其在脊髓损伤修复(SCI)中的成功应用
。通过CsgA纳米原纤维的物理纠缠实现凝胶化,从而在低浓度下产生自支撑水凝胶(≥5mg mL
−1
)。利用CsgA基因序列的可编程性,通过融合功能肽GHK,可以增强生物活性水凝胶。GHK因其抗炎、抗氧化和神经营养因子刺激特性,成为脊髓损伤修复的候选。体外实验表明,CsgA-GHK水凝胶可以调节小胶质细胞M2极化,促进神经干细胞的神经元分化,抑制星形胶质细胞分化。在脊髓腔压迫性损伤大鼠模型中,该水凝胶在减轻炎症和促进损伤部位的神经元再生方面具有疗效,导致显著的功能恢复。这些发现为开发重组CsgA蛋白水凝胶在组织修复应用中的模块化设计平台奠定了基础。
相关研究内容以
“
Genetically Programmed Single-Component Protein Hydrogel for Spinal Cord Injury Repair
”为题于2025年1月10日发表在《
Advanced Science
》。
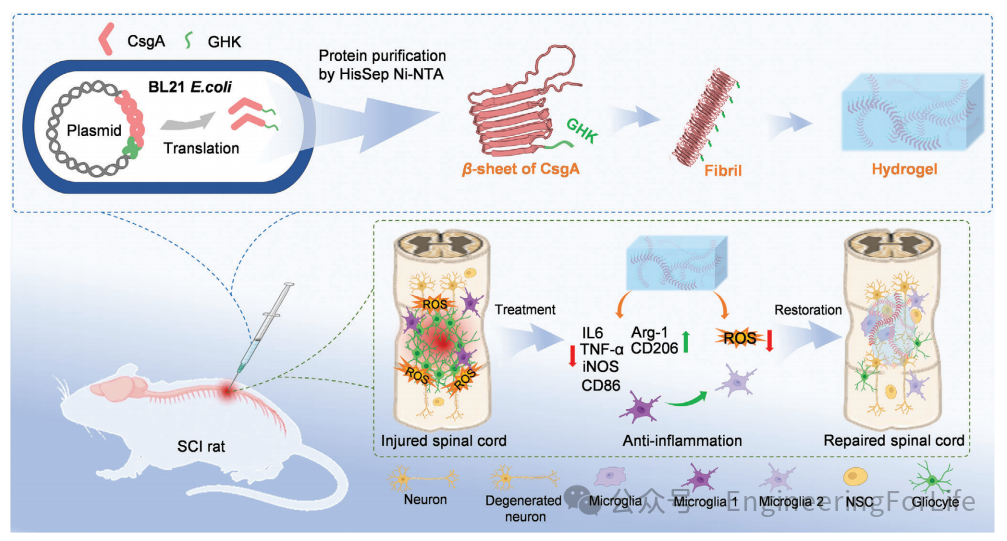
图1 CsgA-GHK自组装纤维水凝胶示意图
为了使水凝胶具有抗炎特性,将人铜结合肽GHK(甘氨酸-L-组氨酸-L-赖氨酸)与CsgA融合。用小鼠小胶质细胞BV2细胞系进行的体外实验表明,CsgA-GHK凝胶可以调节细胞的氧化微环境,显著促进抗炎M2小胶质细胞极化。此外,它还具有促进神经干细胞(NSCs)神经元分化的能力。体内研究表明,植入CsgA-GHK水凝胶可显著改善脊髓损伤后大鼠的功能恢复。因此,本研究可能为在组织修复和再生领域设计功能基因编程蛋白自组装水凝胶铺平道路(图1)。
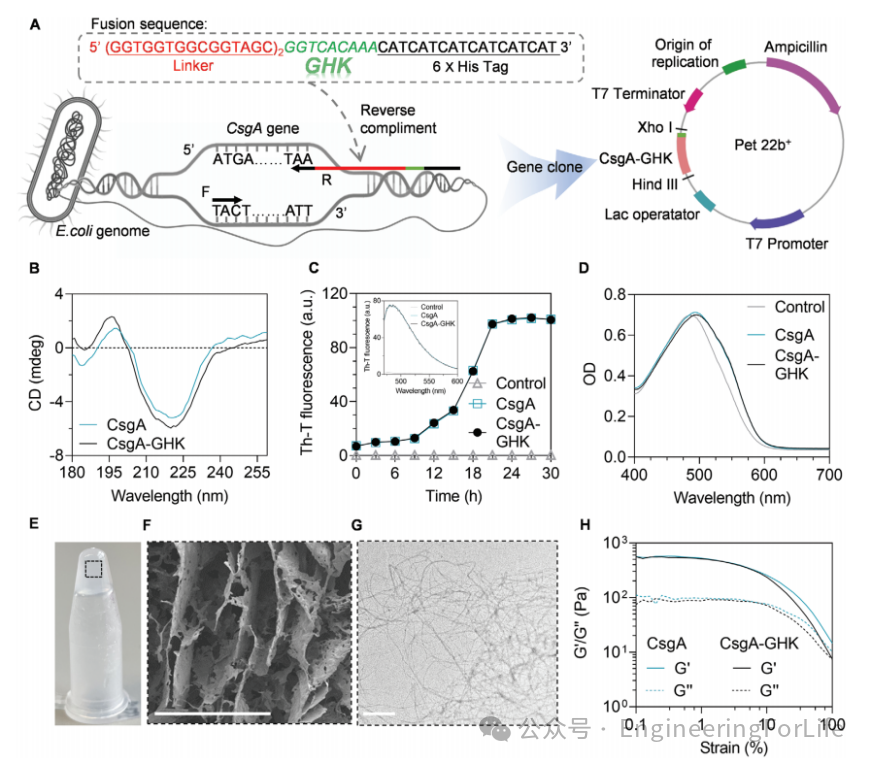
图2 CsgA和CsgA-GHK水凝胶的表征
为了获得重组的CsgA和CsgA-GHK蛋白,本研究构建了pET22b
+
-CsgA和pET22b
+
-CsgA-GHK表达载体,在E. coli BL21菌株中进行蛋白表达(图2A)。两种蛋白在195 nm处有相似的正峰,在220 nm处有相似的负峰,说明GHK的融合对β-sheet结构形成的影响可以忽略不计(图2B)。通过硫黄素T(ThT)实验研究溶液中CsgA或CsgA-GHK的纳米纤维形成。在CsgA或CsgAGHK溶液中加入ThT染料后,荧光强度随时间增加,呈明显的滞后、生长和固定相的s型曲线(图2C)。此外,在CsgA或CsgA-GHK蛋白溶液中观察到刚果红(CR)结合,导致CR吸收光谱出现明显的红移(图2D)。通过透射电镜(TEM)直接观察到CsgA和CsgA-GHK的纳米纤维结构(图2G)。凝胶化48小时,然后离心去除多余水,得到最终的水凝胶(图2E)。扫描电镜(SEM)分析揭示所得到水凝胶的多孔结构(图2F)。当菌株增加到10%时,存储模量(G')和损失模量(G″)均下降,在100%左右出现交叉点(图2H)。
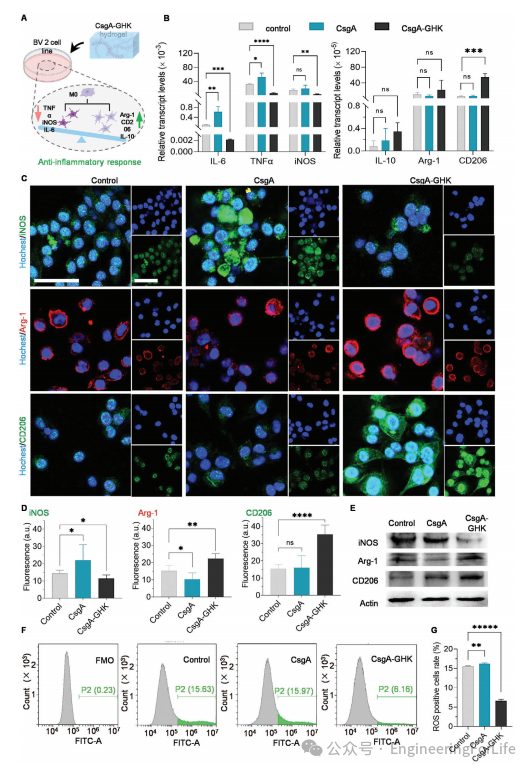
图3 小胶质细胞极化分析
小胶质细胞可以表现出促炎(M1)或抗炎(M2)表型,这些表型包含特定的标记物(图3A)。基因表达分析显示,CsgA-GHK水凝胶培养的BV2细胞中促炎细胞因子(IL-6、TNF和iNOS)的mRNA水平显著低于对照组,抗炎细胞因子(IL-10、Arg-1和CD206)的mRNA表达水平高于对照组,其中CD206的表达显著上调(图3B)。BV2细胞的免疫荧光(IF)成像显示,与对照组相比,CsgA-GHK组的iNOS阳性细胞数量显著减少,而Arg-1/CD206阳性细胞数量显著增加(图3C、D)。通过WB分析评估炎症调节,包括Arg- 1、iNOS和CD206蛋白的表达(图3E),表明
CsgA-GHK水凝胶促进M2小胶质细胞极化
。流式细胞术量化结果显示,CsgA-GHK组ROS阳性细胞比例为6%,与对照组和CsgA组相比,减少60%,两组ROS阳性细胞均约为15%(图3F、G)。
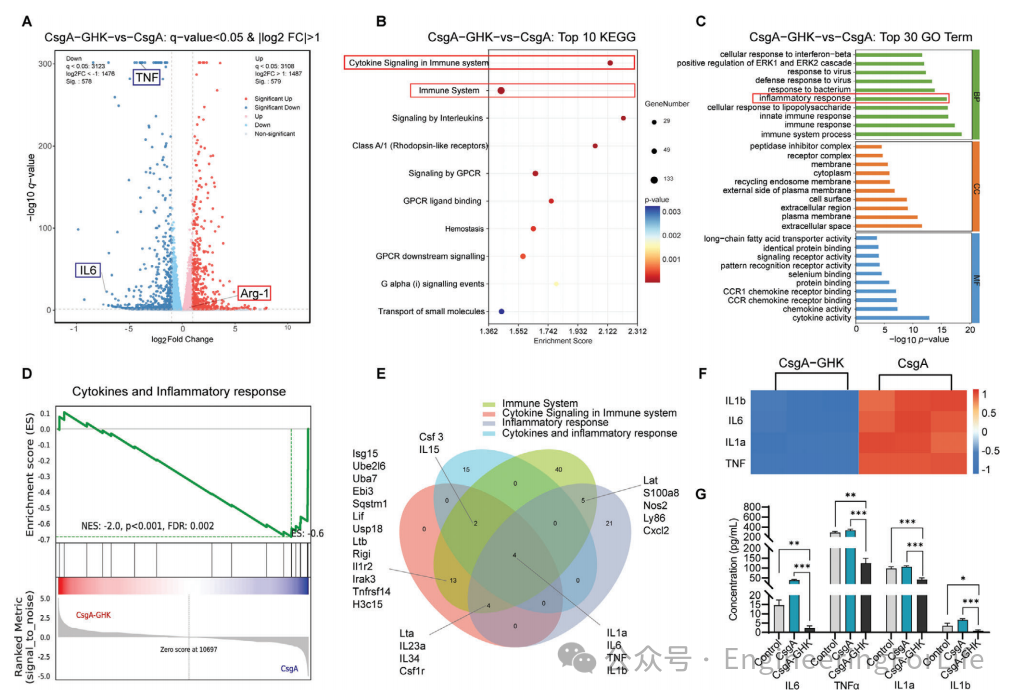
图4 用CsgA-GHK和CsgA水凝胶处理的BV2细胞的RNA-seq
为进一步阐明CsgA-GHK水凝胶处理对BV2细胞影响的分子机制,进行RNA-seq数据分析。与CsgA组相比,CsgA-GHK水凝胶处理导致579个基因上调,578个基因下调(图4A),进一步表明GHK肽对基因表达谱的影响。KEGG通路分析显示,免疫系统是最显著的富集途径。此外,另一种途径“免疫系统中的细胞因子信号通路”已被富集,表明CsgA-GHK水凝胶处理对免疫相关过程的影响(图4B)。分子功能(MF)分类突出与免疫炎症反应相关的通路,如免疫反应,和CCR趋化因子受体结合信号通路(图4C)。此外,基因集合富集分析(GSEA)结果显示,细胞因子和炎症反应通路发生显著变化(图4D)。常见基因的维恩图显示,所有筛选的通路中都包含IL1b、IL6、IL1a和TNF基因(图4E)。基因表达热图显示,与对照组和CsgA组相比,CsgA-GHK水凝胶处理下调多种促炎因子的表达(图4F)。ELISA结果也证实,与CsgA或对照组相比,CsgA-GHK水凝胶对IL6、TNF、IL1a和IL1b蛋白的表达有调控作用(图4G)。综上所述,
CsgA-GHK水凝胶通过调节促炎细胞因子的表达,激活炎症反应通路,发挥其抗炎功能。
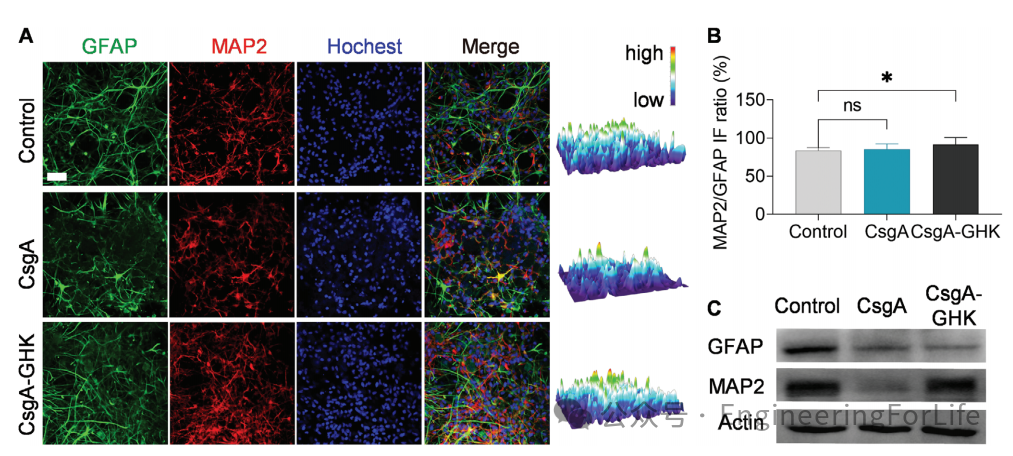
图5 NSC分化行为的比较
MAP2 IF图像的3D热图和WB结果均显示,与CsgA组相比,MAP2在对照组和CsgAGHK组中高表达;与对照组相比,CsgA组和CsgA-GHK组中GFAP蛋白的表达显著降低(图5A、C)。MAP2/GFAP在对照组、CsgA组和CsgAGHK组的荧光强度比值分别为83.7%、85.4%和91.4%,其中CsgA-GHK组的荧光强度显著高于其他组(图5B)。因此,
CsgA-GHK水凝胶为神经元的生长创造一个良好的微环境,同时减少胶质细胞的分化,从而导致GFAP和MAP2表达的改变。
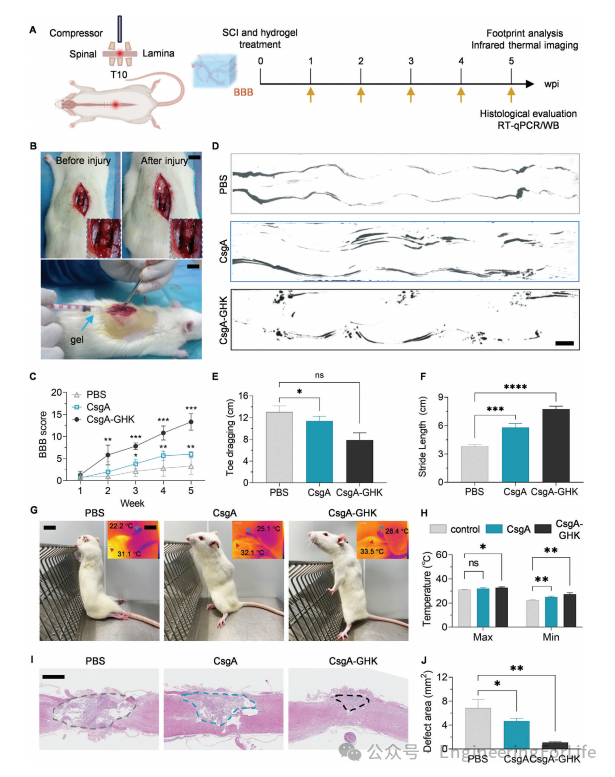
图6 SCI
后大鼠功能恢复情况的评价
CsgA-GHK水凝胶显示出合适的力学性能、特殊的抗炎特性和促进NSCs分化为神经元的能力,接下来继续评估水凝胶在SCI大鼠模型中的应用效果。实验时间线原理图如图6A所示。为了评估SCI后大鼠的功能恢复,采用BBB运动评估。手术过程如图6b所示。脊髓压迫损伤后,动物的双侧后肢立即出现完全瘫痪(0分)(图6C)。SCI后5周,对照组的后肢BBB评分不超过5分,说明自愈合能力有限。相比之下,CsgA-GHK组在术后的前2周内表现出有统计学意义的运动功能恢复(图6C)。在CsgA水凝胶组中,运动功能与损伤后2周的PBS组相当,但在SCI后第3周有显著改善,尽管其程度远低于CsgA-GHK水凝胶(图6C)。这些结果表明,
功能水凝胶能提高大鼠的运动恢复能力。
到术后第五周,大多数植入CsgA-GHK水凝胶的大鼠评分为13分,而使用CsgA水凝胶治疗的大鼠评分为5分,PBS组的大鼠评分为3分(图6D-F)。这些结果表明,
CsgA-GHK水凝胶显著增强SCI后的功能恢复
。使用红外热成像仪测量大鼠的后肢和体温,发现水凝胶处理后体温升高,特别是与PBS和CsgA组相比,CsgA-GHK水凝胶处理后的后足温度显著升高(图6G、H)。同样,组织HE染色也观察到正常的脊髓形态(图6I)。CsgA-GHK水凝胶减少术后5周的空泡化和缺损面积(图6J)。
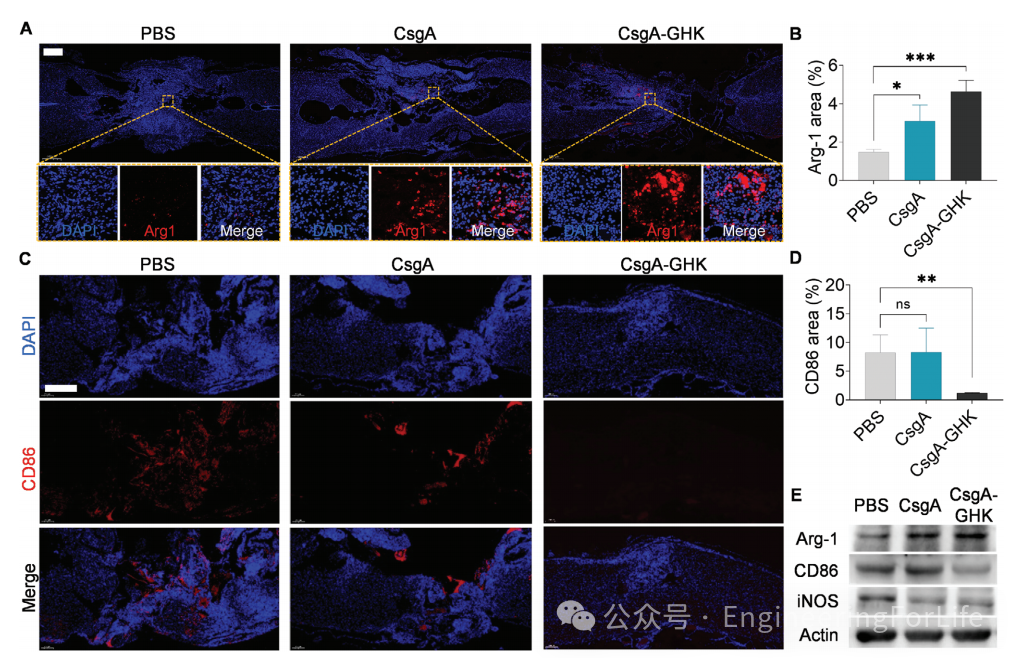
图7 SCI后炎症抑制作用的评价
与PBS组相比,水凝胶处理组在损伤部位的Arg-1阳性细胞的密度明显升高(图7A)。特别是在CsgA-GHK组中,Arg-1的荧光面积明显大于PBS组(图7B)。在损伤部位中心,PBS组和CsgA组的促炎因子CD86的免疫荧光(IF)强度增加,超过CsgA-GHK组(图7C、D)。WB结果进一步证实CsgA-GHK水凝胶的移植降低促炎因子CD86和iNOS蛋白的表达,同时提高抗炎因子Arg-1的水平(图7E)。以上结果表明,
GHK肽可以在早期抑制炎症,有效缓解长期慢性炎症,从而强调CsgA-GHK水凝胶的免疫调节特性。
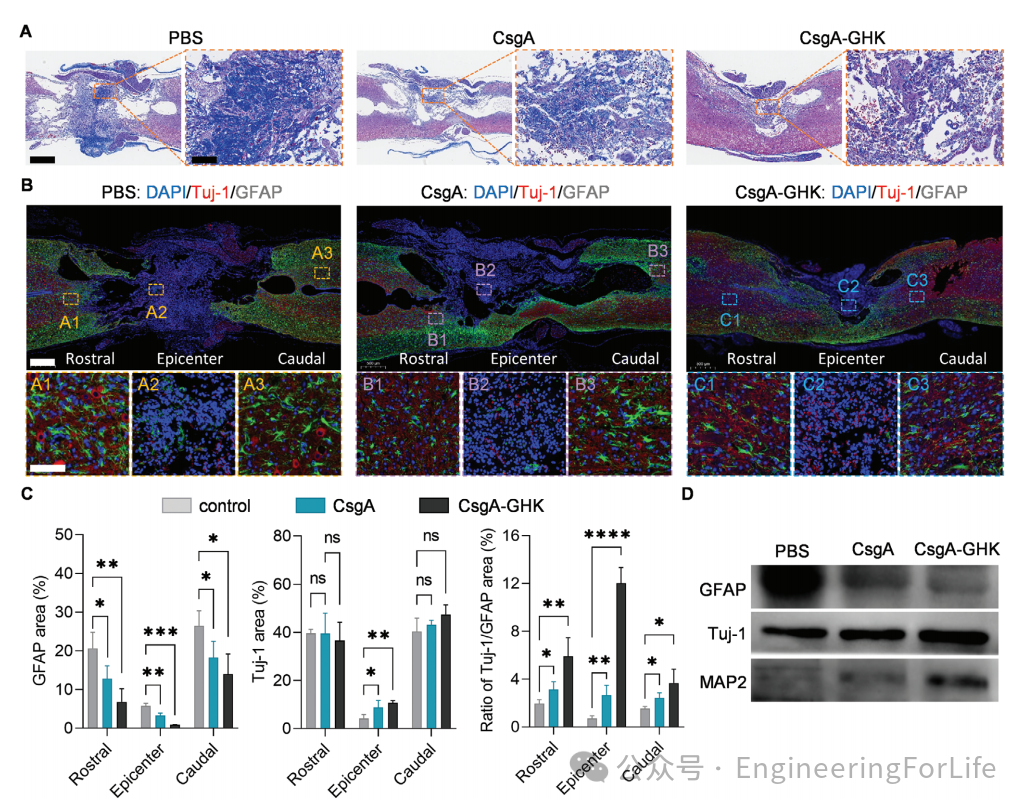
图8 SCI后神经元的再生
为进一步探讨CsgA-GHK水凝胶治疗SCI后功能恢复的机制,分析脊髓组织的组织学变化,评估损伤部位的神经再生和星形胶质瘢痕形成。与PBS组相比,水凝胶植入导致胶原含量降低,CsgA-GHK组在SCI部位的胶原积累很少(图8A)。在CsgA和CsgA-GHK水凝胶组中,Tuj-1蛋白在病变区域中心高表达,而在PBS组中表达相对较少,但表达没有显著差异(图8B)。这些观察结果表明,
CsgA和CsgA-GHK水凝胶促进神经元侵入损伤部位中心
(图8C)。WB分析与免疫荧光结果显示,两个神经元标记(Tuj1、MAP2)的表达,CsgA-GHK组明显高于CsgA水凝胶和PBS组,而CsgA-GHK组病变部位GFAP的表达明显低于CsgA组和PBS组(图8D)。
全文小结
总之,
本研究报道了一种基于CsgA重组蛋白的单组分水凝胶用于SCI治疗。CsgA与GHK的融合不仅利用CsgA的自组装特性,而且还利用GHK的治疗潜力,为制备活性蛋白生物材料提供一种模块化方法
。CsgA-GHK蛋白通过自组装纳米原纤维的纠缠形成水凝胶,排除在其他系统中繁琐的制备程序或化学交联剂。重要的是,
CsgA-GHK水凝胶具有与脊髓组织相匹配的力学性能,使其适合于SCI治疗
。水凝胶中的活性模块显示出显著的抗炎特性。体外实验表明,
CsgA-GHK水凝胶有效促进M2小胶质细胞极化,清除ROS,增强NSCs的神经元分化,减少胶质细胞分化
。此外,水凝胶有效抑制SCI部位的炎症,从而改善损伤微环境。这种协同治疗方法显著改善神经元的功能再生,减少瘢痕组织的形成,并最终恢复运动功能。考虑到多种具有自组装能力的蛋白质的可用性和多种生物活性肽模块的存在,因此本研究将提高设计基于活性蛋白软材料的前景,以推进SCI治疗和其他生物医学干预。
参考资料
:
https://doi.org/10.1002/advs.202405054
来源:
EngineeringForLife
声明:仅代表作者个人观点,用于研究用途,作者水平有限,如有不科学之处,请在下方留言指正!






