
对大部分的同学来说,
文章发在
10分以上的杂志上基本属于遥不可及的范畴了,特别是很多专业领域的顶级杂志也就5分左右。
所以,在很多单位,文章发在了10分以上的杂志上,不说在单位里面横着走,至少也是一段时间里的热点话题了。但是,很多人一听说文章发在
Nature Communication(NC)上,似乎就释然了:
原来是NC,怪不得呢!灌水杂志,谁还不能发啊!
似乎,NC与PMOS一样,是人人可以灌水和看轻的。
今天本宫就介绍一篇发表在
NC上研究
lncRNA促进肝纤维化的
文章,大家可以看看这篇文章是不是如同某些同学说的那样水?
这篇文章是7月26刚刚发表的,研究的
是新lncRNA LFAR1通过激活TGFβ和Notch通路促进肝纤维化这一主题:

文章的通讯作者是天津医科大学的洪伟教授,
洪教授去年申请到的国自然面上项目就是研究
lncRNA LFAR1在肝纤维化中作用的:

面上项目获得资助后一年内就发了NC,又有多少人能做到呢?
下面就让我们假设我们是研究团队,一步步地分析思路。
首先,我们明确研究方向,我们是
肝胆科的大夫,肯定研究肝胆疾病,肿瘤做的人太多了,
申请基金肿瘤口挤破头
,我们就选个肝纤维化吧(
一、
确定疾病类型
)。最近听了X湿兄的讲座,觉得
lncRNA相当靠谱(
到底有多靠谱,单击文末“阅读原文”报名参加8月在北京举办的讲座
)
,就研究下lncRNA在肝纤维化中的作用机制吧(
二、选定研究的基因类型
)。我们的研究是以lncRNA为目标,那么
lncRNA在肝纤维化发生的过程中产生了怎么变化?因何而变化?它的变化进而影响了什么?(
三个问题
)
这些问题是我们接下来的研究需要解决的问题。当然了,上述问题可以部分解决,相应的文章深度也会不同。
先说lncRNA在肝纤维化发生的过程中是如何变化的?
要研究这个,自然
需要样本,样本哪里来?来咱这看肝纤维化的又不开刀啥的,没有组织样本,咱只能研究研究老鼠了(
三、确定研究对象
)。肝纤维化的动物模型也是比较成熟的,注射CCl4就好了,不算太复杂。如何确定其中的变化?有钱就自己做测序,省钱就挖挖别人的测序数据,再到自己构建的动物模型中进行PCR验证,结果同样靠谱。
有了测序结果怎么筛潜在的值得研究的lncRNA?
1、表达量差异够显著;2、有潜在的生物学意义
(与肝纤维化相关的mRNA做共表达分析初步验证它们之间的表达相关性)。
到这里我们应该已经有两部分实验结果了:
1)动物模型成功构建的结果
(组织形态学和生化指标共同确定模型构建成功);
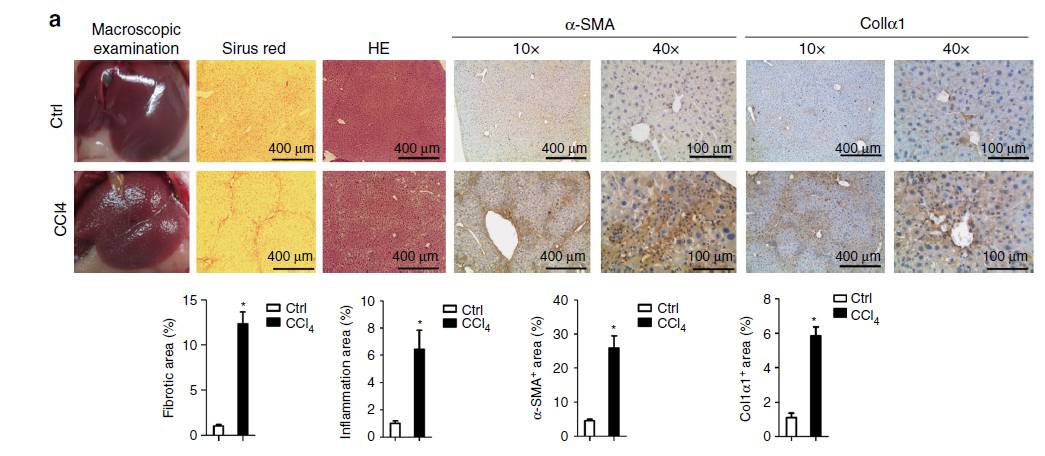

2)lncRNA的测序(或生信分析)的结果
(热图表示差异基因以及后续的PCR验证)。
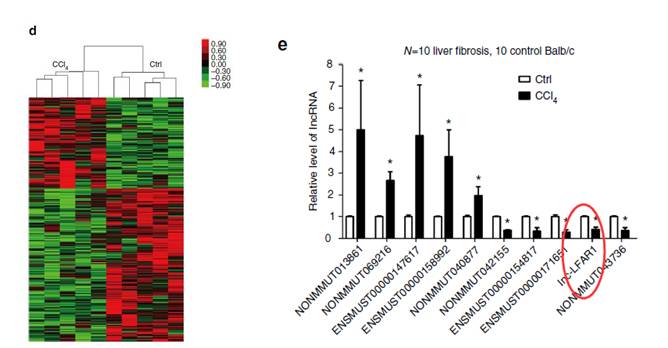
上面的结果表明这10个lncRNA在肝纤维化的过程中都挺“
特殊
”的,究竟该翻哪个的牌子,本宫很是纠结。于是本宫在多个组织的纤维化和非纤维化的样本中分别检测上述lncRNA的表达量,结果发现lncRNA-LFAR1在
肝纤维化中具有非常显著的组织特异性
,
表达量高且差异显著
。所以最后,我们翻了lncRNA-LFAR1的牌子。
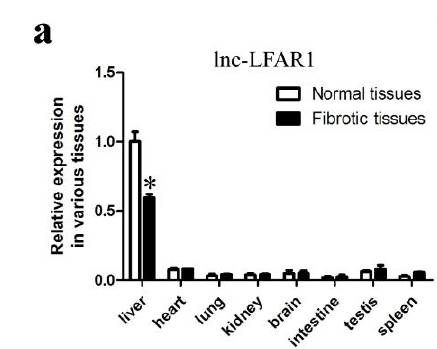
lncRNA-LFAR1在不同组织中的表达量
有关表达量变化的研究似乎结束了,但是看了一下文献中所描述的肝纤维化的发展过程,似乎哪里不对。

文献中说肝纤维化是由肝细胞(HC)损伤和肝星形细胞的激活(HSC)共同作用的结果,这两个细胞在肝纤维化的过程中似乎处于此消彼长的状态,而我们做的测序是组织样本的测序,并非单细胞测序,样本中各种细胞类型都有,所以说
同样的分子在不同类型的细胞中的作用机制很有可能是不同的
。

lncRNA-LFAR1在不同细胞中的表达量
此外,动物建模的过程是一个比较漫长的过程,基因的表达可能会随时间变化,lncRNA-LFAR1在这一过程中是如何变化的,也是需要我们研究的。
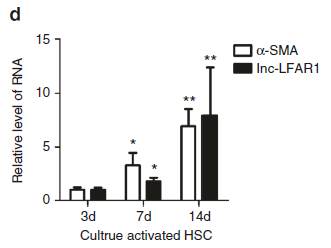
α-SMA and lnc-LFAR1在HSC中不同时间的表达量
要研究lncRNA-LFAR1影响了什么,我们可以设计敲减和过表达实验,以及挽救实验,结合测序进行下游信号通路的检测。不做测序的话可以直接通过文献搜索,瞄准疾病直接相关的下游通路进行检测。
结合测序的我们叫有的放矢,不做测序的我们叫盲狙
。我们通过生物信息学分析结合后续实验验证(PCR、WB)发现lncRNA-LFAR1影响了下游一大票与肝纤维化相关的基因以及激活Notch信号通路。
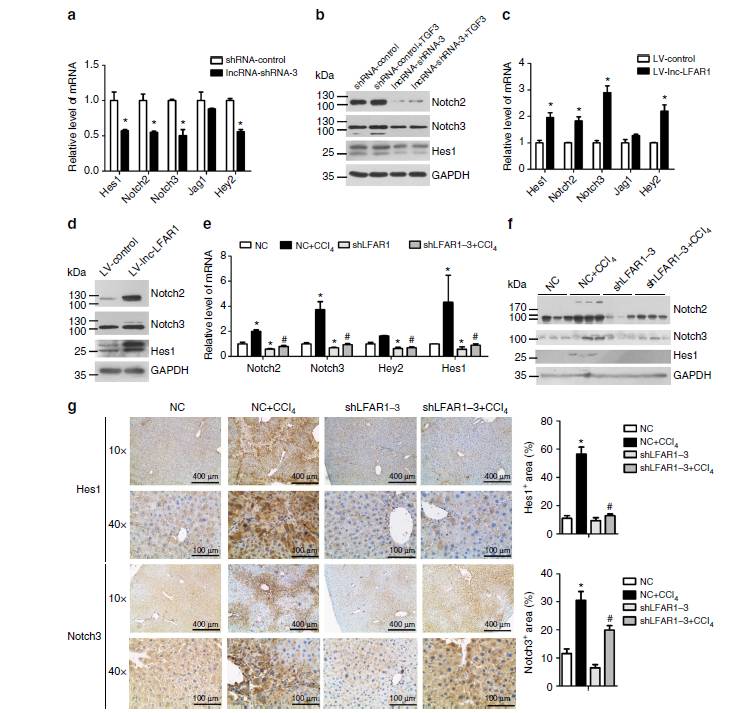
下游机制我们可以通过敲减过表达,检测下游基因表达变化进行研究,而上游机制我们得首先通过查阅文章了解些背景资料,筛选潜在的目标。
肝纤维化的过程中,TGFβ可以促进HSC的激活,而激活的HSC能够进一步自分泌TGFβ维持活化过程。
所以我们在设计挽救实验的时候,将TGFβ处理作为另一个实验条件,
即lncRNA-LFAR1能够挽救TGFβ诱导的HSC的活化
。
但是我们知道TGFβ不可能直接影响到lncRNA-LFAR1,中间应该还有一个牵线的家伙(转录因子)
。通过检索肝纤维化过程中差异表达的转录因子,我们发现Smad2/3是潜在目标,接下来我们就验证Smad2/3和lncRNA-LFAR1的关系,包括敲减过表达实验,CHIP实验还有荧光素酶实验,参见
寻找分子差异表达的上游机制(二)
。
其实文章机制做到这里算是可以了,不过我们运气不错,偶然间又发现
lncRNA-LFAR1还能上调Smad2/3
,怎么调控的?
ceRNA机制?RIP实验结果表明lnc-LFAR1与AGO2没有作用关系(lnc-LFAR1没有调控相应的miRNA),说明不是ceRNA机制;免疫沉淀反应发现lnc-LFAR1与Smad2/3之间存在物理相互作用关系;ChIP实验表明lnc-LFAR1能够提高Smad2/3的启动子活性,促进Smad2/3下游基因的转录。此外我们还通过生物信息学分析结合后续验证发现也被lnc-LFAR1激活。
最后,我们把研究的关键分子:
lncRNA LFAR1和TGFβ/Smad通路之间的调控关系在肝纤维化中的作用
通过一张图画出来:
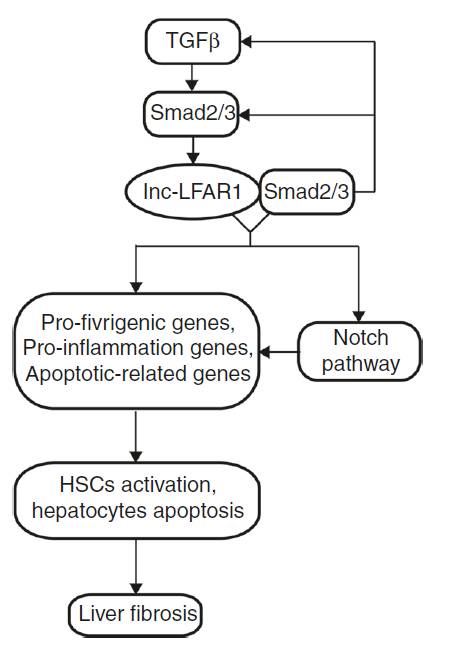
TGFβ促进Smad2/3磷酸化,Smad2/3活化促进lnc-LFAR1转录,lnc-LFAR1反过来能够增强Smad2/3的启动子活性形成正反馈回路,进而激活下游Notch通路,激活HSC,促进肝细胞凋亡,导致肝纤维化。
看到这里,还有同学觉得NC杂志水么?
-------分割线-------
科研竞争如逆水行舟,不仅则退。
国自然评审已经基本结束了,不管已经申请到了还是仍然在努力的道路上,大家时刻保持学习姿态,快快来学习一下小张团队系列讲座
《SCI文章模式及案例分享(lncRNA为例)》
已经成功在上海、杭州、武汉、广州举办,非常感谢大家多日以来的关注,
下一站:北京
。
小张系列免费讲座日程安排如下:
|
城市
|
时间
|
地点
|
人数
|
状态
|
|
上海
|
6月10日
|
华山医院
|
132人
|
完成
|
|
杭州
|
7月2日
|
浙大华家池校区
|
91人
|
完成
|
|
武汉
|
7月16日
|
武汉协和医院
|
160人
|
完成
|
|
广州
|
7月22日
|
南方医本部(白云区)
|
215人
|
完成
|
|
北京
|
8月?日
|
待定(北协和?)
|
报名中
|
ing
|

这次不仅X师兄会为大家介绍lncRNA研究发表不同档次文章的套路,中科院的张博士还会为大家带来
最新最火的CRISPR/Cas9技术
在科研和课题设计中的应用专题。国自然评审的结果还有不到一个月就出来了,你不听听讲座为明年的基金准备吗?
讲座的报名链接见左下角的阅读原文。






